��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ڷ�Ӧ��N2+3H2 2NH3������ӦΪ���ȷ�Ӧ��������ͼ����ʾ����ȷ���ǣ�?��
2NH3������ӦΪ���ȷ�Ӧ��������ͼ����ʾ����ȷ���ǣ�?��
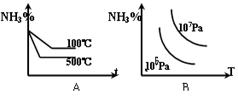
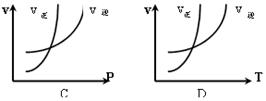
w.k.
�ο��𰸣�D
�����������
�����Ѷȣ���
2������� ��һ�����������ۼ��뵽װ��100mLijŨ�ȵ�ϡ������Һ�г�ַ�Ӧ��
��1��������ʣ��mg�����ۣ��ռ���NO����448mL����״���£���
�� ������Һ�е����ʵĻ�ѧʽ��_______________��
�� ԭ������Һ�����ʵ���Ũ��Ϊ��________________mol/L
��2����������-Һ���������μ���ϡ����ֱ���պò��ٲ�������Ϊֹ����������������ɺ���ɫ����ʱ������������ng��
�ٴ�ʱ��Һ�����ʵĻ�ѧʽ��__________��
��m-n��ֵΪ_____________g ��
����ij�ܱ������м���0.3molA��0.1molC��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��ı仯����ͼ�м�ͼ��ʾ����ͼ����ͼΪt2ʱ�̺�ı�������������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ����ı�һ�ֲ�ͬ��������������������ͬ����֪t3~t4��Ϊʹ�ô�������֪
t0~ t1��c ( B)δ�����ݡ�
��3���� t1=15s ����t0~ t1����CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ________________��

��4��t4~t5�θı������Ϊ____________��B����ʼ���ʵ���Ϊ______________��
��5��t5~t6��������A�����ʵ���������0. 03mol �����˹����������������Ƚ�������ΪakJ��д���÷�Ӧ���Ȼ�ѧ����ʽ________________________��
�ο��𰸣���1����Fe(NO3)2
? �� 0.8
��2����FeSO4 ��5.04
��3��0.004mol��L-1��s-1
��4����Сѹǿ��0.04mol
��5��3A(g)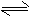 2C(g)+B(g)����H��+100akJ��mol-1
2C(g)+B(g)����H��+100akJ��mol-1
���������
�����Ѷȣ�һ��
3��ѡ���� ��3 mol M��2.5 mol N�����2 L���ܱ������У�������Ӧ�Ļ�ѧ����ʽΪ��
3M(g) + N(g) 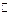 xP(g) + 2Q(g)��5min��Ӧ�ﵽƽ�⣬����Ӧǰ���¶Ȳ��䣬������ѹǿ��С����֪
xP(g) + 2Q(g)��5min��Ӧ�ﵽƽ�⣬����Ӧǰ���¶Ȳ��䣬������ѹǿ��С����֪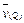 = 0.1mol��L��1��min��1��������˵��������ǣ�?��
= 0.1mol��L��1��min��1��������˵��������ǣ�?��
A��M��ƽ����Ӧ����Ϊ0.15 mol��L��1��min��1
B��ƽ��ʱN��ת����Ϊ25%
C��ƽ��ʱP��Ũ��Ϊ0.25 mol��L��1
D��ƽ��ʱ�����ڵ�ѹǿΪԭ����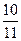 ��
��
�ο��𰸣�B
�����������
�����Ѷȣ���
4������� ��һ���¶��£����ݻ�Ϊ2L �������ڣ�ij��Ӧ�����ʣ���Ϊ���壩�����ʵ����淴Ӧʱ��ı仯������ͼ���Իش��������⣺
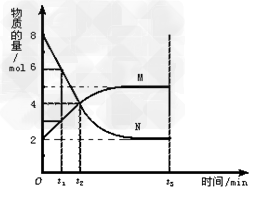
��1 ����t1��5S ����ǰ5S ��M ��ʾ�ķ�Ӧ����Ϊ__________?��
��2 ��t2ʱ������Ӧ����________������ڡ������ڡ���С�ڡ����淴Ӧ���ʡ�
��3 ������˵����ȷ����________
A��t2ʱ�̸÷�Ӧ�ﵽƽ��
B��t3ʱ�̸÷�Ӧ�ﵽƽ��
C����Ӧ��ʼʱ���������Ũ��Ϊ0
D���÷�Ӧ�����ǿ��Ըı��
�ο��𰸣���1 ��0.1mol/(L��s)?
��2?������?
��3 ��BD
���������
�����Ѷȣ�һ��
5������� ijһ�¶��½�1mol?N2��4mol?H2����һ���Ϊ2L���ܱ������У����������ѹǿΪ40Mpa����20min��Ӧ�ﵽƽ�⣬���NH3�ڻ��������ռ25%���������������1��N2��ƽ��ת���ʣ�?��2��H2��ƽ����Ӧ���ʣ�?��3��ƽ��ʱ�����ڵ�ѹǿ��
�ο��𰸣���������ʽ���ⷨ�����ƽ��ʱ����ֵ����ʵ�������������ʵ����ı仯��
��μӷ�Ӧ�ĵ��������ʵ���Ϊnmol
? ?N2 +3H2

? 2NH3��
��ʼ��mol����1? 4? 0
�仯��mol����n? 3n? 2n
ƽ�⣨mol����1-n? 4-3n? 2n?
����2n1-n+4-3n+2n=25%�����n=0.5
��1��N2��ƽ��ת����Ϊ0.5mol1mol��100%=50%
��N2��ƽ��ת����Ϊ50%��
��2��H2��ƽ����Ӧ����v��H2��=��n(H2)V��t=0.5mol��32L20min=0.0375?mol�ML��min��
��H2��ƽ����Ӧ����Ϊ0.0375?mol�ML��min��
��3��ѹǿ֮�ȵ������ʵ���֮�ȣ�ƽ��ʱ�����ڵ�ѹǿΪ(5-2n)mol1mol+4mol��40MPa=(5-2��0.5)mol1mol+4mol��40MPa=32MPa��
��ƽ��ʱ�����ڵ�ѹǿΪ32MPa��
���������
�����Ѷȣ�һ��