微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上制造镁粉是将镁蒸气在气体中冷却。可作为却气体的是(?)
①空气?②CO2?③Ar?④H2?⑤N2
A.①②
B.②③
C.③④
D.④⑤
参考答案:C
本题解析:略
本题难度:简单
2、选择题 将一定质量的Mg和Al的混合物投入2.0mol/L,250 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示。则下列说法正确的是(?)

A.当加氢氧化钠溶液体积为20mL时,溶液的pH值等于7
B.当加氢氧化钠溶液体积为20mL时,溶液中的溶质只有硫酸镁和硫酸铝
C.NaOH溶液的物质的量浓度为5 mol/L
D.生成的H2在标准状况下的体积为11.2 L
参考答案:C
本题解析:A错,当加氢氧化钠溶液体积为20mL时,溶液中溶质为硫酸镁、硫酸铝、硫酸钠,溶液的PH小于7;B错,当加氢氧化钠溶液体积为20mL时,溶液中溶质为硫酸镁、硫酸铝、硫酸钠;C正确,当加入氢氧化钠溶液体积为200mL时,氢氧化钠全部生成硫酸钠,已知硫酸的物质的量为0.5mol,所以氢氧化钠的物质的量为1mol,得NaOH溶液的物质的量浓度为5 mol/L;D错,氢氧化铝的物质的量为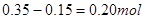 ;氢氧化镁的物质的量为0.15mol,由镁、铝守恒得镁的物质的量为0.15 mol,铝的物质的量为0.20mol;即生成氢应为0.45mol,生成的H2在标准状况下的体积为10.08 L;
;氢氧化镁的物质的量为0.15mol,由镁、铝守恒得镁的物质的量为0.15 mol,铝的物质的量为0.20mol;即生成氢应为0.45mol,生成的H2在标准状况下的体积为10.08 L;
本题难度:一般
3、简答题 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱.但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+.回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为______(用化学式表示).
(2)写出锌和氢氧化钠溶液反应的化学方程式______.
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是______.
①硫酸铝和氢氧化钠?②硫酸铝和氨水③硫酸锌和氢氧化钠④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式______.试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因______.
参考答案:(1)属铝和氢氧化钠反应生成偏铝酸钠和氢气,溶液中铝元素的存在形式为Na[Al(0H)4],故答案为:Na[Al(OH)4];
(2)根据题干信息得锌和氢氧化钠溶液反应的化学方程式为:Zn+2NaOH+2H2O=Na2[Zn(0H)4]+H2↑,故答案为:Zn+2NaOH+2H2O=Na2[Zn(0H)4]+H2↑;
(3)①硫酸铝中加氢氧化钠,先出现沉淀,然后沉淀消失,然后又出沉淀,向氢氧化钠中加硫酸铝没有现象,故用相互滴加的实验方法可以鉴别;
②硫酸铝和氨水不管是谁往谁中相互滴加是现象均是出现白色沉淀,用相互滴加的实验方法不可以鉴别;
③往硫酸锌中加氢氧化钠时,会出现白色沉淀,向氢氧化钠中加硫酸锌时,无现象,故用相互滴加的实验方法可以鉴别;
④往硫酸锌中加氨水时,会出现白色沉淀,向氨水中加硫酸锌时,无现象,故用相互滴加的实验方法可以鉴别;
故答案为:①③④;
(4)可溶性铝盐与氨水反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌,因为可溶性锌盐与氨水反应产生
的氢氧化锌可溶于过量的氨水中,生成Zn(NH3)42+,氨水的量不易控制.故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;可溶性锌盐与氨水反应产生的氢氧化锌可溶于过量
的氨水中,生成Zn(NH3)42+,氨水的量不易控制.
本题解析:
本题难度:一般
4、填空题 (14分)实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
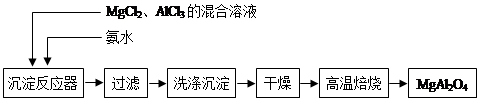
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式?。
(2)如图所示,过滤操作中的一处错误是?。判断流程中沉淀是否洗净所用的试剂是?。高温焙烧时,用于盛放固体的仪器名称是?。
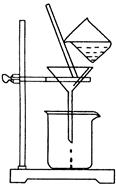
(3)在25℃下,向浓度均为0.01 mol・L-1的MgCl2和AlCl3混合溶液中逐滴 加入氨水,先生成?沉淀(填化学式),生成该沉淀的离子方程式?(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34。)
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
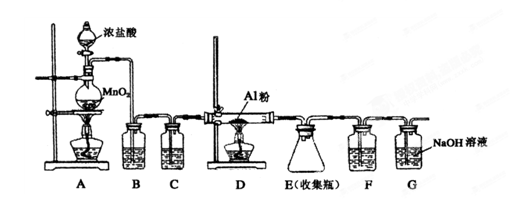
装置B中盛放饱和NaCl溶液,该装置的主要作用是?;F中试剂的作用是?;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为?。
(5)将Mg、Cu组成的1.96g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后的溶液中加入2 mol/L的NaOH溶液80 mL时金属离子恰好完全沉淀。则形成沉淀的质量为?g。
参考答案:(14分)(1)2Al(OH)3 + Mg(OH)2  ?MgAl2O4 + 4H2O(2分)
?MgAl2O4 + 4H2O(2分)
(2)漏斗下端尖嘴未紧贴烧杯内壁(1分)AgNO3溶液(1分)坩埚(1分)
(3)Al(OH)3(1分)? Al3++3NH3・H2O=Al(OH)3↓+3NH4+?(2分)
(4)除去HCl(1分);吸收水蒸气(1分)?碱石灰(2分)
(5)4.00(2分)
本题解析:(1)MgCl2、AlCl3的混合溶液与氨水反应生成氢氧化镁和氢氧化铝沉淀,经过滤、洗涤、干燥后高温焙烧生成MgAl2O4,所以该反应的反应物是氢氧化镁和氢氧化铝,产物是MgAl2O4和水,化学方程式为2Al(OH)3 + Mg(OH)2  ?MgAl2O4 + 4H2O;
?MgAl2O4 + 4H2O;
(2)过滤存在中符合“一贴二低三靠”过滤操作中的一处错误是漏斗下端尖嘴未紧贴烧杯内壁;氯化镁与氯化铝在与氨水反应生成沉淀时,沉淀上易附着有氯离子,检验氯离子所用的试剂是硝酸银溶液;高温焙烧时,用于盛放固体的仪器是坩埚;
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11>Ksp[Al(OH)3]=3×10-34。所以先生成溶解度小的沉淀Al(OH)3;生成Al(OH)3沉淀的离子方程式为Al3++3NH3・H2O=Al(OH)3↓+3NH4+
(4)因为无水AlCl3遇潮湿空气即产生大量白雾,所以制备氯化铝时要求氯气是干燥的,而且浓盐酸易挥发,挥发的HCl也与Al反应,所以需除去HCl,装置B中盛放饱和NaCl溶液,目的就是除去氯气中的HCl;装置C中盛放浓硫酸,目的是干燥氯气;F中也盛放浓硫酸,目的是吸收G中的水蒸气,防止水蒸气进入D中;可用一件仪器装填适当试剂后也可起到F和G的作用,该试剂既能吸收水,还能吸收多余的氯气,所以应该是碱石灰;
(5)Mg、Cu都是2价金属,沉淀的质量也即Mg、Cu的质量加上OH-的质量。该过程中生成NO气体0.896L(标准状况)物质的量是0.04mol,则Mg、Cu失去电子的物质的量等于NO3-得电子的物质的量也等于OH-的物质的量,即n(OH-)=0.04mol×3=0.12mol,所以沉淀的质量是1.96g+0.12mol×17g/mol=4g。
本题难度:一般
5、选择题 逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是
[? ]
A.单质都是由同种元素组成的,只含一种元素的物质一定是纯净物
B.金属铝排在金属活动性顺序表中氢元素的前面,铝与酸反应一定放出氢气
C.中和反应都有盐和水生成,有盐和水生成的反应都属于中和反应
D.氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物
参考答案:D
本题解析:
本题难度:简单