��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����й�ʵ���˵����ȷ����
A����ȥ�����е�ͭ�ۣ���������Ũ������ȷ�Ӧ����й���
B�������κ������Լ��Ϳ��Լ���NaOH��Һ��Al2��SO4��3��Һ
C���Ʊ�Fe��OH��3���壬ͨ���ǽ�Fe��OH��3����������ˮ��
D��ij��Һ���������ܲ���ʹ����ʯ��ˮ����ǵ����壬�����Һһ�����д���CO32-
�ο��𰸣�B
���������A��������ͭ������Ũ������ȷ�Ӧ��B��ȷ��C�����Ʊ�Fe��OH��3���巽��Ϊ����ڵ�����ˮ����ε��뱥�͵��Ȼ�����Һ5��6�Σ����������������Һ�ʺ��ɫΪֹֹͣ���ȵõ������������壻D����ij��Һ���������ܲ���ʹ����ʯ��ˮ����ǵ����壬�����Һ�п�����CO32-��HCO3��
�����Ѷȣ�һ��
2��ѡ���� �����й�ʵ���������ȷ���� ��?��
A���к��ȵIJⶨʵ�����õ��IJ����������¶ȼơ��ձ������β��������
B���ζ�����ʹ��ǰ��������Ƿ�©ˮ
C��ij�εζ���ζ��ܵĶ���Ϊ20.3ml
D����ʽ�ζ��ܲ�����ȡ��������
�ο��𰸣�C
����������ζ��ܵĶ�����0.01ml��ѡ��C����ȷ������ѡ�����ȷ�ģ���ѡC��
�����������ǻ���������Ŀ��飬�ѶȲ���ѧʵ�鳣��������ʹ�÷����ͻ�ѧʵ����������ǽ��л�ѧʵ��Ļ������Ի�ѧʵ��Ŀ����벻����ѧʵ��Ļ�������������������Ҫ���Գ���������ѡ�á�ʵ���������Ϊ���ģ�ͨ����ʲô��Ϊʲô���������ص㿼��ʵ����������Ĺ淶�Ժ�ȷ�Լ��������֪ʶ���ʵ�������������
�����Ѷȣ���
3��ѡ���� ������һЩ���õ�Σ��Ʒ��־������������Ƶ�����Ӧ���ı�ǩ�ǣ�?��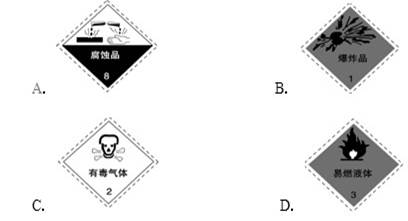
�ο��𰸣�A
������������鳣����Σ��Ʒ��־��ʶ�����жϡ��������Ƽ���ǿ�ĸ�ʴ�ԣ�����ѡ��A��ȷ����ѡA��
�����Ѷȣ���
4��ʵ���� ������ͼ��ʾ����������8������ش𣺢�H2����O2����CH4����HCl����NH3����CO2����H2S����SO2��

��1������ƿ�Ǹ���ģ�����B�ڽ������ռ���������___________����A�ڽ������ռ���������_____________��
��2��������ƿ�ڳ���ˮ�����ռ���������______________������Ӧ��_____�ڽ��롣
��3��������ƿ�м���������Ũ���ᣬ���������������������______________������Ӧ��__________�ڽ��롣?
�ο��𰸣���1���ڢܢޢߢ� ��2�֣�?�٢ۢ�?��2�֣� ��2���٢ڢ�?��2�֣�? A?��1 �֣�
��3���٢ڢۢܢޢ�?��2�֣�? B?��1 �֣�
�����������1������ƿ�Ǹ���ģ�����B�ڽ������ռ����壬��˵��������ܶ�Ӧ���Ǵ��ڿ����ģ���ѡ�ڢܢޢߢࣻ��֮��A�ڽ������ռ����������ܶ�С�ڿ����ģ���ѡ�٢ۢݡ�
��2��������ƿ�ڳ���ˮ�����ռ�������Ӧ����������ˮ�ģ���˴�ѡ�٢ڢۡ���ʱ����Ӧ��A�ڽ��롣
��3��������ƿ�м���������Ũ���ᣬŨ�������ǿ�����ԣ��������ԣ����Կ�������������������Т٢ڢۢܢޢ࣬������H2S������Ũ��������ʱ����Ӧ��B�ڽ��롣
����������������ռ������ǣ�1.��ˮ���������ڲ�������ˮ�����塣����������������2.�����ſ������������ڱȿ����ܶȴ�����ˮ�����壬���������̼��������3�������ſ������������ڱȿ����ܶ�С������ˮ�����壬���簱������Ҫѧ��������ס������������á�
�����Ѷȣ�һ��
5��ѡ���� ̼��Ƴ����������Ħ������ijͬѧ�����һ���Ʊ�̼��Ƶķ�����������ͼ���£�������ʯ��ʯ��������SiO2��

�ش��������⣺
��1���������110��ʯ��ʯ�õ�����66�֣���״�������ɶ�����̼�����Ϊ?L��ʯ��ʯ��̼��Ƶ���������Ϊ?%��
��2������ڢٲ���Ӧ��ȫ���У���ڢڲ���Ӧ���˺�õ��IJ����������ijɷ�Ϊ?��
��3���ڢ۲���Ӧһ�㲻����ͨ��CO2����Ҫԭ����?����Ӧ�����ӷ���ʽΪ?��
��4��CaCO3��һ������Һ���ʣ�25��ʱ��KSP=2.8��10-9���ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2.0��10-4mol/L�������ɳ�������CaCl2��Һ�����ʵ���Ũ����С��?��
��5��ijѧ����ʯ��ʯΪԭ�ϣ��������һ���Ʊ�̼��Ƶ�ʵ�鷽����������ͼ���£�

��ǰһ������Ƚϣ��÷������ŵ���?��
�ο��𰸣���ÿ��2�֣���14�֣�
��1��2.24��107L ��?90.0?��4�֣�
��2��CaSiO3?(2��)
��3��ͨ��CO2���������ƣ�ʹ���ɵ�̼�����CO2�������������ܽ� ��2�֣�
CaCO3+CO2+H2O=Ca2++2HCO3��?��2�֣�
��4��5.6��105mol/L?��2�֣�
��5������Ҫ���ȣ���������������ȼ�ϵ���Ⱦ��2�֣�
���������
��1�� ����̼��Ʒֽ⣺
����̼��Ʒֽ⣺
CaCO3 CaO? + ?CO2 ��?��m
CaO? + ?CO2 ��?��m
100? 56? 22.4 ?44
100��106g?V ?44��106g
�������ɶ�����̼�����Ϊ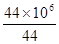 mol��22.4L/mol=2.24��107L
mol��22.4L/mol=2.24��107L
ʯ��ʯ��̼��Ƶ���������Ϊ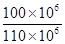 ?��100%=90.9%
?��100%=90.9%
��2��̼��Ƴ��˷ֽ⣬������������SiO2������Ӧ��SiO2+CaCO3=CaSiO3+CO2
���Բ���Һ�������ijɷ���CaSiO3��
��3����CO2����ʱ���������̼��Ʒ�Ӧ��CaCO3+CO2+H2O�TCa2++2HCO3-��4������Һ��QC��KSPʱ���γɳ�����C��Ca2+����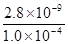 mol?L-1=2.8��10-5mol?L-1��
mol?L-1=2.8��10-5mol?L-1��
��������ǰCaCl2��Һ�����ʵ���Ũ����СΪ5.6��10-5?mol?L-1
��5������ǰһ������Ƚϣ���֪�Ʊ����̲���Ҫ���ȡ��������ȡ�
�����Ѷȣ�һ��