微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列分离方法中,和物质的溶解度无关的是
A.升华
B.萃取
C.纸上层析
D.重结晶
参考答案:A
本题解析:A、固体不经过液体直接变为气体的叫升华,与物质的熔沸点有关系,与溶解度无关,A正确;B、萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,与溶解度有关系,B不正确;C、纸上层析是利用混合物中各组分在固定相和流动相中的溶解度不同而达到分离目的,与溶解度有关系,C不正确;D、结晶法适用于不同溶质的溶解度受温度影响不同而分离的一种方法,重结晶是将晶体溶于溶剂或熔融以后,又重新从溶液或熔体中结晶的过程,与溶解度有关系,D不正确,答案选A。
本题难度:简单
2、填空题 以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成份为Fe(CrO2)2]为主要原料生产重铬酸钠晶体( Na2Cr2O7・2H2O)的主要工艺流程如下:
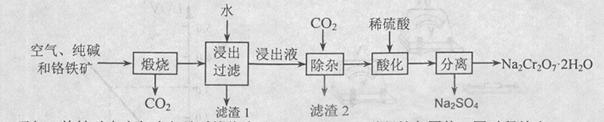
己知:铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,同时A12O3+Na2CO3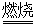 2NaAlO2+CO2↑。请回答:
2NaAlO2+CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为____。
(2)滤渣1的成分为________,滤渣2的成分为____。
(3)将滤渣l放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是?。
(4)铬铁矿中的Al2O3杂质在工业上可用来冶炼铝,该化学方程式为
(5)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7 mo1/L以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀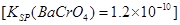 ,再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于?mol/L,后续废水处理方能达到国家排放标准。
,再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于?mol/L,后续废水处理方能达到国家排放标准。
②还原法: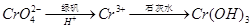 。写出酸性条件下 CrO42-与绿矾在溶液中反应的离子方程式?。
。写出酸性条件下 CrO42-与绿矾在溶液中反应的离子方程式?。
(6)某高效净水剂是由K2FeO4得到的,工业上以溶液W、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的化学方程式是??。
参考答案:(1)+3(1分)
(2)Fe2O3?Al(OH)3(各1分)(其它合理答案也可)
(3)取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红,证明有Fe3+(其它合理答案也可)(2分)
(4)2 Al2O3 4Al + 3O2↑(1分)
4Al + 3O2↑(1分)
(5)①2.4×10-4(2分)②CrO42-+3Fe2++8H+=Cr3++3Fe3++4H2O(3分)
(6)Fe2(SO4)3 + 3KClO + 10KOH = 2K2FeO4 + 3K2SO4 + 3KCl + 5H2O(3分)
本题解析:(1)在铬铁矿Fe(CrO2)2中,Fe的化合价为+2,所以Cr的化合价为+3,
(2)含杂质的铬铁矿经煅烧、溶于水后,只有氧化铁不溶于水,作为滤渣除去,所以滤渣1的成分是Fe2O3,此时溶液为Na2CrO4和 NaAlO2的混合液,通入CO2气体会和NaAlO2反应产生Al(OH)3,所以滤渣2的成分是Al(OH)3,
(3)将滤渣l放入稀硫酸溶解后得溶液W Fe2(SO4)3,检验Fe3+的方法是取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红,证明有Fe3+
(4)工业上用电解熔融氧化铝的方法来得到铝,化学方程式为2 Al2O3 4Al + 3O2↑,
4Al + 3O2↑,
(5)①Ksp(BaCrO4)=1.2×10-10,c(CrO42-)<=5.0×10-7 mo1/L,所以c(Ba2+)>=1.2×10-10/5.0×10-7=2.4×10-4 mo1/L, ②酸性条件下 CrO42-与绿矾FeSO4?7 H2O反应,CrO42-作氧化剂,绿矾作还原剂,其离子方程式为CrO42-+3Fe2++8H+=Cr3++3Fe3++4H2O
(6)W 为Fe2(SO4)3,以溶液Fe2(SO4)3、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的化学方程式是Fe2(SO4)3 + 3KClO + 10KOH = 2K2FeO4 + 3K2SO4 + 3KCl + 5H2O
本题难度:困难
3、填空题
?
| A
| B
| C
| D
| E
| F
| G
|
A
| ―
| ―
| ―
| ―
| ―
| ―
| ↓
|
B
| ―
| ―
| ―
| ―
| ↓
| ↓
| ↓
|
C
| ―
| ―
| ―
| ↓
| ―
| ↓
| ↓
|
D
| ―
| ―
| ↓
| ―
| ↓
| ↓
| ↓
|
E
| ―
| ↓
| ―
| ↓
| ―
| ↓
| ―
|
F
| ―
| ↓
| ↓
| ↓
| ↓
| ―
| ↓
|
G
| ↓
| ↓
| ↓
| ↓
| ―
| ↓
| ―
|
有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示。表中“↓”表示生成沉淀或微溶化合物,“―”表示观察不到明显变化。试回答下面问题:
(1)A的化学式是_________,G的化学式是_________,判断理由是____________________。
(2)写出其余几种物质的化学式:B:______________,C:______________,D:______________,E:______________,F:______________。
参考答案:
(1)KCl? AgNO3?混合时只生成一种沉淀的是KCl,生成的沉淀是AgCl,所以A是KCl,G是AgNO3
(2)Na2SO4? MgCl2? Na2CO3? Ca(NO3)2? Ba(OH)2
本题解析:
分析题给7瓶物质两两反应,只有A和G反应,只生成一种沉淀,从而确定A为KCl;G为AgNO3溶液;又F除与A不产生沉淀外,可产生五种不溶物,可确定F为Ba(OH)2;又B与E、F、G产生三种沉淀,可推知B为Na2SO4;又E与B、D、F产生三种沉淀,可推出D为Na2CO3;C与D、F、G产生三种沉淀推知C为MgCl2,最后剩余E为Ca(NO3)2溶液。
本题难度:简单
4、简答题 对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、渗析、加热分解等.下列各组混合物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用______的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒.
(2)提取碘水中的碘,用______方法.
(3)除去食盐溶液中的水,可采用______的方法.
(4)海水淡化,一般采用______的方法.
(5)除去氧化钙中的碳酸钙可用______的方法.
(6)除去淀粉中的食盐可用______的方法.
参考答案:(1)可用过滤的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒,故答案为:过滤;?
(2)碘易溶于水有机溶剂,根据在不同溶剂中的溶解度不同,可选用苯或四氯化碳进行萃取,
故答案为:萃取;?
(3)水在加热条件下易挥发,可用蒸发的方法除去食盐溶液中的水,故答案为:蒸发;?
(4)海水的淡化是将食盐和水分离,得到水,可用蒸馏的方法分离,故答案为:蒸馏;
(5)碳酸钙加热分解生成氧化钙,可用加热分解法分离,故答案为:加热分解;?
(6)淀粉属于胶体,不能透过半透膜,可用渗析的方法分离,故答案为:渗析.
本题解析:
本题难度:一般
5、选择题 下列分离或提纯物质的方法错误的是( )
A.用渗析的方法精制氢氧化铁胶体
B.用加热的方法提纯含有少量碳酸氢钠的碳酸钠
C.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
D.用盐析的方法分离、提纯蛋白质
参考答案:A、胶体的微粒直径在1nm~100nm之间,不能透过半透膜,可用渗析的方法分离,故A正确;
B、碳酸氢钠加热时易分解,生成碳酸钠和水,所以可用加热的方法提纯含有少量碳酸氢钠的碳酸钠,加热时水挥发,没有引入其它杂质,故B正确;
C、硫酸钡和碳酸钡都难溶于水,不能用溶解、过滤的方法分离,应加入盐酸,充分反应后过滤、洗涤,故C错误;
D、蛋白质在轻金属盐溶液中的溶解度变小,可用盐析的方法分离,故D正确.
故选C.
本题解析:
本题难度:一般