微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态))
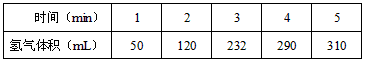
(1)哪一时间段___________(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大,原因是_____________。
(2)哪一段时段的反应速率最小__________________,原因是_________________________。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)______________。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)________________。
参考答案:(1)2~3min;因为该反应是放热反应,2~3min时温度高
(2)4~5min;因为4~5min是H+浓度小
(3)0.1 mol/(L・min)
(4)AB
本题解析:
本题难度:一般
2、实验题 试用实验室提供的下列试剂,设计两个原理不同的简单实验(只要写出两个实验方案即可),证明镁元素的金属性比铝强。试剂:Mg条、Al丝、AlCl3溶液、MgCl2溶液、稀HCl、NaOH溶液
实验方案:①__________________;
实验方案:②__________________。
参考答案:实验方案①:用Mg条和Al丝分别与盐酸反应,观察其反应速率的快慢
实验方案②:将Mg条和Al丝靠在一起,插入稀HCl中,观察其气泡产生的情况
本题解析:
本题难度:一般
3、实验题 (12分)某同学进行实验研究时,欲配制1.0 mol・L-1 Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2・8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。为探究其原因,该同学查得Ba(OH)2・8H2O在283 K、293 K和303 K时的溶解度(g/100 g H2O)分别为2.5、3.9和5.6。
(1)假设试剂由大量Ba(OH)2・8H2O和少量BaCO3组成。设计实验方案,进行成分检验。写出实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
实验步骤
| 预期现象和结论
|
步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。
| ?
|
步骤2:取适量滤液于试管中,滴加稀硫酸。
| ?
|
步骤3:取适量步骤1中的沉淀于试管中,________。
| ?
|
步骤4:?
| ?
|
(2)将试剂初步提纯后,准确测定其中Ba(OH)2・8H2O的含量。实验如下:
①配制250 mL约0.1 mol・L-1 Ba(OH)2溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,_______ _,将溶液转入________中,洗涤,定容,摇匀。
_,将溶液转入________中,洗涤,定容,摇匀。
②滴定:准确量取25.00 mL所配Ba(OH)2溶液于锥形瓶中,滴加指示剂,将______(填“0.020”、“0.05”、“0.1980”或“1.5”)mol・L-1盐酸装入50 mL酸式滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐酸V mL。
③计算Ba(OH)2・8H2O的质量分数=________(只列出算式,不做运算)。
(3)室温下,_______( 填“能”或“不能”)配制1.0 mol・L-1 Ba(OH)2溶液。
填“能”或“不能”)配制1.0 mol・L-1 Ba(OH)2溶液。
参考答案:(共12分)
(1)(每空1分,共5分)
步骤2:
出现白色沉淀,说明该试剂中有Ba2+存在
步骤3:滴加稀盐酸,连接带塞导气管将产生的气体导入澄清石灰水中
澄清石灰水变浑浊,说明该试剂含有BaCO3[来源:]
步骤4:取步骤1中的溶液于烧杯中,用pH计测定其pH
pH明显大于9.6,说明该试剂含有Ba(OH)2
本题解析:略
本题难度:一般
4、填空题 (15分)氯化铁是常见的水处理剂,无水FeCl3的熔点为555K、沸点为588K。工业上制备无水FeCl3的一种工艺如下:

(1)试写出吸收塔中反应的离子方程式:____________________________。
(2)已知六水合氯化铁在水中的溶解度如下:
温度/℃
| 0
| 10
| 20
| 30
| 50
| 80
| 100
|
溶解度(g/100gH20)
| 74.4
| 81.9
| 91.8
| 106.8
| 315.1
| 525.8
| 535.7
|
?从FeCl3溶液中获得FeCl3・6H2O的方法是:?。
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的分子式为:?。
(4)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)= ?mol/L(已知:Ksp[Fe(OH)3]= 1.1×10-36)。
(5)FeCl3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c mol/L Na2S2O3溶液滴定用去V mL。
(已知:I2+2S2O32-=2I-+S4O62-)
①滴定终点的现象是:____________________________。
②样品中氯化铁的质量分数为:? ?。
③某同学根据上述方案,使用上述(2)中获得的FeCl3・6H2O样品代替无水氯化铁样品进行测定。通过计算发现产品中的质量分数大于100%,其原因可能是?。
参考答案:(1)2Fe2++Cl2=2Fe3++2Cl-(2分)
(2)加入少量盐酸加热浓缩,再冷却结晶(3分)
(3)Fe2Cl6(2分)
(4)1.1×10-6?(2分)
(5)①滴入最后一滴,溶液颜色由蓝色变为无色。(2分)
②162.5Vc/m %(2分)
③FeCl3・6H2O烘干时失去了部分结晶水(2分)
本题解析:略
本题难度:一般
5、实验题 课题式学习是研究性学习的一种基本方式,其学习模式为
某化学兴趣小组在学习了电解质的有关知识后,老师提出了一个“电解质水溶液导电能力的强弱的影响因素”的课题。让该小组来完成课题的研究,已知HCl在水中能完全电离。
(1)该小组同学首先用密度为1.049 g・cm-3的乙酸(CH3COOH)和质量分数为36.5%,密度为1.18 g・cm-3的浓盐酸分别配制1 mol/L CH3COOH溶液和1 mol/L HCl溶液各500 mL,则他们应该量取乙酸和浓盐酸的体积分别为_________和__________;
(2)某同学在配制500 mL 1 mol/L的CH3COOH溶液时,向容量瓶中转移溶液时操作如图所示,图中的错误有____________________
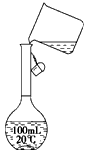
(3)他们首先用如下图所示装置测1 mol/L的CH3COOH溶液和1 mol/L HCl溶液的导电能力,接通电源后发现与HCl溶液相连的灯泡较亮,有同学认为乙酸是弱电解质,你__________(填“同意”或“不同意”)他的观点,通过该现象你得到的结论是___________________________
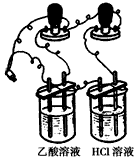
(4)他们又用上述装置测物质的量浓度相同的CuSO4溶液和NaOH溶液的导电能力,接通电源后发现与
CuSO4溶液相连的灯泡较亮,有同学认为NaOH是弱电解质,你 ________(填“同意”或“不同意”)他的观点,通过该现象你得到的结论是____________________________;
(5)通过上述探究实验,你能得到的结论是___________________________________。
参考答案:(1)28.6 mL;42.4 mL
(2)未用玻璃棒引流;未采用500 mL容量瓶
(3)同意;阴、阳离子带电荷数目相同时,单位体积内自由移动离子数目越大,电解质溶液的导电能力越强
(4)不同意;当单位体积内自由移动离子数目相同时,阴、阳离子带电荷数目越多,电解质溶液的导电能力越强
(5)电解质溶液的导电能力是由单位体积内自由移动离子数目和离子所带电荷数目共同决定
本题解析:
本题难度:一般