微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 需要加入还原剂才能实现的转化是( )
A.Na→NaOH
B.HCl→Cl2
C.Fe→Fe3+
D.HNO3→NO
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列变化中,必须加入还原剂才能实现的是( )
A.HN03→NO
B.HCO3-→CO32-
C.S→SO2
D.I-→I2
参考答案:A.HN03→NO,N元素化合价降低,被还原,应加入还原剂才能实现,故A正确;
B.元素的化合价没有发生变化,不是氧化还原反应,故B错误;
C.S元素化合价升高,应加入氧化剂才能实现,故C错误;
D.I元素化合价升高,应加入氧化剂才能实现,故D错误.
故选A.
本题解析:
本题难度:一般
3、选择题 关于氧化还原反应CuO+H2
Cu+H2O,下列说法中正确的是( )
A.CuO是还原剂,H2是氧化剂
B.CuO是氧化剂,H2是还原剂
C.反应中Cu的化合价没有改变
D.反应中H的化合价没有改变
参考答案:在反应CuO+H2?△?.?Cu+H2O中,Cu元素的化合价降低,H元素的化合价升高,在反应中CuO是氧化剂,H2是还原剂.
故选B.
本题解析:
本题难度:一般
4、简答题 .用KMnO4氧化密度为1.19g/cm3,溶质的质量分数为36.5%的?盐酸.反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出上述反应电子得失数目.
(2)求所用盐酸的物质的量浓度.
(3)15.8gKMnO4能使多少克HCl发生上述反应?产生的Cl2在标准状况下的体积为多少?
参考答案:(1)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,Mn元素的化合价+7→+2,和Cl元素的化合价-1→0,反应中氧化剂和还原剂得失电子数目相等,
答:双线桥法标出反应中电子得失数目为
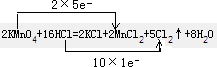
;
(2)c(HCl)=1000ρwM=1000×1.19×36.5%36.5=11.9(mol?L-1),
答:所用盐酸的物质的量浓度为11.9mol?L-1;
(3)设15.8gKMnO4能同xgHCl发生反应,生成标准状况下yLCl2.
? 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
2×158?g?16×36.5?g?5×22.4?L
?15.8?g? x?g? y?L
则?x=16×36.5×15.82×158=29.2?(g),
y=5×22.4L×15.8g2×158g=5.6L.
答:15.8gKMnO4能使29.2克HCl发生上述反应;产生的Cl2在标准状况下的体积为5.6L.
本题解析:
本题难度:一般
5、选择题 制备氰氨基化钙的化学方程式如下:CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑,关于该反应的下列说法,正确的是( )
A.氢元素被氧化,碳元素被还原
B.HCN既是氧化剂又是还原剂
C.CaCN2是还原产物,H2是氧化产物
D.CO为氧化产物,H2为还原产物
参考答案:A
本题解析:A、HCN中氢元素的化合价由+1价变为0价,碳元素的化合价升高,则氢元素被还原,碳元素被氧化,故A正确;
B、HCN中氢元素的化合价由+1价变为0价,碳元素的化合价升高,则HCN自身既是氧化剂又是还原剂,故B错误;
C、因碳元素被氧化,则氧化产物是CaCN2,氢元素被还原,则还原产物H2,故C错误;
D、氢元素被还原,则还原产物H2,但生成物CO中碳元素来自HCN,C的化合价没有发生变化,CO既不是氧化产物也不是还原产物,故D错误;
故选B.
本题难度:简单