微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应中,水作为氧化剂的是( )
A.CO+H2O
CO2+H2
B.3NO2+H2O=2HNO3+NO
C.Cl2+H2O=HCl+HClO
D.2F2+2H2O=4HF+O2
参考答案:A.反应生成H2,H元素化合价降低,水为氧化剂,故A正确;
B.H和O元素化合价没有发生变化,水既不是氧化剂也不是还原剂,故B错误;
C.H和O元素化合价没有发生变化,水既不是氧化剂也不是还原剂,故C错误;
D.O元素被氧化,水为还原剂,故D错误.
故选A.
本题解析:
本题难度:简单
2、简答题 实验室中所用少量氯气是用下列方法制取的,4HCl(浓)+MnO2
Cl2↑+MnCl2+2H2O
试回答下列问题:
(1)该反应是氧化还原反应吗?______,如果是氧化还原反应,请指出______是氧化剂,______是还原剂,______是氧化产物,______是还原产物,根据上述氧化还原反应式判断氧化性:______>______;还原性:______>______.
(2)写出该反应的离子方程式______?
(3)用双线桥法标出该反应电子转移的方向和数目______.
参考答案:(1)元素化合价升高的物质做还原剂被氧化得到氧化产物;元素化合价降低的物质做氧化剂被还原发生还原反应,得到还原产物;氧化还原反应中的氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物;反应前后有元素化合价变化,说明是氧化还原反应;锰元素化合价从+4价变化为+2价,化合价降低做氧化剂被还原为还原产物氯化锰;氯化氢中氯元素化合价升高从-1价变化为0价,化合价升高做还原剂被氧化得到氧化产物Cl2,;氧化还原反应中氧化剂MnO2的氧化性大于氧化产物Cl2,还原剂HCl的还原性大于还原产物MnCl2;
故答案为:是;MnO2;HCl;Cl2;MnCl2;MnO2>Cl2;HCl>MnCl2;
(2)反应中二氧化锰难溶于水,反应的离子方程式为:4H++2Cl-+MnO2=Cl2↑+Mn2++2H2O;
故答案为:4H++2Cl-+MnO2=Cl2↑+Mn2++2H2O;
(3)氧化还原反应中锰元素化合价从+4价降低到+2价;得到电子被还原;HCl中的氯元素化合价从-1价升高到0价失去电子被氧化;电子转移双线桥标注为:
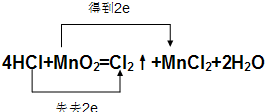
;
故答案为:

本题解析:
本题难度:一般
3、选择题 氮化硅(SiN4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
3SiO2+6C+2N2
Si3N4+6CO.下列叙述正确的是( )
A.在氮化硅的合成反应中,N2是还原剂,SiO2是氧化剂
B.上述反应中每生成1molSi3N4,N2得到12mol是电子
C.若已知上述反应为放热反应,升高温度,其平衡常数增大
D.若使压强增大,上述平衡向正反应方向移动
参考答案:A、在氮化硅的合成反应中,氮元素的化合价由0价降低到-3价,所以氮气是氧化剂,碳元素的化合价由0价升高到+4价,所以碳是还原剂,故A错误;
B、氮元素的化合价总共降低了4×(3-0)=12价,所以每生成1molSi3N4,N2得到12mol电子,故B正确;
C、反应为放热反应,升高温度,平衡逆向进行,其平衡常数减小,故C错误;
D、增大压强,化学平衡向着气体体积减小的方向进行,即向着逆向进行,故D错误.
故选B.
本题解析:
本题难度:简单
4、选择题 下列反应中,同一种物质既做氧化剂又做还原剂的是( )
A.CaCO3=CaO+CO2↑
B.Cl2+H2O=HCl+HClO
C.Cu2(OH)2CO3=2CuO+H2O+CO2↑
D.2H2S+2O2=SO2+2H2O
参考答案:A、CaCO3=CaO+CO2↑中,各元素的化合价都没有发生变化,则不属于氧化还原反应,故A错误;
B、Cl2+H2O=HCl+HClO中,氯气中氯元素的化合价既升高又降低,则氯气既做氧化剂又做还原剂,故B正确;
C、Cu2(OH)2CO3=2CuO+H2O+CO2↑中,各元素的化合价都没有发生变化,则不属于氧化还原反应,故C错误;
D、2H2S+2O2=SO2+2H2O中,S元素的化合价升高,O元素的化合价降低,则O2为氧化剂,H2S为还原剂,故D错误;
故选B.
本题解析:
本题难度:简单
5、选择题 下列关于氧化还原反应说法正确的是( )
A.肯定有一种元素被氧化,另一种元素被还原
B.某元素从化合态变成游离态,该元素一定被还原
C.在反应中不一定所有元素的化合价都发生变化
D.在氧化还原反应中非金属单质一定是氧化剂
参考答案:A.化合价的变化可在同一种元素之间,如Cl2+H2O=HCl+HClO,故A错误;
B.某元素从化合态变成游离态,元素可能被氧化,如Cl-→Cl2,也可能被还原,如Cu2+→Cu,故B错误;
C.氧化还原反应中不一定所有元素的化合价都发生变化,如反应Cl2+H2O=HCl+HClO,只有Cl元素的化合价发生变化,故C正确;
D.在氧化还原反应中非金属单质可做氧化剂,也可做还原剂,如H2,故D错误.
故选C.
本题解析:
本题难度:简单