��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Ե���Ϊ���ȡ�
�ڴ��������£�CO2��H2������ȡ�״����Ҵ����磺2CO2(g)+6H2(g)  ?CH3CH2OH(g)+3H2O(g) ��
?CH3CH2OH(g)+3H2O(g) ��
(��) ��һ��ѹǿ�£�����CO2��Ӧ��ȡ�Ҵ�����÷�Ӧ��ʵ���������±��������������ݻش��������⣺
| 500
| 600
| 700
| 800
|
1.5
| 45
| 33
| 20
| 12
|
2.0
| 60
| 43
| 28
| 15
|
3.0
| 83
| 62
| 37
| 22
|
�¶����ߣ�ƽ�ⳣ��Kֵ��?�����������С�������䡱���������̼��[n(H2)/n(CO2)], ƽ�ⳣ��Kֵ��?�����������С�������䡱����
��600Kʱ��Ӧ�ﵽƽ�⣬Ҫʹ��ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ��
?������ţ���
A����С��Ӧ�����?B��ͨ��CO2?C�������¶ȵ�800K? D��ʹ�ú��ʵĴ���
����ij�¶��£������Ϊl L���ܱ������г���lmol CO2��4mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
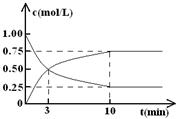
�ӷ�Ӧ��ʼ��ƽ�⣬�״���ƽ����Ӧ����v(CH3OH)=?��
������ƽ��Ũ��Ϊ?mol/L��
�ο��𰸣���С �� ���� ��? AB�� 0.075 mol/(L.min)�� 1.75
���������(��)���ݱ������ݿ�֪�������¶ȵ����ߣ�CO2��ת���ʼ�С����˵�������¶�ƽ�����淴Ӧ�����ƶ���������Ӧ�Ƿ��ȷ�Ӧ���ɴ������¶�ƽ�ⳣ����С��ƽ�ⳣ��ֻ���¶��й�ϵ���ɴ������̼��[n(H2)/n(CO2)], ƽ�ⳣ��Kֵ���䡣���ݷ���ʽ��֪������Ӧ�������С�Ŀ��淴Ӧ������С���������������ѹǿ��ƽ��������Ӧ������У�ͨ��CO2������Ӧ���Ũ�ȣ�ƽ��������Ӧ������У������¶ȣ�ƽ�����淴Ӧ������У��������ܸı�ƽ��״̬�����Դ�ѡAB��
������ͼ���֪����Ӧ���е�10minʱ���ʵ�Ũ�Ȳ��ٷ����仯��˵����Ӧ�ﵽƽ��״̬����ʱ���ɼ״���Ũ����0.75mol/L����ӷ�Ӧ��ʼ��ƽ�⣬�״���ƽ����Ӧ����v(CH3OH)��0.75mol/L��10min��0.075 mol/(L��min)�����ݷ���ʽCO2(g)+3H2(g) ?CH3OH(g)+H2O(g)��֪������������Ũ����0.75mol/L��3��2.25mol/L����ʣ��������Ũ����4mol/L��2.25mol/L��1.75mol/L��
?CH3OH(g)+H2O(g)��֪������������Ũ����0.75mol/L��3��2.25mol/L����ʣ��������Ũ����4mol/L��2.25mol/L��1.75mol/L��
�����������Ǹ߿��еij�����������ͣ������е��Ѷ�����Ŀ��飬�����ۺ���ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������ͷ�ɢ˼ά����������ѧ����ѧ��������
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ����(? )
A�����淴Ӧ������������Ӧ���ʺ��淴Ӧ�������
B����������������ʱ��ʹ�ô���ֻ�ܸı䷴Ӧ���ʣ������ܸı仯ѧƽ��״̬
C����������������ʱ�������¶ȿ���ʹƽ������ȷ�Ӧ�����ƶ�
D����������������ʱ������ѹǿһ�����ƻ����巴Ӧ��ƽ��״̬
�ο��𰸣�B
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0�����������ʵ�Ũ�Ȼ��������ٷ����仯��״̬���ǻ�ѧƽ��״̬��A����ȷ�������¶�ƽ�������ȷ�Ӧ�ķ�����У�C����ȷ��ѡ��D����ȷ���ı�ѹǿƽ�ⲻһ���ƶ���������ȷ�Ĵ�ѡB��
�����Ѷȣ���
3��ѡ���� ��ҵ��������ϩ�������ұ������ⷴӦ��

����˵���������
A���÷�Ӧ������������������ڷ�Ӧ��
B������ѹǿ��Ӧ�����Ӱٷ�������
C�������¶ȿ������ԭ���ұ���ת����
D�����Ϸ��������ϩ�ɼӿ췴Ӧ����
�ο��𰸣�D
���������A����ȷ���������������=��Ӧ���������+���յ�������B����ȷ������ѹǿ���൱��������Ũ�ȣ��������Ŀ����û�иı����Ӱٷ�����C����ȷ������Ӧ�����ȷ�Ӧ�������¶�ƽ�������ƶ����������ԭ���ұ���ת���ʣ�D������ȷ�����Ϸ��������ϩ��������Ũ�Ƚ��ͣ���Ӧ���ʽ��͡�ѡD��
�����Ѷȣ�һ��
4������� �ϳɰ����ع�ҵ�����������漰��������ת����������ͼ��ʾ��
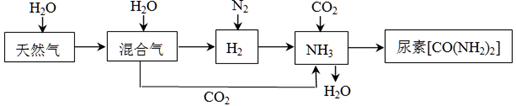
��1����Ȼ������Ҫ�ɷ�ΪCH4���ڸ��¡�������������ˮ������Ӧ����H2��CO�Ļ�ѧ����ʽΪ?��
��2��������һ�����ȼ�ϣ�������ȫȼ��ʱ��Ч�ʽ��ͣ�ͬʱ�����ж����������Ⱦ��
����֪��CH4(g) + 2O2(g)��CO2(g) + 2H2O(l)�� ������H1���D890.3 kJ/mol
2CO (g) + O2(g)��2CO2(g)�������������� ��H2���D566.0 kJ/mol
����鲻��ȫȼ������һ����̼��Һ̬ˮʱ����Ч������ȫȼ��ʱ��_____��������������1λС������
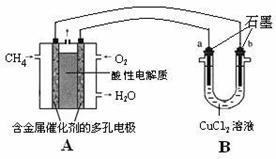
��3������ȼ�ϵ�ؿ����������������ʡ���ͼ�����ü���ȼ�ϵ�ص��50 mL 2 mol��L-1���Ȼ�ͭ��Һ��װ��ʾ��ͼ��
 ��
��
��ش�
�ټ���ȼ�ϵ�ص�������Ӧʽ��____?____��
�ڵ���·����0.1 mol����ͨ��ʱ��________���a����b����������________g��
��4�����䰱ʱ������ʹ��ͭ����Ͻ�����Ĺܵ����š���Ϊ�ڳ�ʪ�Ļ����У�����ͭ����NH3����ʱ�ܱ������е�O2����������[Cu(NH3)4]2+���÷�Ӧ�����ӷ���ʽΪ?��
�ο��𰸣���10�֣�
��1��CH4 + H2O  ?CO + 3H2��2�֣�
?CO + 3H2��2�֣�
��2��0.7��2�֣�
��3���١�O2��4 H+��4e��==2H2O����������2�֣�?�ڡ� b����1�֣�? 3.2��1�֣�
��4��2Cu + 8NH3 + O2 + 2H2O ="==" 2[Cu(NH3)4]2+ + 4OH-��2�֣�
�����������1�����������ṩ�ķ�Ӧ������������������д����ʽ������ʽΪCH4 + H2O  ?CO + 3H2��
?CO + 3H2��
��2��(�ɵ�һ��ʽ�ӳ���2�ڼ�ȥ�ڶ���ʽ��)�ٳ���2�ã�CH4(g) + 3/2O2(g)��CO (g) + 2H2O(l) ��H=- 607.3 kJ/mol��(607.3 kJ/mol)/ (890.3 kJ/mol)=0.7��
��3���ٳ���O2��һ����������ʧȥ���ӣ���Ӧʽ��O2��4H+��4e��==2H2O��
��Cu2++2e-=Cu,0.1mol���ӣ���ͭΪ3.2g��b���������õ��ӣ���b���������ӡ�
��4���������и��ṩ�ķ�Ӧ�����������д�����ӷ���ʽΪ��2Cu + 8NH3 + O2 + 2H2O ="==" 2[Cu(NH3)4]2+ + 4OH-��
���������⿼����ǻ�ѧ���㡢�ϳɰ���ȼ�ϵ�غ͵��ԭ����֪ʶ����Ŀ�Ѷ��У��Ը���֪ʶ��ԭ����������ܽ����⡣
�����Ѷȣ�һ��
5��ѡ���� ��һ���¶��µ��ܱն��������У������������е���һ��ٱ仯ʱ��������ӦA��s��+2B��g��?C��g��+D��g���Ѵ�ƽ�⣨������
A����������ѹǿ
B��B�����ʵ���Ũ��
C��A�����ʵ���Ũ��
D������������ʵ���
�ο��𰸣�A������A�ǹ��壬��Ӧ����ʽ��������Ļ�ѧ������֮����ȣ���������ʵ���ʼ�ղ��䣬�����ݻ��̶������Է�Ӧ��ϵ��ѹǿʼ�ղ��䣬��ѹǿ���䣬�����ж��Ƿ�ﵽƽ��״̬����A����
B��B�����ʵ���Ũ�Ȳ��䣬�������ʵ�Ũ��Ҳ��䣬����ֵ�Ũ�Ȳ��䣬˵�����淴Ӧ������ȣ��ﵽ��ƽ��״̬����B��ȷ��
C������A�ǹ��壬A��Ũ�Ȳ�����Ϊ�ж��Ƿ�ﵽƽ��״̬�����ݣ���C����
D�����ڷ�Ӧ����ʽ��������Ļ�ѧ������֮����ȣ�������ܵ����ʵ���ʼ�ղ��䣬������������ʵ������䣬�����ж��Ƿ�ﵽƽ��״̬����D����
��ѡB��
���������
�����Ѷȣ�һ��