微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列措施符合“绿色化学”思想的是( )
A.直接排放含磷生活污水
B.大量使用氟里昂作为冰箱制冷剂
C.使用可降解塑料代替不可降解塑料
D.使用化学性质稳定、不易分解的有机氯农药
参考答案:C
本题解析:
本题难度:一般
2、选择题 化学工业是国民经济的支柱产业.下列生产过程中不涉及化学变化的是
A.氮肥厂用氢气和氮气合成氨
B.钢铁厂用热还原法冶炼铁
C.硫酸厂用接触法生产硫酸
D.炼油厂用分馏法生产汽油
参考答案:D
本题解析:A、氢气与氮气合成氨是化学变化,错误;B、热还原法炼铁是化学变化,错误;C、接触法制硫酸涉及了一系列的化学反应,是化学变化,错误;D、分馏法生产汽油是利用了石油中各组分的沸点的不同,把物质分离,是物理变化,正确,答案选D。
本题难度:一般
3、选择题 工业上用于制造水泥的主要设备是
A.炼铁高炉
B.制硫酸的沸腾炉
C.水泥回转窑
D.氨的合成塔
参考答案:C
本题解析:水泥的原料为石英、石灰石和纯碱。在水泥回转窑中反应。
本题难度:简单
4、填空题

(1) 已知:450℃时NH3的浓度大于550℃时,则正反应是______? __热反应;
(2) 反应进程中:0~2s内N2的物质的量由2mol变为1mol,则υ(H2)=___________;
(3) 能说明该反应已经达到平衡状态的是_________?__;
A.c(N2)=c(H2)="c" (NH3)? B.容器内压强保持不变?
C.υ(N2)=3υ(H2)? D.容器内的密度保持不变
(4) 可使该反应的反应速率增大,且平衡向正反应方向移动的措施是__________。
A.及时分离出NH3气体? B.适当升高温度
C. 增大压强? D.选择高效的催化剂
参考答案:(1)放热(1分) (2)0.75mol/(L・s) (2分) (3)B (1分) (4)C(1分)
本题解析:本题考查化学反应速率及化学平衡有关知识,关键在于明确化学反应速率的影响因素及化学平衡的判断。(1)450℃时NH3的浓度大于550℃时,说明温度升高,平衡向逆反应方向移动,则正反应是放热反应;(2)υ(H2)=3υ(N2)=3(2-1)/(2×2)= 0.75mol/(L・s);(3) A中浓度相等,但不一定达到平衡,只有浓度不在改变时,表示达到了平衡,该反应是体积不相等的反应,体积固定,故压强不变,表示该反应已达平衡;C项中未指明是正反应速率还是逆反应速率,故不能表示该反应已达平衡;体积固定,质量不变,密度不变,故不能表示该反应已达平衡;故选B。
(4)及时分离出NH3气体,减少生成物,减小逆反应速率,A不合题意;适当升高温度,平衡向逆反应方向移动,B不合题意;增大压强,反应速率增大,平衡向正反应方向移动,C合题意,正确;催化剂只改变反应速率,不影响平衡移动,D不合题意,故选C。
本题难度:一般
5、选择题 在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器接触室(见图)。按此密闭体系中气体的流向,则在A处流出的气体为(? )
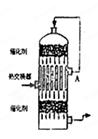
A.SO2
B.SO3、O2
C.SO2、SO3
D.SO2、O2
参考答案:D
本题解析:在接触室里的热交换器是利用前面发生产生的热量给即将发生反应的SO2、O2的混合气体先预热,然后再在催化剂的表面接触氧化,发生反应。因此正确的选项为D。
本题难度:简单