| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《热化学方程式》在线测试(2017年最新版)(二)
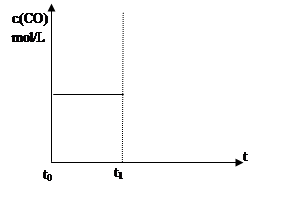 ① 缩小容器体积(用实线表示)。 ② 降低温度(用虚线表示)。 (5)某温度下,将6.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应, C (s) + H2O(g)  CO (g) +H2 (g),达到平衡时测得lgK= -1.0,求此温度下H2O(g)的 CO (g) +H2 (g),达到平衡时测得lgK= -1.0,求此温度下H2O(g)的转化率(计算结果保留3位有效数字,要求写出计算过程)。 (6)己知:① C (s) + H2O(l)  CO (g) +H2 (g) △H1 CO (g) +H2 (g) △H1② 2CO(g) + O2(g) = 2CO2 (g) △H2 ③ H2O (l)= H2 (g) +1/2 O2 (g) △H3 则2C (s) + O2 (g) = 2CO2 (g)的△H= _________ ____。 参考答案:(16分) 本题解析:(1)该反应是吸热反应,温度升高,平衡正向移动,生成物浓度增大,反应物浓度减小,所以化学平衡常数增大; 本题难度:困难 2、填空题 黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分燃烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol・L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL。 参考答案:(1)90.00% 本题解析: 本题难度:一般 3、填空题 “温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。 参考答案:(1)abc(2分)(2)C2H4(g)+H2O(l)=C2H5OH(l) △H="-44.2" kJ/mol(2分) 本题解析:(1)a.采用节能技术能减少化石燃料的使用,减少化石燃料的使用就减少了二氧化碳的排放,正确;b.化石燃料燃烧产物是二氧化碳,减少化石燃料的使用就减少了二氧化碳的排放,正确;c.利用太阳能、风能能减少化石燃料的使用,化石燃料燃烧产物是二氧化碳,减少化石燃料的使用就减少了二氧化碳的排放,正确;故选abc。 本题难度:困难 4、填空题 分碳和氮的许多化合物在工农业生产和生活中有重要的作用。
①T1℃时,该反应的平衡常数K= ; ②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母编号)。 a.加入一定量的活性炭 b.通人一定量的NO c.适当缩小容器的体积 d.加入合适的催化剂 ③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则Q 0(填“>”或“<”)。 参考答案:(1)4NH3+5O2 本题解析:(2)由盖斯定律方程式①+②-③得热化学方程式2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l);△H=-87.0kJ/mol;(3)由原电池原理,结合电解质溶液的碱性确定负极反应式为2NH3+6OH- -6e-=N2+6H2O ;每消耗3.4g NH3转移的电子数为0.6NA;(4)由平衡常数的表达式确定T1℃时,该反应的平衡常数K=c(N2)×c(CO2)/c2(NO)=0.56;30min后气体的浓度均增大,所以可能是通入的NO或缩小了容器的体积;升高温度时三种气体的浓度比值与T1℃平衡状态下增大,所以确定平衡逆向移动,Q <0. 本题难度:困难 5、填空题 (18分)在容积不同的多个密闭容器内,分别充入同量的N2和H2,在不同温度下,同时发生反应N2+3H2 |
参考答案:(1) AB (2) (3)BCFG
(4) AC段,反应开始时温度升高,反应速率增大,反应向正反应方向进行,生成NH3;CE段,已经达到平衡,升高温度使平衡向逆反应方向移动NH3%变小
本题解析:(1)N2、H2合成NH3反应是放热的,升高温度平衡逆向移动,NH3的百分含量降低,所以升高温度NH3的百分含量升高,说明反应未答平衡。因此AB两点是未达到平衡的点。
(2) N2 + 3H2 = 2NH3
起始 1mol 3mol 0
反应 xmol 3xmol 2xmol
T3时 (1-x)mol (3-3x)mol 2xmol
根据T3时体系压强为原来的7/8,则有 ,所以x=0.25mol。
,所以x=0.25mol。
所以生成0.5molNH3放热23.1 kJ,则热化学方程式为N2(g)+3H2(g)=2NH3(g) ΔH=-92.4kJ/mol。
(3)根据N2(g)+3H2(g)=2NH3(g) ΔH=-92.4kJ/mol可知,增大压强,降低温度,吸收氨气,通入氮气,都可以增加氨气的产率。
(4)从AC段可以看出平衡正向移动,说明反应没有达到平衡,所以升高温度扔正向移动,CE段可以看出平衡逆向移动,说明反应达到平衡,升高温度平衡逆向移动。
考点:化学平衡与化学反应热
点评:本题综合性强,主要考查学生分析问题的能力,是高考的热点习题。
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《无机非金属.. | |