微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):Cu+2H2SO4(浓)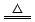 CuSO4+A↑+2H2O
CuSO4+A↑+2H2O
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。则A应该属于______________(用字母代号填写)
a.酸? b.碱? c.盐? d.酸性氧化物? e.碱性氧化物
A物质可以使酸性KMnO4溶液褪色,此反应中__________(填写化学式,下同) 失去电子,氧化剂是____________。
(2)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的A气体在标准状况下体积为_________L (假设气体全部逸出)。
(3)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:___________________ ??
计算反应后所得沉淀的质量为__________________g(保留到0.1g)。
参考答案:(12分) (1)d? SO2?KMnO4 (各1分)? (2)2.24?(2分)?
(3)Ba2++SO42-+2OH-+2H+=2H2O+BaSO4↓? (2分)
Ba2++SO42-+2OH-+Cu2+=Cu(OH)2↓+BaSO4↓(2分)? 4O5.9(3分)
本题解析:(1)A物质可以导致酸雨的形成。则A是二氧化硫,应该属于酸性氧化物;
A物质可以使酸性KMnO4溶液褪色,此反应中SO2?失去电子,氧化剂是KMnO4。
(2)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,由定量关系得:Cu+2H2SO4(浓) CuSO4+SO2 ↑+2H2O,电子转移2mol,就会生成1molSO2 气体,所以生成的SO2 气体在标准状况下体积为2.24L (假设气体全部逸出)。
CuSO4+SO2 ↑+2H2O,电子转移2mol,就会生成1molSO2 气体,所以生成的SO2 气体在标准状况下体积为2.24L (假设气体全部逸出)。
(3)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。此过程发生的反应的离子方程式:Ba2++SO42-+2OH-+2H+=2H2O+BaSO4↓Ba2++SO42-+2OH-+Cu2+=Cu(OH)2↓+BaSO4↓反应后所得沉淀包括硫酸钡和氢氧化钡,由守恒关系可知其质量之和为4O5.9g。
点评:此题要熟悉基本的计算关系式,同时要注意离子方程式书写的方法。
本题难度:一般
2、填空题 (7分)6.02×1024个Na+约含 mol Na+,其质量为 g;4.5molCH4约含有 个CH4,其质量为 g;3.01×1023个SO42-约含 molSO42-,其质量为 g;49gH2SO4约含有 个H,共含有 mol原子。
参考答案:10、230;2.709×1024,72;0.5、48;6.02×1023、3.5 【说明】此题与16题相似
本题解析:略
本题难度:简单
3、填空题 (12分)氯气是一种重要的工业原料。
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4  2CaSO4+2Cl2↑+2H2O
2CaSO4+2Cl2↑+2H2O
他们利用该反应设计如下制取氯气并验证其性质的实验。

(1)回答下列问题:(1)该实验中A部分的装置是 (填标号) 。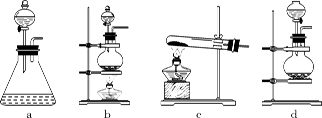
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤): 。
(3)写出D装置中发生反应的离子方程式 (4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol・L?1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2 === Na2S4O6+2NaI,共用去Na2S2O3溶液20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为 。
参考答案:Ⅰ.MnO2 + 4HCl(浓)  MnCl2 + Cl2↑+ 2H2O (2分)
MnCl2 + Cl2↑+ 2H2O (2分)
Ⅱ.(1)b (2分)
(2) 取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化 (2分)
(3) Cl2+H2O ="==" H++Cl?+HClO
H++HCO3? ="==" CO2↑+H2O (合理答案均可,共2分)
(4) 应将尾气通入NaOH溶液中 (2分)
(5) 35.75% (2分)
本题解析:Ⅰ实验室可用二氧化锰和浓盐酸反应制取氯气的化学方程式:MnO2 +4HCl(浓) MnCl2 +Cl2↑+2H2O。
MnCl2 +Cl2↑+2H2O。
Ⅱ⑴A部分是氯气的发生装置,而此装置为固液加热型装置,因此选b。
⑵证明洗气瓶C中的Na2SO3已被氧化,实际上是证明溶液中存在SO42-。
⑶装置D中为碳酸氢钠与氯气的反应,,此时应考虑氯气溶液水发生的反应。故答案为:
Cl2+H2O=H++Cl?+HClO、H++HCO3?=CO2↑+H2O。
⑷整个反应过程中由于氯气具有毒性,因此,装置的末尾应加上一个尾气处理装置。可用碱性溶液吸收。
⑸由此过程中涉及的反应式可得出如下关系式: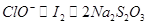 ,所以得:
,所以得: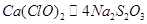
143 4mol
x 0.002mol 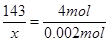 解得
解得 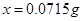
故该漂白粉中Ca(ClO)2的质量分数为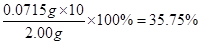
考点:氯气及其化合物的性质与相关计算
点评:本题是一道结合实验与计算的综合题,属于中等难度题型,也是高考中的常考题型。对于此类题型的解答,熟练掌握物质的相关性质,是解题关键。对于计算,则需将多步反应联系起来,找出之间的对应关系,形成关系式形式,可简化计算,减少计算量。
本题难度:困难
4、填空题 (12分)天然碱是一种重要的矿物质,盛产于我国的青海湖地区。某天然碱样品的成分可以看成是碳酸钠、碳酸氢钠和水按物质的量之比1:1:2形成的结晶水合物。请回答下列问题:
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为?。
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=?,盐酸中溶质的质量分数ω(HCl)=?%。
(3)用一个化学方程式表示该天然碱与盐酸的反应:
?。
参考答案:(1)53:42:18(3分)?(2)0.4,20(各3分)
(3)Na2CO3・NaHCO3・2H2O+3HCl=3NaCl+4H2O+2CO2↑(3分)
本题解析:略
本题难度:简单
5、选择题 相同质量的氧气和臭氧中,其氧原子个数( )
A.大于
B.小于
C.等于
D.不能确定
参考答案:C
本题解析:
本题难度:简单