��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣�����������һ��Ũ�ȵ������з�Ӧ�Ļ�ѧ����ʽ���£�
a Fe+b NO3-+c H+="=d" Fe2++f Fe3++g NO��+h N2O��+k H2O(��ѧ��������Ϊ������)
�����������յ�֪ʶ�о������й��ɡ�
(1) c��g��h�Ĺ�ϵʽ��____________________��
(2) b��c��d��f�Ĺ�ϵʽ��_________________________��
(3) d��f��g��h�Ĺ�ϵʽ��_________________��
(4)��a =12����������ǡ����ȫ��Ӧ����b��ȡֵ��Χ��________________��c��ȡֵ��Χ��______________________��
�ο��𰸣�(1) c =" 4g+10h?" (2) c��b="2d" +3f? (3) 2d +3f ="3g+8h?" (4) 6<b<12? 30<c<48
�����������1��Ԫ���غ㣺c="2k?" 3b="g+h+k?" ����6b="2g+2h+c" �֣�b="g+2h?" �ʣ�c = 4g+10h
��2������غ㣺c="2d+3f+b?" ����c��b=2d+3f
��3������ת���غ㣻3g+8h="2d+3f"
��4����Fe��Fe2+��NO3-��N2Oʱ��b����Сֵ��b=12��2/4 = 6
��Fe��Fe3+��NO3-��NOʱ��b�����ֵ��b=12��3/3 =" 12?" ���У�6<b<12
��6<b<12����c=2d+3f+b��c=2d+b��c=3f+b���ã�30<c<48
�����Ѷȣ�һ��
2������� �����漰4����ɲ�ͬ���������Ƕ���ƽ�������νṹ��
�� PtCl2��2KCl��ˮ��Һ��������ѣ�Et2S����Ӧ��Ħ����1�U2���õ����ֽṹ��ͬ�Ļ�ɫ�����÷�Ӧ�Ļ�ѧ����ʽ������������ṹ�ǣ�
�� PtCl2��2KCl��ˮ��Һ������Et2S��Ӧ��õ������Ϊ����ɫ���壬����AgNO3��Ӧ��Ħ����1�U2���õ�������ɲ�ͬ������д������������Ӧ�Ļ�ѧ����ʽ��
�ο��𰸣��� PtCl2��2KCl��2Et2S��[Pt(Et2S)2 Cl2]��2KCl��2�֣�

˳ʽ?��ʽ?����0.5�֣�
�� 2PtCl2��2KCl��4Et2S��[Pt(Et2S)4][PtCl4]��4KCl��3�֣�
[Pt(Et2S)4][PtCl4]��2AgNO3��Ag2[PtCl4]��[Pt(Et2S)4](NO3)2��2�֣�
�����������PtCl2��2KCl��ˮ��Һ����K2PtCl4����ʽ���ڣ��������⣬��Et2S���������ȡ����Ӧ������˳ʽ�ͷ�ʽ��Pt(Et2S)2 Cl2��
��AgNO3��2��1�����ʵ���֮���뵭��ɫ���巴Ӧ�������ֲ�ͬ����������һ��������ΪAg+��������Ϊ�����۵�PtCl42-����Ag2[PtCl4]������һ��������Ŀ����������������ֻ��Ϊ[Pt(Et2S)4](NO3)2���������������ǿ��Կ�����K2PtCl4��Et2S��1��4�ı������������ȡ����Ӧ�����ɵġ���˵���ɫ����Ϊ[Pt(Et2S)4][PtCl4]��
�����Ѷȣ�һ��
3��ʵ���� (��12��)������������Ҫ������������ԭ��������ˮ��Һ�ֳ�Ϊ˫��ˮ��������������ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹��������Ũ�ȣ� ����д���пհף�
��1����10.00 mL����������Һ��250mL ___________(����������)�У���ˮϡ�����̶ȣ�ҡ�ȡ���ȡϡ�ͺ�Ĺ���������Һ25.00mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ�������������
��2���ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽ���£��뽫������ʵĻ�ѧ�������ͻ�ѧʽ�ֱ��������к��ߺ������ڡ�?
?MnO4- +?H2O2?+?H+?="=" ?Mn2+?+?O2?+?(? )
��3����ȡ10mL����������Һ������_________________(���ʽ����ʽ��)�ζ��ܡ����ü�ʽ�ζ���ʢװKMnO4��Һ��ԭ����?���ζ������յ��������__________? _____________��
��4���ظ��ζ����Σ�ƽ������c mol/L KMnO4����ҺV mL����ԭ����������Һ�й��������Ũ��Ϊ_________________________________��
��5����ʢװ������ر���Һ�ĵζ���������ˮϴ��û���ñ�Һ��ϴ����ⶨ���_________(�ƫ�ߡ���ƫ�͡����䡱)��
�ο��𰸣���1������ƿ(1��)��2��2MnO4- + 5H2O2 + 6H+ = 2Mn2+ + 5O2��+8H2O(����ʽ1�֣���ƽ2�֣���3��)
��3����ʽ (1��)?������ؾ���ǿ�����ԣ���ʹ��Ƥ���ϻ�? (2��)��Һ����ɫ��Ϊ�Ϻ�ɫ���Ұ�����ڲ���ɫ(2��)?��4�� 2.5cv(2��)?��5��ƫ��(2��)
�����������1��ȷ����һ�����һ�����ʵ���Ũ����Һ������ƿ���ʴ�Ϊ������ƿ����2������ʽ�У����������ǿ�����ԣ��ܽ�˫��ˮ����Ϊ��������ȷ��ȱ����O2����Ԫ�ػ��ϼ۽�����5�ۣ�����1mol����ʱ����Ԫ�ػ��ϼ�����2�ۣ����ݵ���ת���غ㣬��ƽ��ѧ����ʽ�������ǰ���ϵ��Ϊ2��˫��ˮǰ���ϵ��Ϊ5������ԭ���غ�����ƽ��������ǰ���ϵ����2MnO4- + 5H2O2 + 6H+ = 2Mn2+ + 5O2��+8H2O����3�����ڸ�����ر���Һ����ǿ�����ԣ�����ֻ��ʹ����ʽ�ζ��ܣ��ζ������յ�������ǣ�����һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ���ʴ�Ϊ����ʽ������һ�θ��������Һ����Һ��dz��ɫ����30���ڲ���ɫ����4�����ݻ�ѧ����ʽ���Եõ���ϵʽ��2MnO4-��5H2O2������c mol/L KMnO4����ҺV mL����cV��10-3mol�ĸ������ʱ������˫��ˮ�����ʵ�����2.5cV��10-3mol����5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����һ������Һռ�������ݵ��������û�е�����ƿ����ⶨ���ƫ�ߡ�
�����Ѷȣ�һ��
4��ʵ���� ijʵ��С��ͬѧΪ��̽��SO2�����ʣ�����������ʵ�飨ʵ��ǰ��װ���ڿ������ž�����
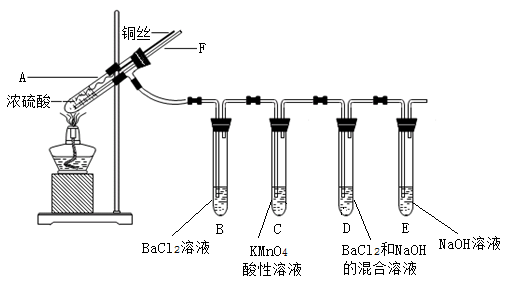
��֪������ķе���338�棬�ƾ��ƿɼ�����400�����ϡ�
��Ҫʵ�鲽�裺
�ټ����Թ�Aֱ��B��D�о����ִ�����ɫ������Ϩ��ƾ��ƣ�
�ڽ�Cu˿�����뿪Һ�棻
�۴ӵ���F����װ����ͨ�����һ��ʱ�䡣
��1���Թ�A�з�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ ��
��2���Թ�B�г��ְ�ɫ������ԭ���� ��
��3���Թ�C����Һ��ɫ��˵��SO2���� ���Ư���ԡ��������ԡ���ԭ�ԡ������뽫�÷�Ӧ�����ӷ���ʽ����������
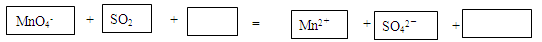
��4���Թ�D�з�����Ӧ�����ӷ���ʽΪ ��
��5������������ȷ���� ��
a�������ƶ�ͭ˿�ɿ�������SO2����
b��Ϊȷ����CuSO4���ɣ������Թ�A�м�ˮ���۲���ɫ
c������ۿ�ʹװ���в���������ȫ�����գ�������Ⱦ����
d��Ϩ��ƾ��ƺ� B�е�Һ�岻�ᵹ������Ϊ�����ɾ�����F�����Թ�A��ʹѹǿƽ��
�ο��𰸣���1��Cu+2H2SO4(Ũ)  CuSO4+SO2��+2H2O ��2�����������������Ȼ�����Ӧ���������ᱵ
CuSO4+SO2��+2H2O ��2�����������������Ȼ�����Ӧ���������ᱵ
��3����ԭ�ԣ� 2MnO4- + 5SO2 +2H2O = 2Mn2++ 5SO42- + 4H+��4��SO2+ 2OH��+Ba2+=BaSO3��+ H2O ��5��acd
�����������1����֤SO2�����ʣ������Ʊ�SO2������ʵ�飺A����ͭ˿��Ũ��������Ʊ�SO2��Cu+2H2SO4(Ũ)  CuSO4+SO2��+2H2O����2������ķе�338�棬�ƾ��ƿɼ�����400�����ϣ��������ᱻ������������BaCl2��Ӧ�������ᱵ������BaCl2��H2SO4=BaSO4����2HCl��(3)����KMnO4����ǿ�����ԣ�SO2�Ⱦ���������Ҳ���л�ԭ�ԣ�����ǿ�����Ե�����ʱ�����ֻ�ԭ�ԣ����SO2�ڴ˱��ֻ�ԭ�ԣ�MnO4����Mn2�������ϼ��ɣ�7�۱���ˣ�2�ۡ�5��SO2��SO42�����ϼ��ɣ�4�۱���ˣ�6�ۡ�2����С��������10��MnO4����Mn2��ϵ����2��SO2��SO42����ϵ����5�����ݷ�Ӧǰ�������������ȣ���H2O�μӣ���H�����ɣ����ݷ�Ӧǰ��ԭ�Ӹ����غ㣺2MnO4- + 5SO2 +2H2O = 2Mn2++ 5SO42- + 4H+��(5)SO2�����������SO2��2NaOH=Na2SO3��H2O��BaCl2��Na2SO3=BaSO3����2NaCl����ʽ�ϲ��õ����ӷ�Ӧ����ʽ��SO2+ 2OH��+Ba2+=BaSO3��+ H2O��(5)a�������ƶ�ͭ˿�ɿ��Ʒ�Ӧ�Ľ��У���Լԭ�ϣ���ȷ��b��A�з�Ӧ���ɵ�CuSO4����Һ����ˮϡ�ͣ���dz������˵������CuSO4������c��SO2�ж��Ի�������Ⱦ�������ȥ����ȷ��d��Ϩ��ƾ��ƺ�B�в�������������Ϊ����ѹǿ��ȣ���ȷ�����acd��ȷ��
CuSO4+SO2��+2H2O����2������ķе�338�棬�ƾ��ƿɼ�����400�����ϣ��������ᱻ������������BaCl2��Ӧ�������ᱵ������BaCl2��H2SO4=BaSO4����2HCl��(3)����KMnO4����ǿ�����ԣ�SO2�Ⱦ���������Ҳ���л�ԭ�ԣ�����ǿ�����Ե�����ʱ�����ֻ�ԭ�ԣ����SO2�ڴ˱��ֻ�ԭ�ԣ�MnO4����Mn2�������ϼ��ɣ�7�۱���ˣ�2�ۡ�5��SO2��SO42�����ϼ��ɣ�4�۱���ˣ�6�ۡ�2����С��������10��MnO4����Mn2��ϵ����2��SO2��SO42����ϵ����5�����ݷ�Ӧǰ�������������ȣ���H2O�μӣ���H�����ɣ����ݷ�Ӧǰ��ԭ�Ӹ����غ㣺2MnO4- + 5SO2 +2H2O = 2Mn2++ 5SO42- + 4H+��(5)SO2�����������SO2��2NaOH=Na2SO3��H2O��BaCl2��Na2SO3=BaSO3����2NaCl����ʽ�ϲ��õ����ӷ�Ӧ����ʽ��SO2+ 2OH��+Ba2+=BaSO3��+ H2O��(5)a�������ƶ�ͭ˿�ɿ��Ʒ�Ӧ�Ľ��У���Լԭ�ϣ���ȷ��b��A�з�Ӧ���ɵ�CuSO4����Һ����ˮϡ�ͣ���dz������˵������CuSO4������c��SO2�ж��Ի�������Ⱦ�������ȥ����ȷ��d��Ϩ��ƾ��ƺ�B�в�������������Ϊ����ѹǿ��ȣ���ȷ�����acd��ȷ��
���㣺�������������Ʊ������ʡ�������ԭ��Ӧ����ƽ��
�����Ѷȣ�����
5��ѡ���� ��2KMnO4��16?HCl====2KCl+2MnCl2��5Cl2����8H2O�ķ�Ӧ�У��������ͻ�ԭ�������ʵ���֮��Ϊ
A��1��8
B��8��1
C��1��5
D��5��1
�ο��𰸣�C
�������������������̵Ļ��ϼ۴ӣ�7�۽��͵���2�ۣ��õ�5�����ӡ��Ȼ�������Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ�ʧȥ1�����ӡ���˸��ݵ��ӵĵ�ʧ�غ��֪���������ͻ�ԭ�������ʵ���֮��Ϊ1��5?����ѡC��
�����Ѷȣ�һ��