��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����ͼ��ʾװ�ý���ʵ�飬��A��μ���B�У�
��1����AΪŨ���ᣬBΪ�������ڽ���Ԫ�ص�Ƭ״���ʣ����ڳ���������ˮ��Ӧ��CΪƷ����Һ��ʵ���й۲쵽��Һ��ɫ����B��______��д��ѧʽ����B��ŨH2SO4��Ӧ�Ļ�ѧ����ʽΪ______����Ӧ�����ձ��м����ˮ���ֿɹ۲쵽�Թ�C�е�����Ϊ______��
��2����BΪNa2CO3��CΪC6H5ONa��Һ��ʵ���й۲쵽С�Թ�����Һ����ǣ�����AӦ���е�������______��Ȼ�����ձ��м����ˮ���ɹ۲쵽�Թ�C�е�������______��
��3����B����ʯ�ң�ʵ���й۲쵽C��Һ���γɳ�����Ȼ������ܽ⣬����Һǡ�ó���ʱ���ر�E��Ȼ�����ձ��м�����ˮ������Ƭ�̣��۲쵽�Թܱڳ��ֹ�������������A��______��д���ƣ���C��______��д��ѧʽ���������ǵĻ��Һ���÷�Ӧ�����ӷ���ʽΪ______������D�ڴ�ʵ���е�������______��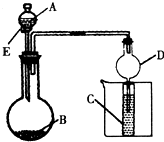
�ο��𰸣���1���������֪��BΪ�������ڽ���Ԫ�ص�Ƭ״���ʣ����ڳ���������ˮ��Ӧ��B����Ϊ������þ����Ũ���᳣���»�ʹ���ۻ�������Bֻ��Ϊþ����Ũ���ᷢ��������ԭ��Ӧ����Ӧ�ķ���ʽΪMg+2H2SO4��Ũ��=MgSO4+SO2��+2H2O��SO2����Ư���ԣ���ʹƷ����ɫ�������ȶ����������ָܻ���ԭ������ɫ��
�ʴ�Ϊ��Mg��Mg+2H2SO4��Ũ��=MgSO4+SO2��+2H2O��C����Һ��죻
��2���۲쵽С�Թ�����Һ����ǣ�˵�����ɶ�����̼����A������Ӧ��̼�������ǿ�����ɱ�����������ˮ��������Һ����壬
�ʴ�Ϊ�����Ա�̼�������ǿ����Һ�ɻ��DZ���壻
��3���Թܱڳ��ֹ�����������˵�����ɰ���������Ũ��ˮ����ε�Ũ��Һ����ʯ�ҷ�Ӧ��ȡ��C��ӦΪ��������������Һ�ķ�Ӧ����C��ӦΪAgNO3�������ǵĻ��Һ������ʱ������CH2OH��CHOH��4CHO+2[Ag��NH3��2]++2OH-ˮ��
���������
�����Ѷȣ�һ��
2������� ��16�֣���ͨ��״���£�AΪ��̬���ʡ�������ͼת����ϵ���ش�
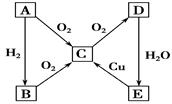
(1)д��A��C��E�Ļ�ѧʽ��A__________��C__________��E__________��
(2)д�����з�Ӧ�Ļ�ѧ����ʽ��
��E�D��C ��________________________________________________________��
��C�D��D ��________________________________________________________��
(3)B��E��Ũ��Һ______������Ӧ(��ܡ����ܡ�)�����ܷ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ____?____����Ӧ����_________________________��
�ο��𰸣���1��S? SO2? H2SO4
��2��Cu + 2H2SO4 (Ũ) = CuSO4?+ SO2?+ 2H2O? 2SO2 + O2  2SO3
2SO3
(3)��? H2S + H2SO4?=" S��" + SO2��?+ 2H2O?��������ɫ��������ɫ�д̼�����ζ������
������������嵥��A�ܺ�������Ӧ��Ҳ�ܺ�������Ӧ��˵���Ƿǽ������ʡ�����������������ü�����������Ӧ���жϣ�A��S����������Ӧ�����Ȼ��⣬�Ȼ���ȼ�ռ�����SO2�����������Ӧ��SO2��SO2��������Ӧ������������������������ˮ�������ᡣŨ�����ڼ��ȵ������º�ͭ����������ԭ��Ӧ����������ͭ��SO2��ˮ����������Ԫ�صĻ��ϼ��ǡ�2�ۣ�������ͼۣ����л�ԭ�ԣ���Ũ������������ԣ����߷���������ԭ��Ӧ���������ʺ�SO2�Լ�ˮ��
�����Ѷȣ�һ��
3������� ͼ��ʾ��Ԫ�����ڱ���1��20���Ҳ�ͬ����Ԫ����ɵĵ��ʼ�������֮��ת����ϵ�������е�ˮ����ȥ��������AΪ���ʣ���ʵ�����У����ù���B����C������ȡ����F��F��G�����Ԫ����ͬ��G��I����������������ͬ����ش�
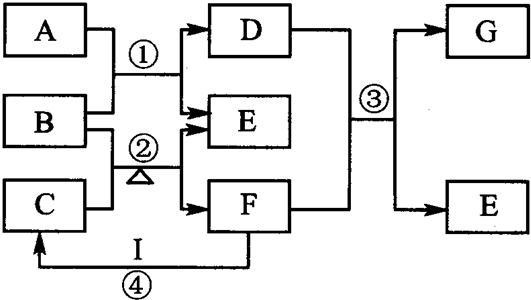
��1��д��B��G�Ļ�ѧʽB______��G______��
��2��д��C�ĵ���ʽ______����Ӧ�ܵ�ʵ������Ϊ______��д��F��һ�־�����;______��
��3�������Ư�����õ�D��Һ����I��ϡ��Һ��д����Ӧ�����ӷ���ʽ��______����D����Һ����I��Ũ��Һ��A���ɣ��䷴Ӧ�����ӷ���ʽΪ��______��
��4��д����Ӧ�۵Ļ�ѧ����ʽ______��
�ο��𰸣���1����ʵ�����У����ù���B����C������ȡ����F��ӦΪNH4Cl��Ca��OH��2��Ӧ���ɰ����ķ�Ӧ����FΪNH3��EΪCaCl2������F����I����C����CΪNH4Cl��BΪCa��OH��2��IΪHCl������F��G�����Ԫ����ͬ��G��I��ΪHCl������18�����ӣ�����������������ͬ���жϣ�GΪN2H4�������У�3�������Ư�����õ�D��Һ����֪DΪCa��ClO��2����AΪCl2��
�ʴ�Ϊ��Ca��OH��2��N2H4��
��2��CΪNH4Cl��Ϊ���ӻ���������ʽΪ

����Ӧ��Ϊ��NH3+HCl�TNH4Cl���а������ɵ�����NH4Cl�������Ƶ��ʣ��ʴ�Ϊ��

�����̣��Ƶ��ʣ��������ᡢ�ƴ������Σ���ԭ�ϻ����������
��3��HClOΪ������ʣ���Ca��ClO��2��Һ�м���������HClO���ɣ�ClO-�����������¾���ǿ�����ԣ���Cl-��Ӧ����Cl2���ʴ�Ϊ��ClO-+H+=HClO��ClO-+Cl-+2H+=Cl2��+H2O��
��4�����ݷ�Ӧ����������������غ㶨�ɿ�д����Ӧ�۵Ļ�ѧ����ʽΪ2NH3+Ca��ClO��2=N2H4+CaCl2+H2O��
�ʴ�Ϊ��2NH3+Ca��ClO��2=N2H4+CaCl2+H2O��
���������
�����Ѷȣ�һ��
4������� ��11�֣���A��B��C��D��EΪ��ѧ��ѧ�����ĵ��ʻ���ת����ϵ��ͼ��ʾ��
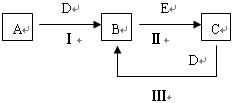
���� A����ʹʪ��ĺ�ɫ��ֽ���������壻C��D��Ϊ��������Ҫ�ɷ֣�E��һ����ɫ��ζ���ж����塣��д��E�Ļ�ѧʽ?��
A����ʹʪ��ĺ�ɫ��ֽ���������壻C��D��Ϊ��������Ҫ�ɷ֣�E��һ����ɫ��ζ���ж����塣��д��E�Ļ�ѧʽ?��
��д����Ӧ��Ļ�ѧ����ʽ?��
����A�ǵ���ɫ�����������D����ɫ���壻C�к��е����������Ӿ�Ϊ10 ��������
��������
��д��A�ĵ���ʽ?
��д����Ӧ��Ļ�ѧ����ʽ?
����A�ǵؿ��к������Ľ�����B�ڻ���������ʱ����ʻ�ɫ��B��C�о�����AԪ�أ���B��C����Һ�л��ʱ�����ɰ�ɫ����
��д��B�Ļ�ѧʽ?��д����Ӧ������ӷ���ʽ?
����A�Ǻ�ɫ��ĩ������ ��B�ǻ���ɫ���壬C��Һ�ʼ��ԣ���Ư���ԡ�
��B�ǻ���ɫ���壬C��Һ�ʼ��ԣ���Ư���ԡ�
д����Ӧ������ӷ���ʽ?��
�ο��𰸣���11�֣����Ţ�CO ��1�֣�? �� 4NH3+5O2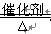 4NO+6H2O?��2�֣�?
4NO+6H2O?��2�֣�?
�Ƣ�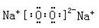 ��1�֣�?��Ca(OH)2+Na2CO3=CaCO3��+2NaOH ��2�֣�
��1�֣�?��Ca(OH)2+Na2CO3=CaCO3��+2NaOH ��2�֣�
�� ��NaAlO2��1�֣� ��Al3����4OH��=AlO2��+2H2O ��2�֣��� H��+Cl��+ClO��=Cl2��+H2O��2�֣�
�����������
�����Ѷȣ�һ��
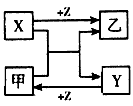
5��ѡ���� X��Y��Z�����ֳ���Ԫ�صĵ��ʣ��ס��������ֳ����Ļ������Щ���ʺͻ�����֮�������ͼ��ʾ��ת����ϵ������˵����ȷ����
[? ]
A��X��Y��Zһ���Ƿǽ�������
B��X��Y��Z��������һ���ǽ�������
C����X��Y��Ϊ�������ʣ���Z��Ϊ�ǽ�������
D������ΪFeI2�����ҿ���ΪFeCl2
�ο��𰸣�C
���������
�����Ѷȣ�һ��