微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向下列溶液中加入BaCl2溶液,无明显现象.再加入氢氧化钠溶液时,有白色沉淀生成的是
A.KNO3
B.Na2SO4
C.AgNO3
D.NaHCO3
参考答案:D
本题解析:加入氯化钡无明显现象,可排除B、C两项,再加入氢氧化钠后,碳酸氢钠转化碳酸盐,可与钡盐产生碳酸钡白色沉淀.
本题难度:一般
2、选择题 向含有Al3+、Fe2+、Mg2+、NH4+的溶液中,加入过量的NaOH溶液,加热并搅拌,再加过量盐酸,溶液中未减少的阳离子是
[? ]
A.Al3+和Mg2+
B.Al3+和NH4+
C.Fe2+和NH4+
D.只有NH4+
参考答案:A
本题解析:
本题难度:简单
3、选择题 在自然界中的矿物中,CuSO4可将FeS2氧化,生成Cu2S、SO42-和Fe2+。下列表示该反应的离子方程式中,正确的是?(?)
A.14Cu2++5S22-+12H2O=7Cu2S+3SO42-+24H+
B.14Cu2++5FeS2+28OH-=7Cu2S+3SO42-+5Fe2++14H2O
C.14Cu2+ +5FeS2+24OH-=7Cu2S+3SO42-+5Fe2++12H2O
D.14Cu2++5FeS2+12H2O=7Cu2S+3SO42-+5Fe2++24H+
参考答案:D
本题解析:先逆向配平得:14Cu2+ +5FeS2→7Cu2S+3SO42-+5Fe2+。该式左边共有28个单位正电荷,右边共有4个单位正电荷。若仅考虑电荷守恒,可在上式左边加上24个OH-,也可在右边加上24个H+,但Cu2+和Fe2+在碱性环境中会形成沉淀,介质应为酸性,故应在上式右边加上24个H+,得:14Cu2++5FeS2→7Cu2S+3SO42-+5Fe2++24H+,最后用观察法即可配平:14Cu2++5FeS2+12H2O=7Cu2S+3SO42-+5Fe2++24H+。上述选项中,A的电荷不守恒,B、C的介质都是碱性,因此都不对。答案:D。
本题难度:一般
4、选择题 下列电离方程式正确的是(?)
A.NaHSO4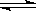 Na++H++SO42一
Na++H++SO42一
B.NaHCO3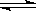 Na++ HCO3一
Na++ HCO3一
C.H2S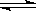 2H++S2-
2H++S2-
D.Mg(OH)2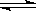 Mg2++2OH-
Mg2++2OH-
参考答案:D
本题解析:用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式。硫酸氢钠、碳酸氢钠是强电解质,应该用等号,AB不正确;H2S是二元弱酸,电离是分步进行的,C不正确,答案选D。
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。该题的关键是准确判断出电解质的强弱,然后具体问题、具体分析即可。
本题难度:简单
5、选择题 下列卤代烃不能发生消去反应生成相同碳原子数的烃的是
A.氯仿
B.碘乙烷
C.1,2-二氯乙烷
D.(CH3)2CHCH2Br
参考答案:A
本题解析:
本题难度:困难