微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关Cl、N、S、Si等非金属化合物的说法不正确的是(?)
A.硅胶、浓硫酸、碱石灰、无水氯化钙都是实验室常用的干燥剂,它们都可以用来干燥NH3、Cl2、SO2、H2等气体
B.将氯气和石灰乳混合可制漂白粉,其有效成分是氯化钙
C.硅是一种良好的半导体材料,可用作做光电池和计算机芯片
D.液氨可用作制冷剂
参考答案:AB
本题解析:无水氯化钙不可以干燥NH3浓硫酸也不可以干燥NH3,A错误。将氯气和石灰乳混合可制漂白粉,其有效成分是次氯酸钙,B错误。
本题难度:一般
2、选择题 下列关于卤素的叙述,错误的是( )
A.单质的颜色随核电荷数的增加逐渐加深
B.单质的氧化性随核电荷数的增加而减弱
C.F2通入NaCl水溶液中反应,生成NaF和Cl2
D.可用硝酸酸化的硝酸银溶液来鉴别Cl―、Br― 、I―离子
参考答案:C
本题解析:A.在卤素单质中,F2是淡黄绿色气体;Cl2是黄绿色气体;Br2是深红棕色液体;I2是紫黑色固体。因此单质的颜色随核电荷数的增加逐渐加深。正确。B.元素的非金属性F>Cl>Br>I,元素的非金属性越强,单质的氧化性就越强,所以卤素单质的氧化性随核电荷数的增加而减弱。正确。C.F2通入NaCl水溶液中发生反应:2F2+2H2O=4HF+O2反应,所以不能生成NaF和Cl2。错误。D.向待测溶液中加入AgNO3溶液,并加入硝酸酸化,若产生白色沉淀,则溶液中含有Cl-;若产生淡黄色沉淀,则含有Br-;若产生黄色沉淀,就证明含有I-。因此可用硝酸酸化的硝酸银溶液来鉴别Cl―、Br― 、I―离子。正确。
本题难度:简单
3、选择题 如图所示,在火棉胶袋(半透膜)内注入淀粉和食盐溶液,用线系紧密封,使细玻管内的液面刚好高出烧杯内蒸馏水的液面,过一段时间后用碘酒和硝酸银溶液分别检验蒸馏水。整个实验过程中,所观察到的现象是
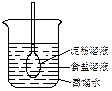
A.细玻管内液面上升
B.细玻管内液面不变
C.蒸馏水遇碘酒变蓝
D.蒸馏水遇硝酸银溶液有白色沉淀生成
参考答案:A、D
本题解析:半透膜袋里的浓度大,因而水进入的比出来的多,细玻璃管液面上升,A正确。食盐中的氯离子通过半透膜进入蒸馏水中,遇硝酸银溶液有白色沉淀生成,而淀粉属于高分子,达到了胶体微粒粒度的范围,不能透过半透膜,因此,加入碘酒不变蓝。
本题难度:简单
4、实验题 实验室用足量MnO2与浓盐酸反应制取氯气,其装置如图1所示:
 ?
?
图1?图2
(1)图1中仪器a的名称是:?;仪器b的名称是:?;b中加入碎瓷片的作用是:?。
(2)请写出仪器b中发生的反应的离子方程式:?
(3)检查装置的气密性之后的操作依次是:?、?、?。(填序号)
A.向烧瓶中加入MnO2粉末
B.加热
C.向烧瓶中加入浓盐酸
(4)该反应会因为盐酸浓度下降而停止。为了测定反应残留液中盐酸的浓度,某探究小组提出下列实验方案:
①甲同学的方案为:与足量AgNO3溶液反应,称量生成沉淀的质量。
②乙同学的方案为:与足量的锌反应,测量生成气体的体积,实验装置如图2所示(夹持装置已略去)。使Y形管中的残留溶液与锌粒反应的正确操作是?(“锌粒转移到残留溶液中”或“残留溶液转移到锌粒中”)。在正确读取量气管读数时,视线要平视,要注意使漏斗液面与量气管中液面相平,除此外还须注意:?。
两种方案我认为?(填甲或乙)同学的方案可行。
参考答案:(1)分液漏斗; 蒸馏烧瓶; 防止液体暴沸
(2)MnO2+4H++2Cl-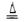 Mn2++2H2O+Cl2↑
Mn2++2H2O+Cl2↑
(3)A、C、B
(4)锌粒转移至残留溶液中; 恢复至室温; 乙
本题解析:图1装置有分液漏斗和蒸馏烧瓶组装而成,加入碎瓷片防止爆沸,检验气密性后,先加入固体,再加液体,最后加热,自下而上,MnO2+4H++2Cl-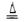 Mn2++2H2O+Cl2↑,盐酸表现还原性和酸性,甲同学检验的是氯离子的量,包括的除了剩余的盐酸,还有表现酸性的盐酸,也就是氯化锰的氯离子。乙同学把锌粒转入盐酸中,保证盐酸完全反应,准确测定盐酸的量,量气管读数时注意:1、回复至室温,2、调节液面相平,3、视线与凹液面相切。
Mn2++2H2O+Cl2↑,盐酸表现还原性和酸性,甲同学检验的是氯离子的量,包括的除了剩余的盐酸,还有表现酸性的盐酸,也就是氯化锰的氯离子。乙同学把锌粒转入盐酸中,保证盐酸完全反应,准确测定盐酸的量,量气管读数时注意:1、回复至室温,2、调节液面相平,3、视线与凹液面相切。
本题难度:一般
5、选择题 今有甲、乙、丙三瓶等体积的新制氯水,浓度均为0.1mol/L。如果在甲中加入少量的碳酸氢钠晶体m mol,在乙中加入少量的亚硫酸氢钠晶体m mol,丙瓶不变,片刻后,甲乙丙三溶液中HClO的物质的量浓度大小关系是(溶液体积变化不计)(?)
A.甲=乙>丙
B.甲>丙>乙
C.丙>甲=乙
D.乙>丙>甲
参考答案:B
本题解析:氯水中存在平衡Cl2+H2O HCl+HClO。次氯酸的酸性其余碳酸氢钠的,所以甲中加入碳酸氢钠只和盐酸反应,促进平衡向向正反应方向移动,次氯酸浓度增大;亚硫酸氢钠具有还原性,次氯酸钠氧化亚硫酸氢钠,所以乙中次氯酸的浓度降低,即答案选B。
HCl+HClO。次氯酸的酸性其余碳酸氢钠的,所以甲中加入碳酸氢钠只和盐酸反应,促进平衡向向正反应方向移动,次氯酸浓度增大;亚硫酸氢钠具有还原性,次氯酸钠氧化亚硫酸氢钠,所以乙中次氯酸的浓度降低,即答案选B。
本题难度:一般