��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪1.505��1023��ij������ӵ�����Ϊ8g����������Ħ��������
A.16g
B.32g
C.64g/mol
D.32g/mol
�ο��𰸣�D
������������������ݹ�ʽN=nNA=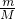 NA�����㼴�ɣ�
NA�����㼴�ɣ�
��𣺸��ݹ�ʽN=nNA=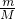 NA����M=
NA����M=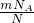 =
=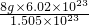 mol-1=32g/mol��
mol-1=32g/mol��
��ѡD��
���������⿼��ѧ���Խ̲�֪ʶ�ļ��䣬���Ը�����ѧ֪ʶ���лش𣬽ϼ�
�����Ѷȣ���
2��ѡ���� ��NA��������ӵ�����������˵������ȷ����
A.48gO3���庬��NA��O3����
B.���³�ѹ�£����ý������������û�1molH2������ת�Ƶĵ�����Ϊ2NA
C.t��ʱ��1?L?pH=6�Ĵ�ˮ�У�����1��10-6NA��OH-
D.��״���£�11.2?L���Ȼ�̼����������Ϊ0.5NA
�ο��𰸣�D
���������������A�������������ʵ������㣻
B������������ԭ��Ӧ�����غ�����������ԭ��ʧ���ӣ���Ԫ��ԭ�ӵõ���������������
C��ˮ����ƽ���� ���������Ӻ�������Ũ����ͬ��
D����״�������Ȼ�̼�������壮
���A��48gO3�������ʵ���Ϊ1mol������NA��O3���ӣ���A��ȷ��
B�����³�ѹ�£����ý������������û�1molH2����������ԭ��ʧ���ӣ���Ԫ��ԭ�ӵõ�������������������ת�Ƶĵ�����Ϊ2NA����B��ȷ��
C��t��ʱ��1 L pH=6�Ĵ�ˮ�У�ˮ����ƽ���� ���������Ӻ�������Ũ����ͬ������1��10-6NA��OH-����C��ȷ��
D����״�������Ȼ�̼�������壬11.2 L���Ȼ�̼���ʵ�������0.5mol����D����
��ѡD��
���������⿼���˰���٤��������Ӧ�ã���Ҫ���������������ʵ���������������������ԭ��Ӧ�����غ����Ӧ�ã�ˮ�ĵ�������������Ħ�����������Ӧ�ã���Ŀ�ϼ�
�����Ѷȣ�һ��
3��ѡ���� NA��ʾ�����ӵ����������й���7.8g�������ƹ����˵����ȷ����
A.������H2O��Ӧ������O2������ĿΪ0.1?NA
B.����������������ĿΪ0.4NA
C.������CO2��Ӧ��ת�Ƶĵ�����ĿΪ0.1?NA
D.����������������ĿΪ0.4NA
�ο��𰸣�C
���������������A������2Na2O2+2H2O�T4NaOH+O2����Ӧ����ʽ���м�����
B���������ƾ������������Ӻ��������ӹ��ɣ�1mol������������3mol���ӣ�
C�����ݹ��������������̼��Ӧ��2Na2O2+2CO2 =2Na2CO3+O2��Ӧ����ʽ���з������
D��1�������Ӻ���10�����ӣ�һ�����������Ӻ���18�����ӣ��ݴ˽��
��𣺹������Ƶ�Ħ��������78g/mol��7.8g�������ƾ���0.1mol��
A���������ƹ���������H2O��Ӧ��2Na2O2+2H2O�T4NaOH+O2�������ݷ���ʽ֪2mol��������������ˮ���Եõ�1mol��������1NA���������ӣ���0.1molNa2O2��ַ�Ӧ����O2�����ʵ���Ϊ0.05mol����������O2������ĿΪ0.05?NA����A����
B��1mol�������ƾ�����2mol�����Ӻ�1mol���������ӹ��ɣ�����1mol������������3mol���ӣ���0.1molNa2O2��0.3mol���ӣ���B����
C�����������������̼��Ӧ��2Na2O2+2CO2 =2Na2CO3+O2���������Թ��������е������һ��ϼ���-1�۱䵽0�ۣ�ÿ����1mol����ת�Ƶ��ӵ���2mol����2NA�����ӣ�����0.1mol�������ƾͿ��ԺͶ�����̼��Ӧת��0.1NA���ӣ���C��ȷ��
D��1mol�������ƾ����к���2mol�����Ӻ�1mol���������ӣ�1�������Ӻ���10�����ӣ�һ�����������Ӻ���18�����ӣ�����1mol�������ƾ����к���38mol���ӣ���0.1molNa2O2������������ĿΪ3.8NA����D����
��ѡC��
���������⿼���йع������Ƶ����ʵ����ļ��㣬�ؼ�����ʱ��ϸ���������������ϵ����ȷ�������ƽṹ����Ŀ�ѶȲ���
�����Ѷȣ�һ��
4��ѡ���� 100mL 1mol?L-1��Ca��HCO3��2��Һ�У�����2.3g�����Ƴ�ַ�Ӧ���й����ʵ���������ȷ���ǣ�NA��ʾ�����ӵ�������
A.A
B.B
C.C
D.D
�ο��𰸣�D
���������������2.3gNa�����ʵ���Ϊ0.1mol����ˮ��Ӧ��������������������������������Ϊ0.1mol������Ϊ0.05mol��100mL1mol?L-1��Ca��HCO3��2��Һ��Ca��HCO3��2��Ϊ0.1mol������������Ca��HCO3��2Ϊ1��1��������ӦCa��HCO3��2+NaOH=CaCO3��+NaHCO3+H2O������0.1molCaCO3��0.1molNaHCO3��
��Һ��HCO3-����ˮ�⡢���룬��Һ��HCO3-�����ʵ���С��0.1mol��N=nNA�����жϣ�
��Ӧ��Na�ǻ�ԭ�������ϼ���0������Ϊ+1�ۣ��ݴ˼���ת�Ƶ�������
����m=nM����̼���������
�������£�����Ħ�������һ����22.4L/mol��
���2.3gNa�����ʵ���Ϊ0.1mol����ˮ��Ӧ��������������������������������Ϊ0.1mol������Ϊ0.05mol��100mL1mol?L-1��Ca��HCO3��2��Һ��Ca��HCO3��2��Ϊ0.1mol������������Ca��HCO3��2Ϊ1��1��������ӦCa��HCO3��2+NaOH=CaCO3��+NaHCO3+H2O������0.1molCaCO3��0.1molNaHCO3��
A����Ӧ��Na�ǻ�ԭ�������ϼ���0������Ϊ+1�ۣ���Ӧ��NaΪ0.1mol����ת�Ƶ���Ϊ0.1NA����Һ��HCO3-����ˮ�⡢���룬��Һ��HCO3-�����ʵ���С��0.1mol����Һ��HCO3-С��0.1NA����A����
B����A������֪ת�Ƶ���Ϊ0.1NA����������Ϊ0.05mol���������£�����Ħ�������һ����22.4L/mol��ռ�е������һ����22.4L����B����
C������̼���Ϊ0.1mol��������=0.1mol��100g/mol=10g����A������֪����Һ��HCO3-С��0.1NA����C����
D������̼���Ϊ0.1mol��������=0.1mol��100g/mol=10g����������Ϊ0.05mol������������ĿΪ0.05NA����D��ȷ��
��ѡD��
���������⿼�鳣�û�ѧ�������йؼ��㡢���ݷ���ʽ�ļ��㡢����ʵĵ��롢����ˮ��ȣ��Ѷ��еȣ�ע������Ħ�������������������
�����Ѷȣ���
5��ѡ���� ���й��ڡ�NaOH���ķ���������
A.������
B.ǿ��
C.������
D.�����
�ο��𰸣�C
������������������������ɲ�ͬ��Ԫ����ɵĴ����
��������ָֻ��������Ԫ�أ�������һ��Ԫ������Ԫ�صĻ����
��ˮ��Һ�������״̬���ܵ���Ļ������ǵ���ʣ���ˮ��Һ����ȫ�����ǵ������ǿ����ʣ����ֵ����ǵ������������ʣ�ǿ�ᡢǿ��ʹֵ�������ǿ����ʣ�
���NaOH����ˮ��Һ�������״̬���ܵ���Ļ�������ڵ���ʣ�����NaOH��ˮ��Һ����ȫ���룬����ǿ����ʣ����������������ѡC��
���������⿼�������ʷ���ļ��ַ�����Ҫע�ⲻͬ�������ݵ��������ϵ��
�����Ѷȣ�����