微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中正确的是
A.发生化学反应时,失去电子越多的金属原子,其还原能力越强
B.目前已发现113种元素,即已发现113种原子
C.核外电子总数不同的原子,可能是同种元素的原子
D.同一元素的各种同位素的化学性质基本相同
参考答案:D
本题解析:A错,还原性的强弱与失去的电子数多少无关,而与失去电子的能力大小有关;B错,元素为质子数相同的核素的总称,元素的种类远少于原子的种类;C错,对于原子,核电荷数=质子数=核外电子数,元素的同类是由质子数决定的;D正确,同位素是指质子数相同而中子数不同的同一元素的不同原子,化学性质基本相同;
本题难度:简单
2、填空题 (6分)在第三周期元 素中,除稀有气体元素外:
素中,除稀有气体元素外:
⑴原子半径最小的元素是?;(填元素符号)
⑵金属性最强的元素是?;(填元素符号)
⑶最高价氧化物对应水化物酸性最强的是?,(用化学式回答,下同):
⑷最不稳定的气态氢化物是?;
⑸最高价氧化物对应水化物碱性最强的是?;
⑹氧化物中具有两性的是?。
参考答案:Cl? Na? HClO4? SiH4? NaOH? Al2O3
本题解析:略
本题难度:一般
3、选择题 氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是
A.35Cl原子所含质子数为18
B.1/18mol的1H35Cl分子所含中子数约为6.02×1023
C.35g35Cl2气体的体积约为11.2L
D.35Cl2气体的摩尔质量为71g.mol-1
参考答案:B
本题解析:A错,35Cl原子所含质子数为17;B正确,1H35Cl分子的中子数为18,所以1/18mol的1H35Cl分子所含中子数约为6.02×1023;C错,未指明标准状况;D错,35Cl2气体的摩尔质量为70g.mol-1
本题难度:一般
4、选择题 有关常见晶体的叙述正确的是(?)
A.氯化铯晶体中,每1个Cs+与其他8个Cs+等距离紧邻
B.干冰晶体中,每1个CO2分子与其他12个CO2分子等距离紧邻
C.石墨中由非极性键构成的最小碳环有6个碳原子,每个该小环平均分配6个碳原子
D.氯化钠晶体中,每个Na+与其他6个Na+等距离紧邻
参考答案:B
本题解析:
【错解分析】掌握晶体结构,特别是氯化钠、二氧化硅的结构
【正解】误区产生一为由CsCl,NaCl中Na+,Cs+与Cl-的比例误导,另一为未很好运用空间想像力。现题中要求是Cs+与Cs+,Na+与Na+在晶体中的等距相邻关系。
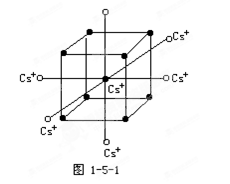
CsCl晶体中每个Cs+周围等距离紧邻关系见图1-5-1所示。可见对于Cs+而言紧邻等距离的Cs+离子数为6个。
NaCl晶体的立方体结构,由Na+与Na+的关系而言,应为12个的关系。
干冰晶体,在教材上图示仅是一个晶胞,仅由此看好像是在每个平面正方形中心的CO2分子与四角的4个CO2紧邻。由立体上诸多晶胞形成的干冰观察,可想象出空间坐标,x,y,z三个轴上有三个平面,每个平面均有1个CO2与4个CO2分子紧邻的关系,所以1个CO2与12个CO2分子等距离紧邻。
石墨的层内由共价键构成的多个正六边形小环,每个碳原子被3个正六边形共用。平均每个小环分配到的碳原子数为6/3=2(个)。
本题难度:简单
5、选择题 下列微粒中半径最小的是(?)
A.Na
B.Na+
C.Mg2+
D.K
参考答案:C
本题解析:微粒半径主要由电子层数及核电荷数来决定
本题难度:一般