微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某化学兴趣小组为探究盛装浓硫酸的铁质材料(碳素钢)与热浓硫酸的反应,设计如下实验。
(1)甲同学没计图一实验装置收集反应产生的气体,写出加热条件下碳素钢与浓硫酸反应生成混合气体的化学方程式_____________________。
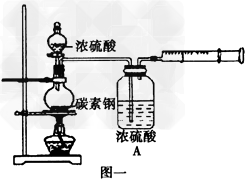
(2)乙同学设计图二实验装置检验甲同学所收集的气体的成分
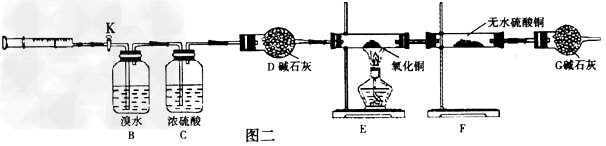
①实验前向B中注入氮气使整个装置充满氮气,实验中将收集到的气体缓缓注入B中,当收集到的气体全部注入B后,还要不断缓缓向B中注入氮气,前后两次向装置中注入氮气,前次的作用是____________,后次的作用是__________________,
②装置B的作用是_________,反应的离子方程式为___________________,
③装置D的作用是__________,装置G的作用是_____________,
④若混合气体中含有氢气,实验过程中能观察到的现象是__________________。
(3)丙同学通过测定混合气体的体积、装置B、D增重的质量来探究混合气体的组成。实验前量取448mL(标准状况下)气体,实验后测得装置B增重0.96g、装置D增重0.088g。
①混合气体中H2的体积分数为_______________;
②若图二实验装置中没有装置C,对实验结果的影响是_______________。
参考答案:(1)2Fe+6H2SO4(浓)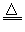 Fe2(SO4)3+3SO2↑+ 6H2O、C+2H2SO4(浓)
Fe2(SO4)3+3SO2↑+ 6H2O、C+2H2SO4(浓)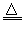 CO2↑+2SO2↑+2H2O、
CO2↑+2SO2↑+2H2O、
Fe+ H2SO4=FeSO4+H2↑
(2)①排出装置中的空气,防止氢气和氧气加热时发生爆炸;使收集到的气体充分反应;
②检验并测定混合气体中的SO2;SO2+Br2+2H2O=4H++SO42-+ 2Br-;③检验并测定混合气体中的CO2;防止空气中的水蒸气进入装置F;④E中固体粉末由黑色变为红色,F中固体由白色变为蓝色
(3)①15%;②CO2的体积分数偏大,H2的体积分数偏小
本题解析:
本题难度:一般
2、选择题 能够用来鉴别BaCl2、KOH、Na2CO3三种物质的试剂是( )
A.AgNO3溶液
B.稀硫酸
C.稀盐酸
D.稀硝酸
参考答案:A.BaCl2、Na2CO3均与AgNO3溶液反应生成白色沉淀,现象相同,不能鉴别,故A错误;
B.BaCl2、KOH、Na2CO3三种物质分别与稀硫酸反应的现象为:白色沉淀、无现象、生成无色气体,现象不同,可鉴别,故B正确;
C.BaCl2、KOH与稀盐酸混合,现象相同,不能鉴别,故C错误;
D.BaCl2、KOH与稀硝酸混合,现象相同,不能鉴别,故D错误;
故选B.
本题解析:
本题难度:一般
3、选择题 用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是( )
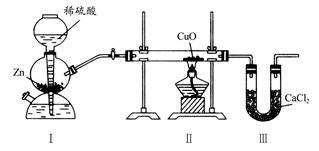
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.CuO没有全部被还原
参考答案:D
本题解析:用H2还原CuO时,装置Ⅲ中CaCl2吸收的是生成的水,而装置Ⅱ中玻璃管通H2前后的质量差为反应时消耗CuO中氧的质量,即生成水中氧元素的质量,而m(水)-m(氧)=m(氢)。当Zn和稀硫酸反应产生的H2不干燥[m(水)偏大],装置Ⅲ后不加干燥装置,使Ⅲ中CaCl2吸收空气中的水分[m(水)偏大],Ⅱ中玻璃管内有水冷凝[m(氧)偏小],都会造成测得m(H):m(O)>1:8。H2O的组成与CuO是否完全反应无关,只与通H2前后玻璃管的质量差和生成的水有关。
本题难度:一般
4、实验题 (10分)某化学学习小组在实验室里利用下图装置测定中和反应中的热效应。实验时将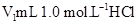 溶液和
溶液和 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持
未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持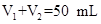 )。
)。
据此请回答下列问题:
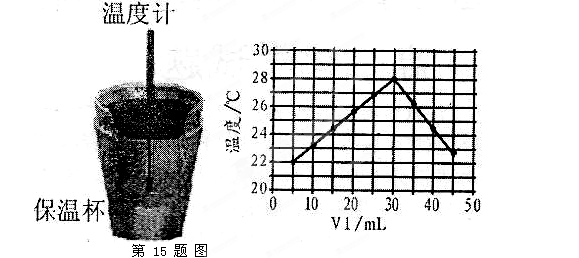 (1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(2)保温杯的作用是_______________________________________________________。
(3)某同学根据所得数据,提出了以下观点,其中正确的是______________________。
A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.该实验表明有水生成的反应都是放热反应
(4)利用图中所给数据,可测得NaOH溶液的浓度约为______________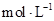
(5)除了使用保温杯外,为了保证实验成功,还要注意哪些问题(说出1点即
可) ____________________________
参考答案:(1)环形玻璃搅拌器(2)防止热量散失(3)B (4)1.5 (5)使用的盐酸和氢氧化钠溶液的浓度要小不要大;温度计的水银球部分要完全浸在溶液中(合理给分)。
本题解析:(1)反应时需要搅拌,所以还缺少环形环形搅拌棒。
(2)在实验中,应该尽可能减少热量的损失,所以保温杯的作用是减少热量的损失。
(3)根据图像可知,当V1=0时,溶液的温度不是22℃,A不正确。随着反应的进行,溶液的温度升高,所以反应放热,B正确。选项C和实验无关系,不正确,答案选B。
(4)当酸碱恰好反应时,放出的热量最多,所以根据图像可判断,氢氧化钠的浓度是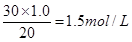 。
。
(5)在实验中,应该尽可能减少热量的损失,所以使用的盐酸和氢氧化钠溶液的浓度要小不要大;温度计的水银球部分要完全浸在溶液中
本题难度:一般
5、实验题 镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含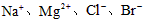 等)中模拟工业生产来提取镁,主要过程如下
等)中模拟工业生产来提取镁,主要过程如下
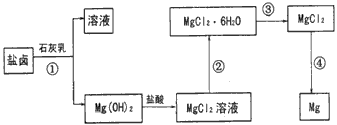
|
回答下列问题:
(1)工业上从盐卤中获取 用石灰乳而不用
用石灰乳而不用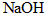 溶液的主要原因是__________________。
溶液的主要原因是__________________。
(2)从过程①得到的 沉淀中混有少量的
沉淀中混有少量的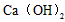 ,除去少量
,除去少量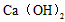 的方法是先将沉淀加入到盛有________溶液的烧杯中,充分搅拌后经__________、___________(填操作方法)可得纯净的
的方法是先将沉淀加入到盛有________溶液的烧杯中,充分搅拌后经__________、___________(填操作方法)可得纯净的 。
。
(3)下图是该兴趣小组设计进行过程③的实验装置图
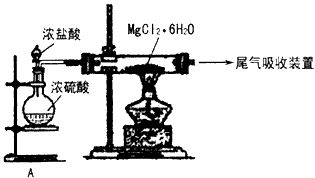
装置A由分液漏斗、________、铁架台(带铁圈)、石棉网、双孔塞和导管组成,该实验装置在过程③中的作用是_________________________。
参考答案:(1)石灰乳原料丰富,成本低
(2) (或氯化镁);过滤;洗涤
(或氯化镁);过滤;洗涤
(3)圆底烧瓶;制备干燥的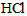 气体,抑制氯化镁水解
气体,抑制氯化镁水解
本题解析:
本题难度:一般