微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 不能说明X的电负性比Y的电负性大的是(?)。
A.与H2化合时X单质比Y单质容易
B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强
C.X原子的最外层电子数比Y原子最外层电子数多
D.X单质可以把Y从其氢化物中置换出来
参考答案:C
本题解析:电负性的大小可依据定义,且和非金属性的强弱一致,因而可根据元
素非金属性的强弱判断。X的电负性比Y大,表明X的非金属性比Y的非
金属性强。A、B、D均能说明X的非金属性比Y强,原子的最外层电子数
不能决定元素得失电子的能力。
本题难度:一般
2、填空题 2.36 g H2O和100 g D2O所含的氧原子数之比为______;分别与足量钠反应后,在标准状况下放出气体的体积比为_____;质量比为_____。
参考答案:2∶5? 2∶5? 1∶5
本题解析:36 g H2O为2 mol,100 g D2O为5 mol。故n(O)∶n(O)=2∶5,V(H2)∶V(D2)=2∶5,W(H2)∶W(D2)=4∶20=1∶5。
本题难度:简单
3、选择题 下列元素中,属于长周期元素的是 ?
A.Li
B.F
C.P
D.Fe
参考答案:D
本题解析:考查周期表的结构。周期表分为7个周期,前三周期属于短周期,第4、5、6周期属于长周期,第7周期属于不完全周期。所以答案选D。
本题难度:简单
4、选择题 第ⅤA族元素中的A、B两种元素所在周期分别最多可排18和8种元素,且B在A的上一周期,当A的原子序数为x时,B的原子序数为
( )。
A.x-18? B.x-8? C.x+8? D.x+18
参考答案:A
本题解析:据题意可知A、B在周期表中的相对位置为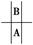 ,且在第ⅤA族,A所在周期元素种类数为18,所以B的原子序数应为x-18。
,且在第ⅤA族,A所在周期元素种类数为18,所以B的原子序数应为x-18。
本题难度:一般
5、填空题 (8分)下表列出了①~⑥六种元素在元素周期表中的位置。
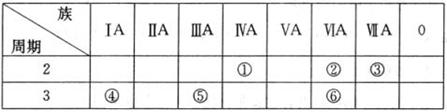
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是__ __(填写元素符号);
(2) ②、⑥两种元素的原子半径大小为:② ⑥(填“<”或“>”);;
(3) 元素①的原子结构示意图??;?
(4)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是
______________?____________。
参考答案:(1)F (2)<(3)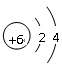 (4)Al(OH)3+OH-=AlO2-+2H2O
(4)Al(OH)3+OH-=AlO2-+2H2O
本题解析:考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断①~⑥分别为C、O、F、Na、Al、S。
(1)同周期元素自左向右非金属性逐渐减弱,所以非金属性最强的是F。
(2)同主族元素自上而下原子半径逐渐增大,所以S的原子半径大于O的原子半径。
(3)C的原子序数是6,所以原子结构示意图为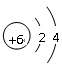 。
。
(4)④、⑤两种元素的最高价氧化物对应的水化物分别是氢氧化钠和氢氧化铝,氢氧化铝是两性氢氧化物能溶于强碱,方程式为Al(OH)3+OH-=AlO2-+2H2O。
本题难度:一般