��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪��ͼÿһ�����е���ĸ����һ�ַ�Ӧ��������ͼ�в���������û���г�����������A����1828��¹���ѧ��ά��ͨ����������淋õ����л��Ϊ�ˣ������״������л�������ֻ���������ϸ������ȡ�ġ����������ۣ�A�Ļ�ѧʽ�ɱ�ʾΪXY4ZM2�����A������Ԫ�ض��Ƕ�����Ԫ�أ���ԭ������֮��Ϊ22��X��M��Z�ֱ�λ�����ڵ����壬ԭ��������������C��D��G��I��J��KΪ���壬����C��K������ЧӦ��������K�Ǻ�������ߵ��л��D��ʹʪ��ĺ�ɫʯ����ֽ������BΪһ�ְ�ɫ���壬�����ʽ�ɱ�ʾΪXY2M2��E�Ļ�ѧʽ�ɱ�ʾΪX3M4���밴Ҫ��ش��������⣮
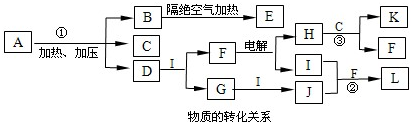
��1��AҲ��һ�ֳ��õķ��ϣ���������______��Ŀǰ��ҵ����______��______��һ���������Ƶã�
��2����Ӧ�٢ڢ۵Ļ�ѧ����ʽ�ֱ�Ϊ______��______��______��
��3��I��B��M����������Ϊ______����B��һ�����������ķ��ӣ��ӽṹ�Ͽɿ����������ӣ�XY2M2���ۺ϶��ɣ���һ�ֵͶ��Ļ���ԭ�ϣ�ijЩ�����������̷�������B����������������ġ�Ӥ���̷��¼������ݴˣ����㻭��B�Ľṹ��ʽ______��
II����֪�����ӵļ���Ϊ107��18�䣬���й���B��˵������ȷ����______��������ţ�
�ٺ��в�����̼ԭ�ӣ���һ���������ܷ����ӳɷ�Ӧ
���������ᷴӦ������
����һ���������ܷ���������Ӧ
�ܷ���������ԭ�Ӷ���ͬһƽ����
���ڸ����·ֽ�ų�N2���ʿ�������ȼ��
����һ�������¿������������ӳɷ�Ӧ
�ߺ���������A�ĺ�����
������һ�ּ��Ի���������ڼ״�����ȩ���л���
�����ʳ�ú�B��Ⱦ�̷۵�Ӥ�����������ʯ������ϵͳ����
���ǰ�ɫ��ĩ���д̼�����ζ
��4��������E��һ�����������ϣ�����һ�ֽṹ����-X3M4�����п�����ʯ��������Ӳ�ȣ����Ʋ�ò��Ͽ��ܵ���;֮һ��______��
��5��Һ̬D����H2O��Ҳ���������Ҳ�����������ͬ���������ӣ���Һ̬D���뷽��ʽΪ______��
��6�����ڽṹ��N2H4��D�Ĺ�ϵ����H2O2��H2O�Ĺ�ϵ��N2H4�ܷ������з�Ӧ��
N2H4+H3O+�TN2H+5+H2O?N2H4+H2O�TN2H5++OH-
N2H5++H2O�TN2H62++OH-?N2H5++H2O�TN2H4+H3O+
�ݴ˿ɵó��Ľ�����______��
A����ˮ�������ԡ�����������������?B������ˮ�е����H+����
C�����Ƕ�Ԫ�������������������?D�����Ƕ�Ԫ����
�ڷ��䡰�����ߺš��ɴ��ij���2�Ż�������£�N2H4����ȼ�ϣ����������������������߷�Ӧ���ɵ�������̬ˮ����֪4g?N2H4��g����������Ӧ�зų�71kJ��������д���Ȼ�ѧ����ʽ______��
�ο��𰸣��������ӡ�C��K������ЧӦ����������֪C��K������CO2��CH4���ӡ�K�Ǻ�̼����͵��л����֪KΪCH4��CΪCO2���ӡ�D��ʹʪ��ĺ�ɫʯ����ֽ��������֪��DΪNH3���Ӷ�����֪A�к���C��H��O��N4��Ԫ�أ��ٴӡ����A������Ԫ�ض��Ƕ�����Ԫ�أ���ԭ������֮��Ϊ22��X��M��Z�ֱ�λ�����ڵ����壬ԭ��������������֪���б�����Ԫ�أ���YΪ�⣬XΪ̼��MΪ����ZΪ��������ʵ��ʽΪ��N2H4CO����A�ɷֽ������������ʣ�CH2N2��CO2��NH3�����жϳ�A�ķ���ʽΪCO?��NH2��2����Ϊ���أ�Ŀǰ��ҵ����CO2��NH3��һ�������·�Ӧ���Ƶã�CO2+2NH3
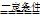
CO?��NH2��2+H2O���ٴ�NH3��G��J�ı仯������ͬһ������I���𣬹ʶ��жϳ�IΪO2�������Ƴ�FΪH2O��HΪH2��LΪHNO3���ƶ�����Ϊ��A��CO ��NH2��2��B��C3H6N6��C��CO2��D��NH3��F��H2O��G��NO��H��H2��I��O2��L��HNO3��J��NO2��K��CH4��
��1��AҲ��һ�ֳ��õķ��ϣ��ƶ�Ϊ���أ�����Ϊ�����ػ�̼�����������̼������Ŀǰ��ҵ����CO2��NH3��һ�������·�Ӧ���Ƶã�CO2+2NH3
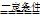
CO ��NH2��2+H2O��
�ʴ�Ϊ�����ػ�̼�����������̼������CO2��NH3
��2����Ӧ�٢ڢ۵Ļ�ѧ����ʽ�ֱ�Ϊ��6��NH2��2CO��C3H6N6+NH3��+3CO2����4NO2+O2+2H2O=4HNO3 ��CO2+4H2��CH4+2H2
��3����BΪ�����谷����Ԫ�صĺ������ݷ���ʽC3H6N6����Ϊ66.7%���ṹ��ʽΪ��
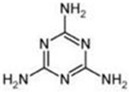
��
�ʴ�Ϊ��66.7%

�����ڵĽṹ��ʽ�к��в�����̼���ʶ���һ���������ܷ����ӳɷ�Ӧ���������ʢ���ȷ��
�ڰ����Լ��Ժ����ᷴӦ�����Σ��ʢ���ȷ��
�����ڵĽṹ��ʽ�к��в�����̼���ʶ���һ���������ܷ����ӳɷ�Ӧ���������ʢ���ȷ��
���������NH3�ļ���Ϊ107��18�䣬��-NH2�е�����ԭ�Ӳ�������ͬһƽ���ϣ��ʢܴ���
���ڸ����·ֽ�ų������ȶ���N2���ʿ�������ȼ�����ʢ���ȷ��
�����ڵĽṹ��ʽ�к��в�����̼���ʶ���һ���������ܷ����ӳɷ�Ӧ���ʢ���ȷ��
�����صĺ���Ϊ46.67%���������谷�ĺ�����Ϊ66.7%������������A�ĺ��������ʢߴ���
�������谷Ϊ����ˮ�������Ϊ���Է��ӣ�����һ�ּ��Ի���������ڼ״�����ȩ���л���ʢ���ȷ��
�����ʳ�ú������谷��Ⱦ�̷۵�Ӥ�����������ʯ������ϵͳ�������ʢ���ȷ��
���ǰ�ɫ���壬��ζ���ʢ����
�ʴ�Ϊ���ܢߢ�
��4��������E��һ�����������ϣ�����һ�ֽṹ����-X3M4�����п�����ʯ��������Ӳ�ȣ�����Ӳ�����������Ʋ�ò��Ͽ��ܵ���;֮һ�ǣ�����ĥ���ϡ����²��ϵ�
��5��Һ̬D����H2O��Ҳ���������Ҳ�����������ͬ���������ӣ���Һ̬D���뷽��ʽΪ����ˮ�ĵ���Ϊ2H2O
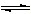
H3O++OH-��ͨ����Ȳ��ѵó�Һ̬NH3���뷽��ʽΪ��2NH3?

NH4++NH2-��?�ʴ�Ϊ��2NH3

NH4++NH2-��
��6���ٽṹ��N2H4��D�Ĺ�ϵ����H2O2��H2O�Ĺ�ϵ����N2H4�� N2H5+��صķ�Ӧ��֪��1mol N2H4���Խ��1molH+�γ�1mol N2H5+��1mol N2H4Ҳ���Խ��2molH+�γ�1mol N2H62+������ˮ��Һ�Լ��ԣ����Ƕ�Ԫ�����ѡC���ʴ�Ϊ��C��
��4g?N2H4�����ʵ���Ϊ0.125mol����1molN2H4��Ӧ�зų�������Ϊ568kJ�������Ȼ�ѧ����ʽΪ��N2H4��g��+NO2��g��=32N2��g��+2H2O��g������H=-568kJ/mol��
�ʴ�Ϊ��N2H4��g��+NO2��g��=32N2��g��+2H2O��g������H=-568kJ/mol
���������
�����Ѷȣ�һ��
2������� ��8�֣�����ͼ��ʾ���ʼ���ת���ϵ����Ӧ���ڹ�ҵ�Ͽ���������������C����Ӧ���ڹ�ҵ�Ͽ�����������J��Na2FeO4������Ӧ�١��ڡ��ܺ͢ݾ�����ˮ��Һ�н��еķ�Ӧ��������D��E��G�������壬B����ɫҺ�壻F��ˮ��Һ����Ϊɱ����������H��һ������ʯ����Ҫ�ɷ֣���������Ԫ����ɣ���������Ԫ�ص���������Ϊ70%��
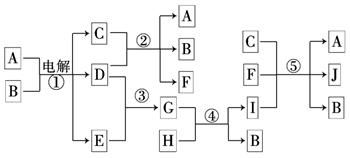
��ش��������⣺
��1��д��F�Ļ�ѧʽ��________________��
��2�����ǽ���Ӧ���漰�Ļ�ѧ��ҵ��Ϊ ________________��
��3��д��B��D��Ӧ�����ӷ���ʽ____________________________________ ____��
____��
��4��д����Ӧ�ܵ����ӷ���ʽ____________________________ __________________��
__________________��
��5��д����Ӧ�ݵ����ӷ���ʽ_____________________________________________ _��
_��
��6���������ƣ�Na2FeO4����������Ϊ��һ�֡���ɫ������Ч���ľ�ˮ������ԭ��Ϊ��
��Na2FeO4����ǿ�����Կ�ɱ��������
��___________________________________________________________________
�ο��𰸣���1�� NaClO��1�֣�?
��2���ȼҵ��1�֣�
��3��Cl2�� H2O = H+��Cl-��HClO����1�� ��
��4��Fe2O3��6 H+=2Fe3����3H2O��1�֣�
��5��2Fe3����3ClO����10OH��===2FeO��3Cl����5H2O��2�֣�
��6��Na2FeO4����ԭΪFe3����Fe3��ˮ������Fe��OH��3����������ˮ�е�������������γɳ�����ʹˮ���壨2�֣�
�����������
�����Ѷȣ���
3������� A��B��C��D�������ʶ�����ͬ��Ԫ��������ͼ��ʾת����ϵ���Իش��������⣺
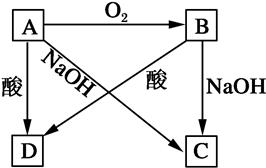
��1����A��һ�ֳ����ǽ���������һ�ְ뵼����ϡ�д�����з�Ӧ�ķ���ʽ��
��B��D�Ļ�ѧ����ʽ��__________________________________________________��
��A��C�����ӷ���ʽ��__________________________________________________��
��2����A��һ�ֳ�����������ʱ��Ϊǿ�ᡣд����A��D�����ӷ���ʽ��__________________________��
�ο��𰸣���1����SiO2��4HF��2H2O��SiH4��?��Si��2OH����H2O��SiO32����2H2��
��2��2Al��6H����2Al3����3H2��
�����������ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȣ��ݴ˿����жϡ�
��1����A��һ�ֳ����ǽ���������һ�ְ뵼����ϣ���A�ǵ��ʹ衣�赥����������Ӧ���ɶ������裬��B��SiO2�����������������������ܺ�����������Һ��Ӧ���ɹ����ƺ�ˮ����C�ǹ����ƣ����ʹ�Ҳ�ܺ�����������Һ��Ӧ���ɹ����ƺ����������Ƿǽ������ʣ�ֻ�ܺ�����ᷴӦ�����ķ��������������������Ҳ�ܺ�����ᷴӦ�����ķ������ˮ����D��SiH4�����
��B��D�Ļ�ѧ����ʽΪSiO2��4HF��2H2O��SiH4����
A��C�����ӷ���ʽΪSi��2OH����H2O��SiO32����2H2����
��2����A��һ�ֳ����������������ܺ�����������Һ��Ӧ���ǽ���������A��Al������������ȼ����������������B������������������������Һ��Ӧ����ƫ�����ƺ���������C��ƫ�����ơ������������������Ҳ�ܺ�����������Һ��Ӧ����ƫ�����ơ������ʱ��Ϊǿ�ᣬ��D�����Σ�����A��D�����ӷ���ʽΪ2Al��6H����2Al3����3H2����
�����Ѷȣ�����
4������� ��Fe�ۡ�Cu�ۡ�FeCl3��Һ��FeCl2��CuCl2��Һ�������ij�����г�ַ�Ӧ���ٶ����������뷴Ӧ�������ж������������Һ�д��ڵĽ������Ӻͽ������ʡ�
��1����������ʣ�࣬�������в�����?��
��2�����Ȼ�ͭ��ʣ�࣬�������л�������?��
��3�����Ȼ������Ȼ�ͭ����ʣ�࣬�������в�������?��?������?��
��4�����Ȼ�����ʣ�࣬�������в�������?��
�ο��𰸣���1��Fe3+��Cu2+��?��2��Fe2+��Fe3+��Cu��Fe2 +��3��Fe��Cu ��Fe2+ ?��4��Fe��Cu��
�����������
�����Ѷȣ���
5������� ��10�֣���ջش�
��1����������һ�ָ����մɲ��ϡ�����Ԫ��������֪ʶ��д��������Ļ�ѧʽ��??��
��2����A��B��C��D��E��F����Ԫ�أ����Ǿ���������Ԫ�أ���ԭ�����������������������γɵĻ����������¼��֣�
�γɵĻ�����
| ��
| ��
| ��
| ��
| ��
|
�������и�Ԫ�ص�ԭ�Ӹ�����
| A:C=1:1
| B:A=1:3
| D:C=1:1
| E:F=1:3
| A:F=1:1
|
��֪A��B��Ԫ�صĺ˵����֮�������ԭ������������֮�ͣ�Bԭ�������������ȴ�����������3����Cԭ�ӵ������������Ǵ�����������3����D��E��Fͬ���ڣ�D��Aͬ���壻E��F��ԭ������֮��Ϊ30���������ӻ�����ش�
�� FԪ��λ�����ڱ��е�λ��??��
�� EԪ�ص�ԭ�ӽṹʾ��ͼΪ?���ҵĵ���ʽΪ??�����ĵ���ʽΪ??��B������������ˮ����Ļ�ѧʽΪ?��
�����ˮ��Һ�м���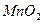 ����Ӧ�Ļ�ѧ����ʽΪ?��
����Ӧ�Ļ�ѧ����ʽΪ?��
�ο��𰸣���1��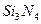 ��1�֣�
��1�֣�
��2���ٵ������ڵ�VIIA�壨1�֣�?
��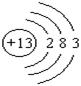 ��1�֣�?
��1�֣�?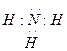 ?��2�֣�?
?��2�֣�?
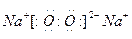 ��2�֣�?
��2�֣�?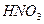 ��1�֣�
��1�֣�
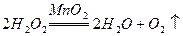 ��2�֣�
��2�֣�
�����������
�����Ѷȣ���