微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 不能用2H + + CO32- = CO2↑+H2O表示的反应是?
A.醋酸溶液与碳酸钠溶液反应
B.稀盐酸与碳酸钠溶液反应
C.稀硫酸与碳酸钾溶液反应
D.硫酸氢钠溶液与碳酸钾溶液反应
参考答案:A
本题解析:略
本题难度:简单
2、填空题
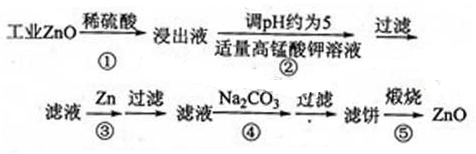
提示:在本实脸条件下,Ni(Ⅱ)不能被氧化:高锰酸钾的还原产物是MnO2
回答下列问题:
(1)反应②中除掉的杂质离子是??,发生反应的离子方程式为 ?;在加高锰酸钾溶液前,若pH较低,对除杂的影响是?。
(2)反应③的反应类型为?,过滤得到的滤渣中,除了过量的锌外还有?。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是?。
(4)反应④中产物的成分可能是ZnCO3・xZn(OH)2取干操后的滤饼11.2g,煅烧后可得到产品8.1g,则x等于?。
参考答案:(1)Fe2+和Mn2+;
MnO4-+3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+;
3Mn2++2MnO4-+2H2O===5MnO2↓+4H+;不会形成Fe(OH)3和MnO2沉淀。或无法除去Fe2+和Mn2+;
(2)置换反应;Ni
(3)取最后一次洗涤液少量,滴入稀盐酸,加入氯化钡溶液,没有白色沉淀生成,证明洗涤干净。
(4)1
本题解析:
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,发生的离子方程式为MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;?
(2)反应③为锌与镍离子的发生反应得到锌离子和镍,反应类型为置换反应;得到的滤渣中,除了过量的锌外还有金属镍。
(3)取最后一次少量水洗夜于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净。
(4)根据关系式
ZnCO3?xZn(OH)2~(x+1)ZnO
125+99x?81(x+1)
11.2g? 8.1g
解得:x=1
本题难度:一般
3、选择题 下列离子方程式正确的是
[? ]
A.用醋酸除去水垢: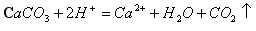
B.苯酚与碳酸钠反应:C6H5OH+CO32- → C6H5O-+CO2↑+H2O
C.苯酚钠溶液中通入少量CO2: CO2 + H2O + C6H5O- →C6H5OH + HCO3-
D.乙酸乙酯与氢氧化钠溶液反应: CH3COOC2H5+OH- →CH3COOH + C2H5O-
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列离子方程式正确的是?(?)
A.纯碱溶液显碱性的化学原理:CO32-+2H2O 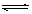 H2CO3+2OH-
H2CO3+2OH-
B.在偏铝酸钾溶液中滴加入足量稀盐酸:AlO2-+H++H2O=Al(OH)3↓
C.澄清石灰水中通入少量CO2气体:Ca2++2OH-+CO2=CaCO3↓+H2O
D.Fe粉与足量稀硝酸反应:3Fe+8H++2NO3-=3Fe2++2NO↑+4 H2O
参考答案:C
本题解析:A.多元弱酸盐水解分步进行,且以第一步为主:CO32-+H2O 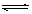 HCO3-+OH-
HCO3-+OH-
B.得到的Al(OH)3沉淀会溶于强酸:AlO2-+4H+=Al3++2H2O
C.正确
D.稀硝酸过量,铁只能以Fe3+形式存在:Fe+4H++NO3-=Fe3++NO↑+2H2O
本题难度:一般
5、选择题 能正确表示下列化学反应的离子方程式是
[? ]
A.碳酸钙与盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
B.铜片与浓硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O
C.二氧化锰与浓盐酸反应: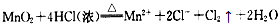
D.硫酸铜与氢氧化钡反应:Ba2++SO42-=BaSO4↓
参考答案:A
本题解析:
本题难度:简单