��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��4�֣����ʵ���Ũ����ͬ�� �� ��ˮ �� �Ȼ�� �� ̼����� �� ������� �� �����������Һ��c��NH4+����С��˳����__________________����ҺpH��С��˳����__________________��
�ο��𰸣��ݢܢڢۢ٣� �٢ۢڢݢ�
���������1Ħ��������ܵ����2Ħ��笠����ӣ�����笠�����Ũ�����1Ħ��������狀�̼����泥��Ȼ�臨��ܵ����1Ħ��笠����ӣ�����������������Ӵ�������笠�����ˮ�⣬̼������ٽ�笠�ˮ�⣬�������������笠�Ũ�ȴ����Ȼ�林���̼����泥���ˮ�����������ȫ���룬����笠�����Ũ����С����ˮ�Լ��ԣ�̼�������˫ˮ�⣬��Һ�Լ��ԣ��������笠������Ȼ�泥�ˮ���笠����Ӷ࣬����ǿЩ��������淋���������ӣ���Һ�����ԣ�����pH��С������pH��˳��Ϊ�٢ۢڢݢ�
���㣺��Һ�е�����Ũ�Ⱥ�pH�ıȽϣ�
�����Ѷȣ�һ��
2��ѡ���� ������ʵ����ʵ�ó��Ľ�����ȷ����
[? ]
��������������������ʵ����ʵ��������������������������������
A������������Cl2��ˮ��Һ���Ե��硡������������������Cl2�ǵ����
B���ڿ�����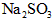 �ױ��ʣ�
�ױ��ʣ� ���ױ��ʡ��������ԣ�
���ױ��ʡ��������ԣ�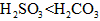
C������C6H5ONa��Һ��ͨCO2������ֻ��ǡ������������ԣ�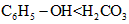
D�������°�����ȼ���������ڷŵ�ʱ����������Ӧ�������ǽ����ԣ�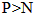
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ��״���£���2.24LNH3ͨ��1L 0.1mol/L�Ĵ�����Һ�У���ȷ��������Һ��NH4+��CH3COO-��H+��OH-Ũ�ȴ�С˳��ͨ���������ݼ��ɵó���ȷ���۵���
A��NH3��H2O��CH3COOH�ĵ��볣��
B��NH3��H2O��CH3COONH4�ĵ��볣��
C����Һ��pH
D�������Ӧ�����
�ο��𰸣�AC
�����������
�����Ѷȣ�һ��
4��ѡ���� ij�¶���HF�ĵ��볣��Ka=3.3��10-4 mol��L-1��CaF2���ܶȻ�����Ksp=1.46��10-10��mol��L-1��3���ڸ��¶���ȡŨ��Ϊ0.31 mol��L-1��HF��Ũ��Ϊ0.002 mol��L-1��CaCl2��Һ�������ϡ�����˵����ȷ���ǣ�?��
A�����¶��£�0.31 mol��L-1��HF��Һ��pH=2
B�������¶Ȼ�����Ũ�ȣ�HF�ĵ���ƽ�ⳣ����������
C������Һ��ϲ����������
D���͵�CaF2��Һ�м�ˮ��c(Ca2+)һ���ȼ�ˮǰ��С
�ο��𰸣�A
���������A�����볣��Ka��HF����3.3��10-4��HFΪ������ʣ�������ȫ���룬25��ʱ��0.31mol/LHF��Һ��c��H+����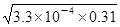 ��1��10��2mol/L��pH��1����A��ȷ��B�����볣��ֻ���¶ȵ�Ӱ�죬����Ũ�ȵı仯���仯����B����C��0.31 mol/L��HF��Һ��c��H+����c��F-����1��10��2mol/L����C�����ڸ��¶���ȡŨ��Ϊ0.31 mol��L-1��HF��Ũ��Ϊ0.002 mol��L-1��CaCl2��Һ�������Ϻ�c��F-����0.5��10��2mol/L��c��Ca2+����0.001mol/L����c2��F-����c��Ca2+������0.5��10��2��2��0.001��2.5��10��8��1.46��10-10����˸���ϵ����CaF2������������C����ȷ��D���͵�CaF2��Һ�м�ˮ����Һ�������DZ��͵ģ�����c(Ca2+)��һ���ȼ�ˮǰ��С��D����ȷ����ѡA��
��1��10��2mol/L��pH��1����A��ȷ��B�����볣��ֻ���¶ȵ�Ӱ�죬����Ũ�ȵı仯���仯����B����C��0.31 mol/L��HF��Һ��c��H+����c��F-����1��10��2mol/L����C�����ڸ��¶���ȡŨ��Ϊ0.31 mol��L-1��HF��Ũ��Ϊ0.002 mol��L-1��CaCl2��Һ�������Ϻ�c��F-����0.5��10��2mol/L��c��Ca2+����0.001mol/L����c2��F-����c��Ca2+������0.5��10��2��2��0.001��2.5��10��8��1.46��10-10����˸���ϵ����CaF2������������C����ȷ��D���͵�CaF2��Һ�м�ˮ����Һ�������DZ��͵ģ�����c(Ca2+)��һ���ȼ�ˮǰ��С��D����ȷ����ѡA��
�����Ѷȣ�һ��
5������� ������c��H+��=0.1mol/L������һԪ��HX��HY����Һ��50mL���ֱ����������þ�ۣ���ַ�Ӧ���ռ�H2�����ΪV��HX����V��HY������V��HX����V��HY�������á�������������=����գ���
��1��Ũ�ȣ�c��HX��______c��HY����?����ǿ����HX______HY��
��2����ʼʱ�������������ʣ�v��HX��______v��HY������Ӧ�������������������ʣ�v��HX��______v��HY������Ӧ��Ϻ���Һ���ε�Ũ�ȣ�c��MgX2��______c��MgY2����
�ο��𰸣���1����Hԭ���غ�֪�����ɵ��������Խ������������ʵ���Խ�࣬����Һ�������ͬʱ��������ʵ���Խ�࣬��Һ��Ũ��Խ������c��HX����c��HY����?
��Ϊc��HX����c��HY��������Һ��c��H+����ȣ�����HX�ĵ���̶�С��HY�ĵ���̶ȣ�����̶�Խ���������Խǿ������HX ������С��HY�����ԣ�
�ʴ�Ϊ����������
��2�����ӵ�Ũ��Խ��Ӧ����Խ�죬�տ�ʼʱ��������Ũ����ͬ�����Է�Ӧ������ȣ����ŷ�Ӧ�Ľ��У�������Ũ�ȼ�С���������������Ӳ�����ٵ����ӣ�����HX ��������Ũ�ȴ���HY��������Ũ�ȣ����Է�Ӧ�������������������ʣ�v��HX����v��HY������Һ��c��HX����c��HY����������ԭ���غ�֪��������þ��Ӧ����Һ���ε�Ũ��
c��MgX2����c��MgY2�����ʴ�Ϊ���T����������
���������
�����Ѷȣ�һ��