微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氮气及含氮的化合物在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2 mol NH3,放出92.4 kJ热量。
(1)若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则Q 184.8kJ(填“>”、“<”或“=”)。一定条件下,在密闭恒容的容器中,能表示反应达到化学平衡状态的是 。
a.3v逆(N2)=v正(H2) b.2v正(H2)= v正(NH3)
c.混合气体密度保持不变 d.c(N2):c(H2):c(NH3)=1:3:2
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为
2NH3 (g)+ CO2 (g) CO(NH2)2 (l)+ H2O (l)。
CO(NH2)2 (l)+ H2O (l)。
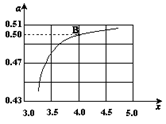
(2)在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)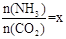 ,右图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
,右图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
(3)图中的B点处,NH3的平衡转化率为 。
(4)已知: 3Cl2+2NH3→N2+6HCl
2、选择题 美国亚利桑那州大学(ASU)和阿贡国家实验室的科学家最近设计出生产氢气的人造树叶,原理为:2H2O(g) 2H2(g)+O2(g)。有关该反应的说法正确的是
2H2(g)+O2(g)。有关该反应的说法正确的是
A.△H <0?
B.△S <0?
C.化学能转变为电能?
D.氢能是理想的绿色能源
3、选择题 在密闭容器中进行反应X2(g)+3Y2(g)?2Z2(g),若X2、Y2、Z2的起始浓度分别为0?1mol/L、0?3mol/L、0?2mol/L,达到平衡时下列物质的浓度可能为( )
A.X2为0?2mol/L
B.Y2为0?2mol/L
C.Z2为0?4mol/L
D.Y2为0?6mol/L
4、选择题 工业制硫酸中,存在可逆反应2SO2(g)+O2(g)?2SO3(g),在已达到平衡后的反应容器中充入少量18O2,一段时间后18O存在于( )
A.O2
B.O2和SO2
C.O2和SO3
D.SO2、O2和SO3
5、选择题 在一个密闭容器中发生如下反应:2SO2?(g)+O2(g)?2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2mol?L-1、0.1mol?L-1、0.2mol?L-1,当反应达到平衡时,可能出现的数据是( )
A.C(SO3)=0.4?mol?L-1
B.C(SO3)+C(SO2)=0.15?mol?L-1
C.C(O2)=0.3?mol?L-1
D.C(SO3)+C(SO2)=0.4?mol?L-1