|
高中化学知识点讲解《有关氧化还原反应的计算》在线测试(2017年最新版)(八)
2017-09-25 16:37:18
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在100ml硝酸和硫酸的混合液中,两种酸的物质的量浓度之和是0.6mol/l.向混合液中加入足量的铜粉,加热充分反应,所得溶液中铜离子的物质的量浓度最大值为(忽略反应前后溶液体积变化)
A.0.30mol/l
B.0.225mol/l
C.0.45mol/l
D.0.36mol/l
|
参考答案:D
本题解析:由反应3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知当硫酸与硝酸按3:2混合时,生成铜离子的浓度最大,最大值为0.36mol/l;答案选D。
考点:氧化还原反应,离子反应
本题难度:一般
2、选择题 下列哪组微粒互称为同位素(?)
A. 和 和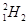
B.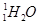 和 和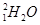
C.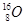 和 和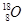
D.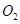 和 和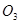
参考答案:C
本题解析:略
本题难度:一般
3、简答题 用100g?9.8%?H2SO4溶液和足量金属Zn反应,可以得到标准状况下气体多少升?(要求有简要步骤)
参考答案:n(H2SO4)=100g×9.8%98g/mol=0.1mol,
?9.8%H2SO4溶液为稀硫酸,和足量金属Zn反应生成硫酸锌和氢气,
H2SO4+Zn=ZnSO4+H2↑
1mol? 22.4L
0.1mol? V(H2)
V(H2)=22.4L×0.1mol1mol=2.24L,
答:得到标准状况下气体2.24L.
本题解析:
本题难度:一般
4、填空题 酒后驾车。这时酒精(CH3CH2OH)被K2Cr2O7氧化为醋酸(CH3COOH)。该氧化还原反应的方程式可表示为:2K2Cr2O7+3CH3CH2OH+8H2SO4→2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O?
在这一反应中,氧化剂是?,还原剂________,氧化产物是?,还原产物是?。
参考答案:(4分)K2Cr2O7;CH3CH2OH; CH3COOH;Cr2(SO4)3
本题解析:根据反应的方程式可知,Cr元素的化合价从+6价降低到+3价,得到3个电子。乙醇中碳元素的化合价从-2价升高到0价,失去2个电子,所以氧化剂是K2Cr2O7,还原剂是CH3CH2OH,氧化产物是CH3COOH,还原产物是Cr2(SO4)3。
点评:该题是基础性试题的考查,难度不大。该题的关键是准确标出有关元素的化合价变化情况,然后结合题意具体问题、具体分析即可,学生不难得分。
本题难度:一般
5、实验题 某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质。设计了如下图所示装置进行实验.?
已知:1.0 mol/L的Fe(NO3)3溶液的pH=1。
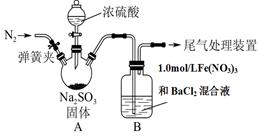
请回答:
(1)装置A中用于添加浓硫酸的仪器名称为?。
(2)实验前鼓入N2的目的是?。
(3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性。
(4)分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与NO3-反应;
①若观点1正确,除产生沉淀外,还应观察到的现象是?。
②按观点2,装置B中反应的离子方程式是?,
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是(填序号)?。
A.1 mol/L稀硝酸
B.1.5 mol/L Fe(NO3)2溶液
C.6.0 mol/L NaNO3溶液和0.2 mol/L盐酸等体积混合的溶液
D.3.0 mol/L NaNO3溶液和0.1mol/L硫酸等体积混合的溶液
参考答案:(1)分液漏斗(2分)
(2)排净装置中的空气,防止溶液中SO2被空气中的O2氧化而干扰实验(2分)
(3)BaSO4(1分);还原(1分)
(4)①静置一段时间后,溶液由棕黄色变为浅绿色(2分)
②3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+
或3SO2+2NO3-+2H2O=3SO42-+2NO+4H+;Ba2++SO42- = BaSO4↓(2分)
③?C(2分)
本题解析:(2)反应前要充入N2,排除装置A中的空气,反应对实验的干扰。
(3)硝酸具有氧化性,白色沉淀为BaSO4,说明SO2具有还来源:91 考试网原性。
(4)经过分析,各个观点,得出观点1是SO2和Fe3+、酸性条件下NO3-都反应。
①Fe3+把SO2氧化,离子方程式是SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+。
②Fe(NO3)3中有Fe3+,a错;NO3-在酸性条件下有氧化性,b错。故选c。
SO2制备 Fe3+、NO3-的氧化性。2制备 Fe3+、NO3-的氧化性。
本题难度:一般
|