��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���з�Ӧ����������������������ԭ������(? )
A������������
B��������ͭ
C���������Ʊ�Ư��
D������������������Һ
�ο��𰸣�C
������������ж��ֻ��ϼ�̬���ڴ������Ӧ���Ȼ�õ����ӳ�Ϊ-1�۵��ȵĻ������ʱ����Ϊ������������ijЩ��Ӧ��(��C��)����Ҳ��ʧȥ���ӣ���Ϊ��̬�Ļ������ʱ��������ԭ����
������Cl2��Clԭ�Ӻ���ֻ��3�����Ӳ㣬�������7�����ӣ��ڻ�ѧ��Ӧ�к����õ��ӱ��ֳ�ǿ�����ԡ��仹ԭ��һ��ֻ���绯��Ӧ�����ֳ�����
�����Ѷȣ���
2��ѡ���� Cl2��Br2��I2�����������ԣ���������Cl2>Br2>I2��Cl2�ܰ�����廯�����û������������������ơ���
NaBr��NaI�Ļ��Һ�У�ͨ��һ������������Һ���ɲ�������գ��õ�����ʣ�����ʵ���ɲ�������
[? ]
A��NaCl
B��NaCl? NaBr
C��NaCl? NaBr? NaI?
D��NaCl?NaI
�ο��𰸣�D
���������
�����Ѷȣ���
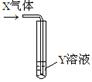
3��ѡ���� ��X����ͨ��Y��Һ�У�ʵ������Ԥ�������һ�µ������
?
| X����
| Y��Һ
| Ԥ�������
| 
|
��
| CO2
| ����Na2CO3��Һ
| ��ɫ��������
|
��
| SO2
| Ba(NO3)2��Һ
| ��ɫ��������
|
��
| Cl2
| AgNO3��Һ
| ��ɫ��������
|
��
| NH3
| AlCl3��Һ
| ��ɫ��������
|
?
A��ֻ�Т٢ڢ�?B��ֻ�Т٢ڢ�? C��ֻ�Т٢ۢ�? D���٢ڢۢ�
�ο��𰸣�D
���������
�������:�ٽ�CO2ͨ�뵽����Na2CO3��Һ�з�����ѧ��Ӧ��CO2+H2O+ Na2CO3=2NaHCO3��NaHCO3��Na2CO3���ܽ��С������г�����������ȷ����SO2��ˮ��Ӧ��������H2SO3����Һ�����ԣ�Ba(NO3)2���Ե����NO3-����������Һ�о���ǿ�����ԣ����SO2��Ba(NO3)2�����ܷ����ĸ��ֽⷴӦ��SO2ͨ�뵽Ba(NO3)2��Һ�пɷ���������ԭ��Ӧ��3SO2+2H2O+2NO3��=3SO42- ʮ4 H++2NO����SO42-+Ba2+=BaSO4��������Cl2+H2O=HCl+HClO��HCl+AgNO3=AgCl��+HNO3����ȷ����NH3 +H2O= NH3��H2O��3NH3��H2O+AlCl3=Al(OH)3��+3NH4Cl����ȷ���ʴ�ΪD��3-�����������¾���ǿ�������Լ�H2SO3���л�ԭ�Ե����ʡ�����
�����Ѷȣ�һ��
4������� ��ͬ±��ԭ�Ӽ����ͨ�����õ��Ӷԣ��γ�±�ػ������ͨʽΪ��XX��n��n
= 1��3��5��7���ҷǽ�����X�䣾X����±�ػ�������Ϊǿ���������ش��������⣺
��1��±�ػ������У��е���͵�Ӧ��?��д����ʽ����ͬ����
��2����n = 7������������ɵ�±�ػ�����ӦΪ?��
��3���ֽ�23.3gBrCln����ˮ����ͨ�����SO2������HBr��HCl��H2SO4�������ᣬȻ����û� ������Һ�м������Ba(NO3)2��Һ���ˣ��������Һ�м����������������Һ�����������77.3g��������n��ֵ(д���������)��
������Һ�м������Ba(NO3)2��Һ���ˣ��������Һ�м����������������Һ�����������77.3g��������n��ֵ(д���������)��
��4��ij±�ػ�������ˮ�ķ�ӦΪ ClFn + H2O �� HClO3 + Cl2 +O2 + HF����ClFn��H2O�����ʵ���֮��Ϊ3��5����n��ֵ(д���������)��
�ο��𰸣���ClF��2�֣�?��IF7��2�֣�?��n = 3��3�֣�
��BrCln�����ʵ���Ϊx��?��
��80+35.5n��x = 23.3
��188+143.5n��x=" 77.3?" ��2�֣�
 ?
?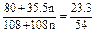 ?n =" 3?" ��1�֣�
?n =" 3?" ��1�֣�
�ȣ�3�֣���ClFn��H2O�����ʵ���֮��Ϊ3��5�ɵ�������ƽ�ķ���ʽ
3ClFn + 5H2O �� ��10��3n��HClO3 +��3n��7���M2Cl2 +��9n��25���M2O2 + 3nHF��1�֣�
������
10��3n��0
��3n��7���M2��0
��9n��25���M2��0?��1�֣�n =" 3?" ��1�֣�
�����ⷨ����������
�����������
�����Ѷȣ�һ��
5��ѡ���� ������ʵ����ͬһԭ�����͵��ǣ�������
A��Cl2��Fe��Cu��Ӧ���ɸ��Ȼ���
B��NH4HCO3���塢����I2���Ⱦ��ܱ������
C��SO2��Cl2����ʹƷ����Һ��ɫ
D��ClO-��Fe2+��H+�����ܴ�������
�ο��𰸣�A����������ǿ�����ԣ��������Ӧ�������̬�Ȼ����A��ȷ��
B��NH4HCO3����ֽ⣬����I2����������ǰ���ǻ�ѧ�仯�������������仯����B����
C��SO2��ʹƷ����Һ��ɫ�����ں���ɫ�л��ﷴӦ������ɫ���ȶ������ʣ�����Cl2��ˮ��Ӧ���ɾ���ǿ�����Ժ�Ư���Ե�HClO����Cl2ʹƷ����Һ��ɫ������Ư��ԭ����һ������C����
D��HClO�Ⱦ��������ԣ��־��������ԣ�ClO-��Fe2+������Fe3+����H+����Ӧ�����������HClO����Ӧԭ����ͬ����D����
��ѡA��
���������
�����Ѷȣ���