微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198KJ・mol-1.
P-O 360kJ・mol-1.氧气分子内氧原子间的键能为498kJ・mol-1则P4+3O2==P4O6的反应热△H为
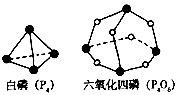
[? ]
A.+1638 kJ・mol-1
B.-1638 kJ・mol-1
C.-126 kJ・mol-1
D.+126 kJ・mol-1
2、选择题 已知在一定条件下,CO的燃烧热为283kJ/mol,CH4的燃烧热为890kJ/mol,由1mol?CO和3mol?CH4组成混合气体在上述条件下充分燃烧,释放的热量为( )
A.2912?kJ
B.2953?kJ
C.3236?kJ
D.3867?kJ
3、填空题 火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol 液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256KJ 的热量。
(1 )液态肼(N2H4)和液态双氧水反应的热化学方程式为? 。
(2 )又已知H2O(l) =H2O(g);ΔH=+44kJ/mol 。则8g 液态肼与液态双氧水反应生成液态水时放出的热量是?kJ 。
(3 )此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是______________ 。
(4 )已知N2(g) + 2O2(g) ==== 2NO2(g);ΔH=+67.7kJ/mol
?N2H4(g) + O2(g) ==== N2(g) + 2H2O(g);ΔH=-534kJ/mol
则肼与NO2完全反应生成氮气和液态水的热化学方程式? 。
4、选择题 白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P a kJ・mol-1、P-O b kJ・mol-1、P===O c kJ・mol-1、O===O d kJ・mol-1。根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是
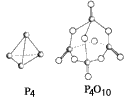
[? ]
A.(6a+5d-4c-12b) kJ・mol-1
B.(4c+12b-6a-5d) kJ・mol-1
C.(4c+12b-4a-5d) kJ・mol-1
D.(4a+5d-4c-12b) kJ・mol-1
5、计算题 在一定条件下,CH4和CH3OH的燃烧的热化学方程式分别为:
CH4(g)+2O2(g)=CO2(g) + 2H2O(g) ΔH=-890kJ/mol
CH3OH(g)+1.5O2(g)=CO2(g) + 2H2O(g) ΔH=-750kJ/mol
如果有CH4和CH3OH的混合气体充分燃烧,放出的热量为806kJ,将生成的气体通过浓硫酸,浓硫酸增重36g。则混合气体中CH4和CH3OH的体积比________。?