��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����������ȼ��
�ο��𰸣�2Fe+ 3Cl2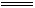 2FeCl3
2FeCl3
�����������������ǿ�����ԣ��ɽ�������Ϊ�۵��Ȼ�����2Fe+ 3Cl2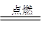 2FeCl3
2FeCl3
�����Ѷȣ���
2��ʵ���� ��ҵ�ϳ�ͨ�����·ֽ�FeSO4�ķ����Ʊ�Fe2O3���仯ѧ����ʽΪ��
2FeSO4 ="===" Fe2O3 +SO2��+SO3��?Ϊ����FeSO4���·ֽ�IJ����������ʵ�飺
��ȡ����FeSO4���·ֽ�õ��Ĺ��壬��һ����ϡ�����ܽ⣬�����Һ�м���������KSCN��Һ���۲���Һ��ɫ�ı仯�Լ���Fe3+�Ƿ���ڡ�
�ڽ�FeSO4���·ֽ����������ͨ����ͼ��ʾ��װ���У��Լ���������������Ƿ���SO2��SO3����ش��������⣺

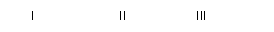
��1��д����KSCN����Fe3+�����ӷ���ʽ?��
��2��װ��I���Լ�Ϊ�Ȼ�����Һ�����в�����ʱ�Ȼ�����Һ���а�ɫ������������ͬѧ˵�������ɫ����������BaSO4��BaSO3�Ļ�����ͬѧ˵�������ɫ������BaSO4����ͬѧ˵�������ɫ������BaSO3���������һ����ʵ������Ǽ��Լ���
?
����Ϊ������һλͬѧ�Ĺ۵���ȷ��?
��3��װ��II���Լ�ΪƷ����Һ����������?��Ʒ����Һ�пɹ۲쵽������?��
��4��װ��III���Լ�ΪNaOH��Һ����Ŀ����?��
�ο��𰸣���1��Fe3++3SCN-=Fe��SCN��3
?(2)ȡ���а�ɫ��������������ϡ���ᣬ���������ܽ��������ݲ����������ΪBaSO4
��
��3����������������к�SO2��Ʒ����Һ��ɫ
��4����ȥ�����SO2����ֹ��Ⱦ������
�����������
�����Ѷȣ�һ��
3��ѡ���� FeS2�ṹ������Na2O2�����ᷴӦʱ����H2S2��H2S2������H2O2���ֽ⡣ʵ������ϡ������ȡH2Sʱ��ijѧ����FeS2��������FeSʹ�ã���FeS2��Ӧ����������ɵ������ǣ�(? )
A��H2S
B��S
C��FeS
D��FeCl2
�ο��𰸣�C
���������FeS2���ᷴӦʱ����H2S2��H2S2������H2O2���ֽ⣬���Է�Ӧ�е����������Ȼ�����������S��H2S��������������FeS����ѡC��2������
��������������Ϣ�����⣬�����е��Ѷȵ����⣬��Ҫ������������ѧ������ѧ��������˼ά�������Լ�֪ʶ��Ǩ�����������ѧ��������û���֪ʶ�����ʵ�������������
�����Ѷȣ���
4������� ��ѧ��ȤС��Ϊ̽��ij����ʯ����Ҫ�ɷ�ΪFe203��Si02�������ʣ���������ʵ�飺
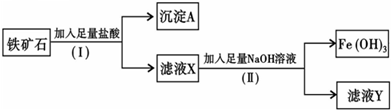
��1�����裨I���з�����Һ�ͳ����IJ���������______��
��2������A��һ������______������������______������ԡ����ԡ��������
��3������ҺY�м���KSCN��Һ����Һ��______�����ɫ����ɫ������
��4��д�����裨��������Fe��OH��3�����ӷ���ʽ______��
�ο��𰸣���1������ʯ����Ҫ�ɷ�ΪFe203��Si02��������������������������ᷴӦ�����Ȼ�����ˮ����������Ϊ�������Ҳ������ᷴӦ������ͨ�����˵ķ������룬
�ʴ�Ϊ�����ˣ�
��2���������費�����ᷴӦ�����Թ��˺�õ��ij���AΪSiO2�����������ܹ���ǿ����Һ��Ӧ�����κ�ˮ�����Զ��������������������
�ʴ�Ϊ��SiO2�����������
��3����Һ�к��������ӣ��������ܹ�����������ӷ�Ӧ���ɺ�ɫ�����軯����
�ʴ�Ϊ����ɫ��
��4�������Ϊ������������������Һ��Ӧ��������������������Ӧ�����ӷ���ʽΪ��Fe3++3OH-�TFe��OH��3����
�ʴ�Ϊ��Fe3++3OH-�TFe��OH��3����
���������
�����Ѷȣ�һ��
5������� ��һ����ͭ�����ǻ�ѧ�е���Ҫ�Լ���������������������ͭ����Һ��֤�����ǵĻ�ԭ�ԡ�
����������ͭ����Һ��������Ӧ�ã�
��1��ʵ������ȡ����������ͭ����Һ�IJ������������Թ������10%��________��Һ2mL������2%��_________��Һ4~6�Σ�����ѡ�����ͭ�����������ơ��������ɡ�����������Ŀ��_______________________________________________��
��2�����и������ʵ���Һ�������Ƶ�������ͭ����Һ����Ҫʱ���Լ��ȣ����ܼ����������______��
A��HCOOCH3��C6H5COOH��C6H5CH2OH
B��NaHSO4��BaCl2��Na2CO3����̪
C��HCOOH��HCOONa��HCOOCH2CH3
D�������ǣ�CH2OHCHOHCH2OH