| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《物质的量》高频试题预测(2017年最新版)(十)
参考答案:B 本题解析:A、原子数为3NA;B、正确;C、非标况下,11.2L不一定为0.5mol;D、钠离子数为0.1NA。 本题难度:一般 2、选择题 将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3 mol・L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是 |
参考答案:C
本题解析:镁、铜在稀硝酸中反应,是方程式是类似的,都是放出NO,而不会是产生H2。加碱后,最终都生成二价氢氧化物沉淀,沉淀质量比合金质量增加的就是氢氧根,5.1克是0.3mol,也就是原来金属合计有0.15mol,全部是铜的话,最大质量为9.6克;根据方程式计算,释放的NO有0.1mol,标况是2.24升;消耗的氢氧化钠有0.3mol,100毫升;参加反应的硝酸有0.4mol。若全部是镁,则质量为3.6g,释放的NO还是有0.1mol,标况是2.24升;消耗的氢氧化钠有0.3mol,100毫升;参加反应的硝酸有0.4mol。所以正确的只有C选项。
考点:金属与稀硝酸的反应
点评:本题不论金属是镁还是铜,消耗的硝酸,生成的一氧化氮的量是相同的。
本题难度:一般
3、选择题 配制100mL 1.0 mol/L Na2CO3溶液,下列操作正确的是?
[? ]
参考答案:D
本题解析:
本题难度:简单
4、选择题 设NA为阿伏加德罗常数,下列叙述正确的是
A.2.4g Mg与足量的二氧化碳完全反应失去的电子数为0.2NA
B.22.4 L氯气与过量的铁完全反应,转移电子数为2 NA
C.含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2
参考答案:
本题解析:
本题难度:一般
5、选择题 哥本哈根气候大会的中心议题是“节能减排”,美国二氧化碳排放量居世界之首,人均年排放CO2约20吨,20吨CO2在标准状况下的体积为
A.2×107L
B. L
L
C.2×107×22.4 L
D. ×22.4 L
×22.4 L
参考答案:D
本题解析:以“节能减排”为知识背景,实际是以物质的量为中心的计算。先求20吨二氧化碳的物质的量: ,再求标准状况下的体积:
,再求标准状况下的体积: ,故选D
,故选D
点评:物质的量为中心的计算中,要熟练掌握这些公式: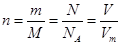 。试题基础、简单。
。试题基础、简单。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《氧化还原反.. | |