��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��14�֣�ij�о�С�������������о���

��1�������ϳ�ʱ���ͬѧ�۲쵽�������ǣ���ͼ�е������������������?������ĸ�����������Ҫ�ɷ���?
��2������ʵ�������жϣ�����������ʴ�����У������ĵ缫��ӦΪ?
��3����������ⲿ������??���ڴ������£���������������ʴת��ΪFe��OH��2�ĵ�ط�Ӧ����ʽΪ?
��4����Ϊ�˷�ֹ�������⣬��С��ͬѧ���������������һ��������ý��������?
A. ��? B. ͭ? C. п?
��5����������ʴ����ҵ�����г���Ը������С�����������������Ч�������������ĸ�ʴ����ν���������������ڸ�������Ƚ�������������ʹ������γ�һ�����ܵ�����ɫ����Ĥ�������������̿ɱ�ʾ���£�

�ٲ�����ó���Һ��15%��������Һ������������Ŀ�����ڳ�ȥ����������⣬�ò���Ӧ�����ӷ���ʽΪ___________________________________��
��Ϊ���龭������������������Ƿ�ϸ�����Ʒ�������5%������ͭ��Һ�������Ʒ���ϸ�����������С�ɿף�δ�γ����ܵ�����Ĥ����һ��ʱ�佫�۲쵽������Ϊ__________________________��
�۳����������ڷ���Һ��NaNO2��NaNO3��NaOH��ɵĻ��Һ���н��ݣ�����IV���������˸��ӵĻ�ѧ��Ӧ��
��Ӧһ��____Fe ��____NaNO2 ��___NaOH ��____Na2FeO2 ��____H2O ��___NH3��
��Ӧ����8Fe��3NaNO3 �� 5NaOH �� 2H2O �� 4Na2Fe2O4 �� 3 NH3��
��Ӧ����Na2FeO2 �� Na2Fe2O4 �� 2H2O �� Fe3O4 �� 4NaOH
��ƽ����Ӧһ���Ļ�ѧ����ʽ����ϵ��ֱ�����ں����ϣ�����Ҫѭ��ʹ�÷���Һ�������۽Ƕȷ�������Ҫ��ʹ�ù��ķ���Һ��_________
A. ֻ�����NaNO2? B. ֻ�����NaNO2��NaNO3
C. ��Ҫ����NaNO2��NaNO3��NaOH? D. ��������κ����ʶ�ֱ��ʹ��
�ο��𰸣���14�֣���1��A��? Fe2O3���� Fe2O3�� xH2O��
��2��O2��2 H2O��4e���� 4 OH��
��3����ʪ�Ŀ�������������ˮ����? 2Fe ��O2 ��2 H2O��2 Fe(OH)2
��4��C?��5���� Fe2O3��6 H����2 Fe3����3 H2O
������Ʒ�����к�ɫ���������� 3��1��5��3��1��1��B
�����������1��B��C�����ܸ�����������ֹ�������绯ѧ��ʴ����A���ܣ����������ױ���ʴ����A���������Ҫ�ɷ���Fe2O3���� Fe2O3�� xH2O����
��2�������ĵ绯ѧ��ʴ�У�����������������Һ�����Ժ��������������������õ����ӣ�����ӦʽΪO2��2 H2O��4e���� 4 OH����
��3����Ҫ��ʴ�绯ѧ��ʴ������봦�ڳ�ʪ�Ŀ�������������ˮ������Ӧ���ܷ�Ӧʽ��2Fe ��O2 ��2 H2O��2 Fe(OH)2.
(4)���ڶƲ�һ������֮������ʴ�绯ѧ��ʴ���������ƽ����Ա���ǿ�Ľ��������Դ�ѡC��
��5�����������Ҫ�ɷ�������������ϡ���ᷴӦ�ķ���ʽΪFe2O3��6 H����2 Fe3����3 H2O��
����Ϊ���Ļ�����ǿ��ͭ�����ܺ�����ͭ��Ӧ�û���ͭ����������Ʒ�����к�ɫ����������
���ڷ�Ӧ����ʧȥ��������ԭ�������ϼ۴�0�����ߵ���2�ۡ����������������ƣ���Ԫ�صĻ��ϼ۴ӣ�3�۽��͵���3�ۣ��仯6����λ�����������ͻ�ԭ�������ʵ���֮����1�U3�ģ����Է���ʽΪ3Fe ��NaNO2 ��5NaOH��3Na2FeO2 ��H2O ��NH3������3����Ӧ�ϲ����õ�12Fe��NaNO3��4NaNO2��10H2O=4Fe3O4��5NH3����5NaOH����˵����Ӧ�����ĵ��������ƺ��������ƣ�������Ҫ������ߣ���ѡB��
�����Ѷȣ�һ��
2��ʵ���� ��13�֣�ʵ������ȼ�Ϸ��ⶨij�ְ����ᣨCxHyOzNp���ķ���ʽ��ɣ�ȡWg���ְ�������ڴ����г��ȼ�գ�����CO2��H2O��N2��������ͼ��ʾװ���ý���ʵ�飨����̨�����С��ƾ��Ƶ�δ����������ش��й����⣺
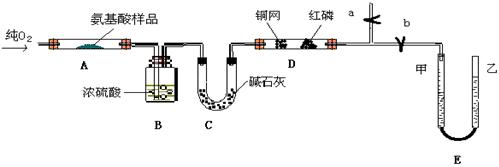
��1��ʵ�鿪ʼʱ�����ȴ�ֹˮ��a���ر�ֹˮ��b��ͨ��һ��ʱ�����������������
Ŀ����?��֮��ر�ֹˮ��a��
��2����װ��B��C�ɷֱ�ȷ�����ⰱ�����к��е�?��?������
��3��Eװ�õ������Dz���?����������ɴ�ȷ�����ⰱ�����к��е�?
��������Ϊ�˽�ȷ�ز����������������ڶ���Ӧǰ�����Һ��Ķ��������ֵ
�Ĺ����У�Ӧע��?������ţ���
a�������밼Һ����ʹ���ƽ? b���ȴ�Ƭ�̣����ҹ���Һ�治������ʱ�����̶���
c������ʱӦ�����ƶ��ҹܣ�ʹ�ס�������Һ����ƽ
d������ʱ��һ��ʹ�ס�������Һ����ƽ
��4��ʵ���вⶨ����һ���ݿ��ܲ�ȷ??
��������?
��5���ϸ��˵������������ֻ��ȷ���������?��
��Ҫȷ���˰�����ķ���ʽ����Ҫ�ⶨ�ð������?��
�ο��𰸣�

�����������
�����Ѷȣ�һ��
3��ʵ���� ��̬������A�����ֶ�����Ԫ����ɣ�����ˮ�������ֽⷴӦ������ͬѧ����ͼװ��(�г�װ����)�������̽��ʵ�顣

(1)����B��������________��
(2)ʵ���У����е���ֽ���������к�ɫ��ĩ��Ϊ��ɫ����M���ɣ�����е��Լ�Ϊ________�����з�����Ӧ�Ļ�ѧ����ʽΪ________��V�е��Լ�Ϊ________��
(3)����ͬѧ����ͬ��ʵ�飬��װ������˳��Ϊ��?��?��?��?V?������ʱ��������Ϊ________��ԭ����________��
(4)��������Ӧ��2.5 g������A�����Ͽ��Ƶ�0.56 L(��״��)M����A�Ļ�ѧʽΪ________��
�ο��𰸣�(1)��Һ©����(2)��ʯ�ң�3CuO��2NH3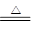 3Cu��N2��3H2O��ŨH2SO4��(3)��ֽ����������ͭ�백����Ӧ���ɵ�ˮ��δ��Ӧ�İ����γɰ�ˮ��ʹ��ɫʯ����ֽ����
3Cu��N2��3H2O��ŨH2SO4��(3)��ֽ����������ͭ�백����Ӧ���ɵ�ˮ��δ��Ӧ�İ����γɰ�ˮ��ʹ��ɫʯ����ֽ����
(4)Mg3N2
���������(1)���л�����©���Ƿ�Һ©����(2)����ʵ������ͼ��֪���ú�ɫʯ����ֽ������ǰ�����������һ�ּ������壬�ü�ʯ�Ҹ��ﰱ�����������л�ԭ�ԣ��ɽ���ɫ��CuO��ԭΪ��ɫ��Cu������������ΪN2��β���еİ�����Ũ�������գ����N2����ˮ���ռ���(3)����ͭ�백����Ӧ���ɵ�ˮ��δ��Ӧ�İ����γɰ�ˮ��ʹ��ɫʯ����ֽ������
(4)0.56 L M��N2�����ʵ���Ϊ0.025 mol������A��N������Ϊ0.7 g������һ��Ԫ�ص�����Ϊ1.8 g��������A��δ֪Ԫ�صĻ��ϼ����ۿɵã�ֻ���ǣ�2�۵�Mg���ʸ�������Mg3N2��
�����Ѷȣ�һ��
4��ʵ���� ij�о���ѧϰС�齫һ��Ũ�ȵ�Na2CO3��Һ����CuSO4��Һ�еõ���ɫ��������ͬѧ��Ϊ���߷�Ӧֻ����CuCO3һ�ֳ�������ͬѧ��Ϊ��������ٽ�ˮ�⣬ֻ����Cu(OH)2һ�ֳ�������ͬѧ��Ϊ������
CuCO3��Cu(OH)2���ֳ���������������֪��CuCO3��Cu(OH)2�������ᾧˮ��
��1��������ͬѧ�����⣬�����ɵij����м���________�Լ������۲쵽________ʱ����˵����ͬѧ�IJ�����ȷ����Na2CO3��Һ��CuSO4��Һ��Ӧ�����ӷ���ʽΪ��_______________________��
��2������̽��������ijɷֽ�����ͨ��_______��ϴ�ӵIJ�������Һ�з���������ٵ��¸��Ȼ��������������ɷ֡�
��3����������CuCO3��Cu(OH)2���߶��У���ͨ��������ʾװ�õ����ӣ����ж����������ⶨ����������ÿһװ���еķ�Ӧ�����վ���ȫ����Ӧǰϵͳ�д��ڵĿ������Բ��ƣ���

��������װ������˳��Ϊ_____��_____��_____��_____��_____��
��ʵ�����ʱҪͨ������Ŀ�������������____________________��
����������Ʒ������Ϊm�ˣ�CO2����װ������������n�ˣ��������Cu(OH)2����������Ϊ��_____��
����֤����ͬѧ˵����ȷ��ʵ��������____________________��
�ο��𰸣���1��ϡ���������������𰸺������ɣ���Cu2++CO32-+H2O= Cu(OH)2��+CO2��
��2������
��3����C �� A �� B �� D �� E ���� C �� A �� B �� E �� D ����
���ų�װ����������H2O��CO2���壬�Ա���ȫ���գ�
��1-(31n/11m)
��װ��B���������ӣ��䣩
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʵ���ܻ�óɹ�����
A������ˮ���𱽡��Ҵ�����ϩ�����Ȼ�̼
B����Ũ��ˮ������˳�ȥ������������
C��������ˮ�����ۻ���Ƴ��屽
D�����÷�Һ©������������ͼױ�
�ο��𰸣�A
����������������Ȼ�̼����ˮ������ȡ���л���ֱ����ϲ���²㡣�Ҵ�����ˮ���ܣ���ϩ����ˮ�����ӳɷ�Ӧ��A���Լ���B�����ɵ����屽���ܹ��ܽ��ڱ��У����ܳ�ȥ��B����C����ȷ��Ӧ����Һ�壻������ͼױ����ܣ�����ֱ�ӷ�Һ��D����ȷ����ѡA��
�������������л��е����ʳ�ȥ����ô�������ᴿ���������һ��IJ�ͬ���ʱ˴˷ֿ����õ���Ӧ��ֵĸ�������з��롣�ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ��
�����Ѷȣ���