微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在H2SO3+2H2S=3H2O+3S反应中,被氧化与被还原元素的质量比为
A.1:1
B.2:1
C.1:2
D.3:2
参考答案:B
本题解析:分析:H2SO3+2H2S=3H2O+3S中,S元素的化合价由+4价降低为0,由-2价升高为0,化合价升高被氧化,化合价降低被还原,以此来解答.
解答:H2SO3+2H2S=3H2O+3S中,S元素的化合价由+4价降低为0,.化合价降低被还原,H2SO3中S元素被还原;
由-2价升高为0,化合价升高被氧化,H2S中S元素被氧化,
由反应方程式可知,被氧化与被还原的S元素的原子个数比为2:1,
则被氧化与被还原元素的质量比为2:1,
故选B.
点评:本题考查氧化还原反应,明确氧化还原反应中元素的化合价变化及基本概念即可解答,题目难度不大.
本题难度:困难
2、选择题 下列物质只含有非极性键的是(?)
A.H2O
B.HCl
C.NaOH
D.O2
参考答案:D
本题解析:同种原子之间的共价键为非极性共价键,H2O 中是两个极性H―O键,故答案为D
本题难度:一般
3、填空题 (10分)2SO2(g)+ O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH =" -" 99 kJ・mol-1
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH =" -" 99 kJ・mol-1
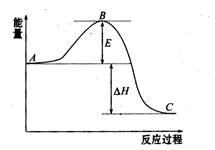
请回答下列问题:
(1)图中A表示_____________________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________。
(2)图中ΔH =" __________" kJ・mol-1。
(3)如果反应速率v(SO2)为0.06 mol・L-1・min-1,则v(O2)为__________ mol・L-1・min-1。
(4)已知S(s) + O2(g) = SO2(g) ΔH =" -" 296 kJ・mol-1,则由S(s)生成5 mol SO3(g)的ΔH= kJ・mol-1。
参考答案:(1)反应物能量 降低 (2)-198(3)0.03 (4)- 1975
本题解析:图中A表示反应物总能量,E表示该反应的活化能,加入催化剂会降低反应的活化能,故加入V2O5会使图中B点降低;图中ΔH为反应的反应热,为-198kJ/mol;根据同一反应不同物质表示该反应的反应速率,速率之比等于化学计量数之比,故v(SO2)为0.06 mol・L-1・min-1,则v(O2)为0.03 mol・L-1・min-1;根据盖斯定律:由S(s)生成5 mol SO3(g)的ΔH=5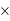 - 296 kJ・mol-1+5
- 296 kJ・mol-1+5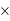 - 99 kJ・mol-1="-" 1975kJ・mol-1。
- 99 kJ・mol-1="-" 1975kJ・mol-1。
考点:化学反应原理。
本题难度:一般
4、选择题 下列氧化还原反应中氧化产物和还原产物不相同的是
A.CO2+C?2CO
B.Cl2+2NaOH=NaCl+NaClO+H2O
C.KClO3+6HCl=KCl+3Cl2↑+3H2O
D.SO2+2H2S=3S+2H2O
参考答案:B
本题解析:分析:氧化产物和还原产物如相同,应是含有相同元素的物质之间发生氧化还原反应,以此解答该题.
解答:A.只有C元素的化合价发生变化,CO既是氧化产物又是还原产物,故A不选;
B.只有Cl元素的化合价发生变化,氧化产物为NaClO,还原产物为NaCl,不相同,故B选;
C.只有Cl元素的化合价发生变化,Cl2既是氧化产物又是还原产物,故C不选;
D.只有S元素的化合价发生变化,S既是氧化产物又是还原产物,故D不选.
故选B.
点评:本题考查氧化还原反应,为高考常见题型,注意把握元素化合价的变化,为解答该题的关键,题目难道不大.
本题难度:一般
5、选择题 25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量。下列表示该反应的热化学方程式中正确的是
A.CH4O(l)+3/2O2(g) == CO2(g)+2H2O(l) △H==-725.8kJ/mol
B.2CH4O(l)+3O2(g)== 2CO2(g)+4H2O(l) △H==+1451.6kJ/mol
C.2CH4O+O2 == 2CO2+4H2O(l) △H==-22.68kJ/mol
D.CH4O(l)+3/2O2(g) == CO2(g)+2H2O(g) △H==-725.8kJ/mol
参考答案:A
本题解析:甲醇燃烧是放热反应,△H<0,B不正确;C中没有注明物质的状态,不正确;D中水的状态不是液态,不正确,因此正确的答案选A。
考点:考查热化学方程式的正误判断
点评:书写和应用热化学方程式时必须注意以下几点:①明确写出反应的计量方程式,各物质化学式前的化学计量系数可以是整数,也可以是分数。②各物质化学式右侧用圆括弧表明物质的聚集状态。③反应热与反应方程式相互对应。若反应式的书写形式不同,则相应的化学计量系数不同,故反应热亦不同。
本题难度:一般