微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (18分)如图装置中,A、B两池溶液的体积均为200mL,
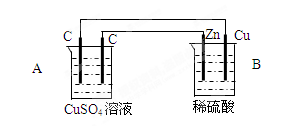
⑴判断装置的名称:A池为??B池为?
⑵A池中左边石墨棒为?极,电极反应式为??
A池中电池总反应式??
(3)若工作一段时间后,B池中Cu棒上析出224ml气体(标准状态),则电路中通过
了?mol电子,B池中溶液质量?(填“增加”、“不变”或“减少”)??g,若反应前后溶液的体积不变,反应后A池溶液的pH为?
参考答案:(1)电解池,原电池
(2)阳,4OH--4e-=2H2O+O2↑? 2H2O+2CuSO4 2Cu+O2↑+2H2SO4?
2Cu+O2↑+2H2SO4?
(3)0.02,?增加,? 0.63,? 1?(每空2分)
本题解析:(1)锌能和稀硫酸反应,所以根据装置可知,A是电解池,B是原电池。
(2)锌比铜活泼,所以锌是负极,铜是正极,则A池中左边石墨棒为阳极,溶液中的OH-放电,方程式为4OH--4e-=2H2O+O2↑。惰性电极电解硫酸铜溶液的方程式为2H2O+2CuSO4 2Cu+O2↑+2H2SO4。
2Cu+O2↑+2H2SO4。
(3)B池中Cu棒上析出的气体是氢气,物质的量是0.01mol,所以转移电子是0.02mol。B中的总反应式为Zn+2H+=Zn2++H2↑,所以B池中溶液质量增加0.65g-0.02g=0.63g。根据电子得失守恒可知,A中产生的氢离子是0.02mol,其浓度是0.02mol÷0.2L=0.1mool/L,所以pH=1。
本题难度:一般
2、填空题 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。
已知:① X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;② Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。?
请回答:
(1)Z2Y的化学式是?。?
(2)Z2Y2与X2Y反应的化学方程式是?。
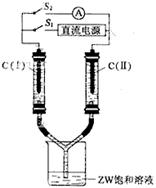
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。?一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:
C(I)的电极名称是?(填写正极或负极);
C(II)的电极反应式是??。
(4)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是?。
参考答案:(1)Na2O? (2)2Na2O2+2H2O=4NaOH+O2↑ (3)负极,Cl2+2e-=2Cl-?(4)Cu + H2O2 + 2H+= Cu2++2H2O
本题解析:中学阶段A2B2型的化合物主要指Na2O2和 H2O2,共价化合物是H2O2,离子化合物是Na2O2,所以根据X、Y、Z、W的原子序数大小顺序课判断X是H,Y是O,Z是Na,W是Cl。
(1)Z2Y的化学式是Na2O。?
(2)Z2Y2与X2Y反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑。
(3)根据装置图可知,接通S1后该装置是电解池,即相当于是惰性电极电解饱和氯化钠溶液。C(Ⅰ)附近溶液变红,说明该电极是阴极,生成的气体是氢气,另外一电极生成的是氯气。断开S1,接通S2,电流表的指针发生偏转,说明此时形成原电池,其中氢气所在的电极是负极,即C(I)的电极名称是负极。C(II)的电极是正极,氯气得到电子,电极反应式是Cl2+2e-=2Cl- 。
(4)双氧水具有氧化性,钠氧化单质铜,则反应的离子方程式是Cu + H2O2 + 2H+= Cu2++2H2O。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,主要是考查学生对常见化合物以及电化学原理的熟悉了解程度,有利于调动学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是记住常见的化合物,明确原电池和电解池的工作原理,然后结合题意灵活运用即可。
本题难度:一般
3、选择题 镀锌铁在发生析氢腐蚀时,若有0.2 mol电子发生转移,下列说法正确的是
①有5.6 g金属被腐蚀?②有6.5 g金属被腐蚀?③在标准状况下有2.24 L气体放出?④在标准状况下有1.12 L气体放出
A.①②
B.②③
C.①④
D.③④
参考答案:B
本题解析 :试题分析:镀锌铁发生电化学腐蚀,锌作负极:Zn-2e- Zn2+,有0.2 mol电子转移,有0.1 mol Zn溶解;在正极上:2H++2e-
Zn2+,有0.2 mol电子转移,有0.1 mol Zn溶解;在正极上:2H++2e- H2↑,生成0.1 mol H2,所以正确的答案选B。
H2↑,生成0.1 mol H2,所以正确的答案选B。
考点:考查金属腐蚀的有关判断、计算
点评:该题是中等难度的试题,试题注重基础,侧重考查学生分析问题、解决问题的能力,有助于培养学生的逻辑思维能力和创新思维能力。该题难度不大,学生不难得分。
本题难度:简单
4、选择题 一定条件下,碳钢腐蚀与溶液pH的关系如下:
pH
| 2
| 4
| 6
| 6.5
| 8
| 13.5
| 14
|
腐蚀快慢
| 较快
| 慢
| 较快
|
主要产物
| Fe2+
| Fe3O4
| Fe2O3
| FeO2-
|
?
下列说法不正确的是(?)
A.在pH<4溶液中,碳钢主要发生析氢腐蚀
B.在pH>6溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e-=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
参考答案:C
本题解析:A项,酸性较强条件下,碳钢主要发生析氢腐蚀,正确;B项,在pH>6的溶液中,酸性较弱,主要发生吸氧腐蚀,正确;C项,碳钢腐蚀的正极反应为O2+2H2O+4e-=4OH-,错误;D项,除O2后,腐蚀速率减缓,正确。
本题难度:一般
5、选择题 下列叙述不正确的是
[? ]
A.钢铁在干燥的空气中不易被腐蚀
B.可以用船尾连锌块的方法来保护船身
C.金属的电化学腐蚀比化学腐蚀更普遍
D.用铝质铆钉铆接铁板,铁板易被腐蚀
参考答案:D
本题解析:
本题难度:简单