��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ��NO2��g��+CO��g��

CO2��g��+NO��g����Ӧ���������仯ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ��������ͼ�������й�˵����ȷ���ǣ�������

A���÷�Ӧ���ʱ��H=+234kJ/mol
B����X��ʾ��Ӧʱ�䣬��Y��ʾ�Ŀ����ǻ��������ܶ�
C����X��ʾ�¶ȣ���Y��ʾ�Ŀ�����CO2�����ʵ���Ũ��
D����X��ʾCO����ʼŨ�ȣ���Y��ʾ�Ŀ�����NO2��ת����
�ο��𰸣��������仯ͼ��֪����Ӧ�������ߣ������������ͣ����Ը÷�ӦΪ���ȷ�Ӧ����HΪ��-������A����
B����Ӧ������������䣬���ݦ�=mv��֪���Ѳ��䣬������ͼ��B����
C������ƽ���ƶ�ԭ���������¶�ƽ�������ȷ����ƶ��������淴Ӧ�����ƶ�������CO2�����ʵ���Ũ�Ƚ��ͣ���C��ȷ��
D������ƽ���ƶ�ԭ��������CO��Ũ�ȣ������NO2��ת���ʣ�ͼʾת���ʽ��ͣ���D����
��ѡC��
���������
�����Ѷȣ���
2��ѡ���� ����˵������ȷ����
A����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ��
B�����ȷ�Ӧ�ڳ�����һ������������
C����Ӧ�Ƿ��Ȼ����ȣ����뿴��Ӧ��������������е�����������Դ�С��
D�������м���Խ�����������Խ�ߣ�����Խ�ȶ�
�ο��𰸣�C
�����������Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ����Ҫ�뷴Ӧ�������������������Դ�С�й�ϵ�����뷴Ӧ��������ϵ�ģ�AB����ȷ��C��ȷ�����ܴ�С�ͷ��ӵ������ߵ���ϵ��D����ȷ����ѡC��
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��飬���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������������ѧ�������������������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷӰ�췴Ӧ�ȴ�С�����أ�Ȼ��������ü��ɡ�
�����Ѷȣ���
3��ѡ���� ���б仯�������ȷ�Ӧ����
�ٸɱ����� �ڽ��������ȱ�ɰ�ɫ��ĩ ��Ũ����ϡ�� ������طֽ�������
����ʯ�Ҹ�ˮ��Ӧ������ʯ��
A���٢�
B���ڢ�
C���٢ܢ�
D���ڢ�
�ο��𰸣�D
����������٢ۢ��еı仯��Ӧ���Ƿ��ȷ�Ӧ���ʴ�����ѡD��
���������⿼����ǻ�ѧ��Ӧ�������仯�����֪ʶ����Ŀ�ѶȲ�����dz�����Ӧ�������仯�ǽ���Ĺؼ���
�����Ѷȣ���
4������� ����P��s����Cl2������Ӧ����PCl3��PCl5����Ӧ���̺�������ϵ��ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ�
��ͼ�ش���������
��1��P��Cl2��Ӧ����PCl3���Ȼ�ѧ����ʽ______��
��2��PCl5�ֽ�����PCl3��Cl2���Ȼ�ѧ����ʽ______��
�����ֽⷴ��һ�����淴Ӧ���¶�T1ʱ�����ܱ������м���0.8mol?PCl5����Ӧ�ﵽƽ��ʱ��ʣ��0.6mol?PCl5����ֽ��ʦ�1����______������Ӧ�¶���T1���ߵ�T2��ƽ��ʱPCl5�ֽ��ʦ�2����2______��1������ڡ�����С�ڡ����ڡ�����
��3����ҵ���Ʊ�PCl5ͨ�����������У��Ƚ�P��Cl2��Ӧ�����м����PCl3��Ȼ���£��ٺ�Cl2��Ӧ����PCl5��ԭ����______��
��4��P��Cl2��������Ӧ����1mol?PCl5�ġ�H3=______��P��Cl2һ����Ӧ����1mol?PCl5�ġ�H4______��H3������ڡ�����С�ڡ����ڡ�����ԭ����______��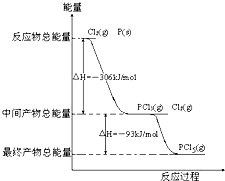
�ο��𰸣���1���Ȼ�ѧ����ʽ��дҪ��ע�������ʵľۼ�״̬���жϷ��ȷ�Ӧ�������ȷ�Ӧ����Ӧ������ʵ����뷴Ӧ�ȳɶ�Ӧ�ı�����ϵ������ͼʾP��s��+Cl2��g����PCl3��g������Ӧ�����������������������������÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ��Ϊ��H=-306 kJ/mol���Ȼ�ѧ����ʽΪP��s��+32Cl2��g���TPCl3��g������H=-306 kJ/mol��
��2P��s��+3Cl2��g��=2PCl3��g����H=-612kJ/mol���ʴ�Ϊ��2P��s��+3Cl2��g��=2PCl3��g����H=-612kJ/mol��?
��2����H=������������-��Ӧ����������Cl2��g��+PCl3��g��=PCl5��g�����м������������������ղ�������������÷�Ӧ�Ƿ��ȷ�Ӧ������ PCl5��g��=PCl3��g��+Cl2��g�������ȷ�Ӧ���Ȼ�ѧ����ʽΪPCl5��g��=PCl3��g��+Cl2��g����H=+93 kJ/mol��PCl5�ֽ��ʦ�1=0.8-0.60.8��100%=25%��PCl5��g��=PCl3��g��+Cl2��g�������ȷ�Ӧ�������¶������ȷ�Ӧ�����ƶ�������Ӧ���ֽⷴӦ�����ȷ�Ӧ�������ȷ�Ӧ�������¶�������Ӧ�����ƶ���ת��������
�ʴ�Ϊ��PCl5��g���TPCl3��g��+Cl2��g����H=+93kJ?mol-1��25%�����ڣ�?
��3��Cl2��g��+PCl3��g��=PCl5��g�����Ƿ��ȷ�Ӧ������ƽ������ȷ�Ӧ�����ƶ�������������PCl5��g�������ɣ�
�ʴ�Ϊ����ΪPCl5�ֽⷴӦ�����ȷ�Ӧ���¶�̫�ߣ�������PCl5�����ɣ�
��4�����ݸ�˹���ɣ�P��Cl2��������Ӧ��һ����Ӧ����PCl5�ġ�HӦ������ȵģ�P��Cl2��������Ӧ����1 molPCl5���Ȼ�ѧ����ʽ��
2P��s��+3Cl2��g��=PCl3��g������H1=-612 kJ/mol��
Cl2��g��+PCl3��g��=PCl5��g������H2=-93 kJ/mol��
P��Cl2һ����Ӧ����1molPCl5�ġ�H3=-306 kJ/mol+��-93 kJ/mol��=-399 kJ/mol�����ݸ�˹���ɣ���ѧ��Ӧ������һ����ɣ����Ƿֲ���ɣ���ѧ��Ӧ���ʱ���һ���ģ�
�ʴ�Ϊ��-399kJ/mol�����ڣ����ݸ�˹���ɿ�֪�����һ����ѧ��Ӧ���Էֲ����У�����ֲ���Ӧ�ķ�Ӧ��֮����÷�Ӧһ�����ʱ�ķ�Ӧ������ͬ�ģ�
���������
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ������������������ڷ�Ӧ���������ķ�������ԭ��Ӧ��
A�����ȷ�Ӧ
B���Ȼ�����Һ��ˮ��
C���������ƺ����ᷴӦ
D����̿�ڸ�������ˮ������Ӧ
�ο��𰸣�B
�������������������������ڷ�Ӧ����������˵����Ӧ�����ȷ�Ӧ��A�����ȷ�Ӧ�Ƿ��ȷ�Ӧ��Ҳ��������ԭ��Ӧ��A����ȷ��B���Ȼ�����ˮ�������ȷ�Ӧ���Ҳ���������ԭ��Ӧ��B��ȷ��C��������Ӧ�Ƿ�������ԭ��Ӧ�������ڷ��ȷ�Ӧ��C����ȷ��D����̿�ڸ�������ˮ������Ӧ����������CO�������ȷ�Ӧ��������������ԭ��Ӧ��D����ȷ����ѡB��
�����Ѷȣ�һ��