��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij��ѧ��ȤС��Ϊ̽���绯ѧԭ�����������ͼװ�ã�����ͭΪ�缫���ձ���ʢװ����ͭ��Һ����������������ȷ����

A��a��b������ʱ����Ƭ�ϻ��н���ͭ����
B��a��b�õ�������ʱ����Ƭ�Ϸ����ķ�ӦΪ��Fe-3e- = Fe3+
C������a��b�Ƿ����ӣ���Ƭ�����ܽ⣬��Һ����ɫ���dz��ɫ
D��a��b�ֱ�����ֱ����Դ����������Cu2����ͭ�缫�ƶ�
�ο��𰸣�B
���������A��a��b������ʱ������Fe��Cu���á���������Һ�з�����Ӧ��Fe+CuSO4=FeSO4+Cu����Ƭ�ϻ��н���ͭ��������ȷ��B��a��b�õ�������ʱ������ԭ��ء�Fe��������Cu����������Ƭ�Ϸ����ķ�ӦΪ��Fe-2e- = Fe2+������C����A��B�ķ������ѷ��֣�����a��b�Ƿ����ӣ���Ƭ�����ܽ⣬��Һ����ɫ��dz����ȷ��D����a��b�ֱ�����ֱ����Դ������������aΪ������bΪ����������ͬ�ֵ����ų⣬���ֵ���������ԭ��Cu2����ɽ϶��ͭ�缫�ƶ���SO42-�����缫�ƶ�����ȷ��
�����Ѷȣ�һ��
2������� ��1����֪��P4�����ף�s����5O2��g����P4O10��s��?��H����2983.2kJ/mol
P�����ף�s����5/4O2��g����1/4 P4O10��s��? ��H����738.5kJ/mol
�����ת��Ϊ�����Ȼ�ѧ����ʽΪ?���ɴ�˵�������ȶ��ԱȰ���?��
��2������[KAl(SO4)2��12H2O]ˮ��Һ��?����ᡱ��������С����ԣ��������ܾ�ˮ�������ӷ���ʽ������ԭ��Ϊ?��
��3�����ص�����ת����ʽΪ?��ԭ��ط�Ӧ?���һ������һ�������Է���
��4��pH=3�������pH=3�Ĵ�����Һ��ϡ�����������100����ϡ�ͺ������pH?(����ڡ�����С�ڡ����ڡ�)�����pH������ʱpH=x�������pH=y��NaOH��Һ��1�U10������Ȼ�ϣ���Ӧ����Һǡ�ó����ԣ���x��y����Ĺ�ϵ��?��
�ο��𰸣�
��1��P4�����ף�s����4P�����ף�s��?��H����29.2kJ/mol?�ߣ��á�����ǿ���ȣ�
��2����? Al3++3H2O  Al(OH)3�����壩+3H+
Al(OH)3�����壩+3H+
��3������ת��Ϊ��ѧ��?һ��
��4������? x+y=13
�����������1����Ӧ��-�ڡ�4�ó�P4�����ף�s����4P�����ף�s��?��H����29.2kJ/mol����Ӧ���Ⱥ����ȶ�����2��������������ˮ������ԣ���4��ϡ��ʱ�����ܵ���������ӣ�����ϡ�ͺ������pH���ڴ�����������е�ʽΪ10-x��1=10-��14-y����10? x+y=13
�����Ѷȣ�һ��
3��ѡ���� ������������ȷ����(����)��
A��ԭ��صĸ��������õ��ӵĻ�ԭ��Ӧ
B��ԭ����нϻ��õĽ���������
C��ԭ����еĵ缫һ��Ҫ�����ֲ�ͬ�Ľ������
D��ԭ����з���������Ӧ�ĵ缫�Ǹ���
�ο��𰸣�D
���������ԭ��ص��������������ֻ����Բ�ͬ�Ľ�����Ҳ�������ɽ�����ǽ���(����ʯī)���ɣ�ԭ��صĸ���ʧȥ���ӷ���������Ӧ����A��B��Cѡ�����ֻ��Dѡ����ȷ��
�����Ѷȣ�һ��
4��ѡ���� ijԭ��صĵ�ط�ӦΪFe��2Fe3+��3Fe2+����˵�ط�Ӧ�����ԭ�����
[? ]
A��ͭƬ����Ƭ��FeCl3��Һ��ɵ�ԭ���
B��ʯī����Ƭ��Fe(NO3)3��Һ��ɵ�ԭ���
C����Ƭ��пƬ��Fe2(SO4)3��Һ��ɵ�ԭ���
D����Ƭ��ʯī��Fe(NO3)2��Һ��ɵ�ԭ���
�ο��𰸣�AB
���������
�����Ѷȣ���
5������� ij��ѧ�о�С�齫пƬ��ͭƬ����ij�ֵ������Һ��пƬ��ͭƬ�õ����������γ�ԭ���װ�ã�
��1�����������Һ��ϡ���ᣬ����������Ӧ����______�����п����ͭ������ͬ������Һ�е�H+����______����ͭ���ϵĵ缫��Ӧʽ��______��
��2�����������Һ������ͭ��Һ��ͭ���ϵĵ缫��Ӧʽ��______������Ӧ��������0.2mol���ӷ���ת�ƣ���������Һ��������______g��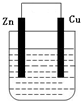
�ο��𰸣���1����װ����ԭ��أ�пʧ���Ӷ���������ͭ��������������ʧ���ӷ���������Ӧ�������ϵõ��ӷ�����ԭ��Ӧ��ԭ��طŵ�ʱ��������������ͭ�ƶ��������������ӵõ��������������缫��ӦʽΪ��2H++2e-=H2����
�ʴ�Ϊ��п��ͭ��2H++2e-=H2����
��2����װ���У�������пʧ���ӣ�������ͭ���ӵõ�������ͭ���缫��ӦʽΪ��Cu2++2e-=Cu��������п���п���ӽ�����Һ������������ͭ��������Һ���ӵ�����=0.2mol2��(65-64)g/mol=0.1g��
�ʴ�Ϊ��Cu2++2e-=Cu��0.1��
���������
�����Ѷȣ�һ��