��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʵ����������Ӧ�Ľ��۾���ȷ����
ѡ��
| ��?��
| ��?��
| ��?��
|
A
| ����ҺX�еμ�NaOHϡ��Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿ�
| ��ֽ������
| ��ҺX����NH
|
B
| ����������ˮ����FeCl2��NaI�Ļ����Һ�У��ٵμ�CCl4�������ã����ϲ���Һ�еμ�KSCN��Һ
| �ϲ���Һ����죬
�²���Һ�Ϻ�ɫ
| �����ԣ�Br2��Fe3+��I2
|
C
| ��ˮ����ͨ�����ȵ�����
| ��ĩ���
| ����ˮ�ڸ����·�����Ӧ
|
D
| ��Ư���ϼ����Ũ�����ᣬ��ʪ����۵⻯����ֽ�����Թܿ�
| �������ݣ���ֽδ����
| Ư���Ѿ�ʧЧ
|
?
�ο��𰸣�D
���������A������NH4+��Ҫ��ŨNaOH��Һ�����ȣ�ϡNaOH��Һ����ʹNH3�ӷ�����������B���μ�CCl4���²���Һ�Ϻ�ɫ��˵��Br2����I?������I2���ϲ���Һ����죬��֤��Br2��Fe3+�������ԣ�����C����ˮ����ͨ�����ȵ����ۣ�����ˮ������Ӧ����Fe3O4��Fe3O4Ϊ��ɫ���������D���������ݣ�ʪ����۵⻯����ֽδ������˵�����������岻��Cl2����Ư���Ѿ�ʧЧ����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ���������Ӧ������������������ǿ������˳��Ϊ��?��
��2Fe+3Cl
 2FeCl
2FeCl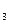
��Fe+2HCl FeCl
FeCl +H
+H ��
��
��2KMnO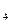 +16HCl��Ũ��
+16HCl��Ũ�� 2KCl+2MnCl
2KCl+2MnCl +5Cl
+5Cl ��+8H
��+8H O
O
��MnO +4HCl��Ũ��
+4HCl��Ũ�� MnCl
MnCl +Cl
+Cl ��+2H
��+2H O
O
��O +4HCl��Ũ��
+4HCl��Ũ�� 2Cl
2Cl ��+2H
��+2H O
O
A��Cl ��MnO
��MnO ��O
��O ��KMnO
��KMnO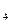 ��HCl
��HCl
B��KMnO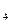 ��MnO
��MnO ��O
��O ��Cl
��Cl ��HCl
��HCl
C��KMnO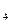 ��O
��O ��MnO
��MnO ��Cl
��Cl ��HCl
��HCl
D��KMnO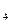 ��O
��O ��Cl
��Cl ��MnO
��MnO ��HCl
��HCl
�ο��𰸣�B
������������ҳ������Ӧ�������������������ٰ�������ж������жϡ��������ԣ������������������ͬһ��ԭ����������IJ��ﻯ�ϼ�Խ�ߣ�����������������Խǿ��������������ͬ����Խ�����ķ�Ӧ������Ҫ��Խ�ͣ�����������������Խǿ���������Ӧ�е���������������KMnO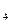 ��MnO
��MnO ��O
��O ��Cl
��Cl ��HCl��
��HCl��
�����Ѷȣ�һ��
3������� ��Ҫ����ա�
(1)��S2����Fe2����Fe3����Mg2����S��I����H���У�ֻ�������Ե���?��ֻ�л�ԭ�Ե���?���������������л�ԭ�Ե���?��
(2)ijͬѧд������������ѧ����ʽ(δ��ƽ)
��NO��HNO3�D��N2O3��H2O
��NH3��NO�D��HNO2��H2O
��N2O4��H2O�D��HNO3��HNO2
��������Ϊһ��������ʵ�ֵ���?��
(3)��������������ԭ��Ӧ�У���������ǿ��������?��
��2FeCl3��2KI=2FeCl2��2KCl��I2
��2FeCl2��Cl2=2FeCl3
��2KMnO4��16HCl(Ũ)=2KCl��2MnCl2��5Cl2����8H2O
��������Cl����I�����棬Ϊ������I����Cl�������������������⣬��Ӧ��������Ӧ�е�?����������
�ο��𰸣�(1)Fe3����Mg2����H����I����S2����Fe2����S��(2)��
(3)KMnO4��FeCl3
���������(1)����Ԫ�ػ��ϼ����������жϡ�(2)������ͬ��Ԫ�ز�ͬ��̬���������ʷ���������ԭ��Ӧʱ���������и�Ԫ�صļ�̬Ӧ�������ַ�Ӧ��Ԫ�ؼ�̬֮�䡣NԪ�أ�3���룫2��֮��ӦΪ0�ۻ�1�ۣ������ܳ��֣�3�۵ĵ������Ԣ�ʽ����ʵ�֡�(3)�ɢ�֪�����ԣ�FeCl3��I2����ԭ�ԣ�I����Fe2�����ɢ�֪�����ԣ�Cl2��FeCl3����ԭ�ԣ�Fe2����Cl�����ɢ�֪�����ԣ�KMnO4��Cl2����ԭ�ԣ�Cl����Mn2�����ɴ���֪������ǿ��˳��ΪKMnO4��Cl2��FeCl3��I2����ԭ��ǿ��˳��ΪI����Fe2����Cl����Mn2��������KMnO4������Cl����Fe2����
I����FeCl3ֻ����I�������Ա���ѡ���Cl2���������IJ����I2��������ǿ��������FeCl3��
�����Ѷȣ�һ��
4��ѡ���� ���ݱ�����Ϣ�жϣ�����ѡ���ȷ����
���
| ��Ӧ��
| ����
|
��
| KMnO4 ��H2O2 ��H2SO4
| K2SO4 ��MnSO4 ������������
|
��
| Cl2 ��FeBr2
| FeCl3��FeBr3
|
��
| MnO4�� ������������
| Cl2 ��Mn2+ ������������
|
A���ڢ��鷴Ӧ���������ΪH2O�� O2
B���ڢ��鷴Ӧ��Cl2 �� FeBr2�����ʵ���֮��С�ڻ����1
�ο��𰸣�
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪���з�Ӧ��Co2O3 + 6HCl(Ũ) = 2CoCl2 + Cl2��+ 3H2O?��I��
5Cl2 + I2 + 6H2O =" 10HCl" + 2HIO3?��II��
����˵����ȷ����
A����ӦI��HCl��������
B����ӦII ��Cl2����������Ӧ
C����ԭ�ԣ�CoCl2�� HCl �� I2
D�������ԣ�Co2O3�� Cl2��HIO3
�ο��𰸣�D
���������A����ӦI��HCl�ǻ�ԭ��������B����ӦII ��ClԪ�ػ��ϼ۽��ͣ�������ԭ��Ӧ������C��ͬһ��Ӧ�У���ԭ���Ļ�ԭ�Դ��ں��в���Ļ�ԭ�ԣ������л�ԭ�ԣ�CoCl2 < HCl < I2������D��ͬһ��Ӧ�У��������������Դ�����������������ԣ����Է�ӦI��Co2O3����������Cl2�����������ӦII ��Cl2����������HIO3�����������ȷ����ѡD��
�����Ѷȣ�һ��