微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。
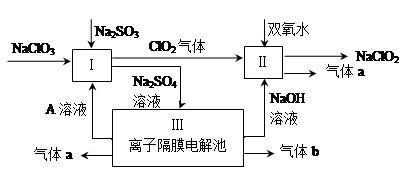
(1)Ⅰ、Ⅲ中发生反应的还原剂分别是?、?(填化学式)。
(2)Ⅱ中反应的离子方程式是?。
(3)A的化学式是?,装置Ⅲ中A在?极区产生。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
5NaClO2 + 4HCl =" 5NaCl" + 4ClO2↑ + 2H2O。
① 该反应中氧化剂和还原剂的物质的量之比是?。
② 研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是?。
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量相同,从电子守恒的角度解释其原因是?。
参考答案:(1)Na2SO3? H2O(2分)
(2)2ClO2 + H2O2 + 2OH- = 2ClO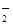 + O2↑+ 2H2O(2分)
+ O2↑+ 2H2O(2分)
(3)H2SO4(2分)?阳 (2分)?
(4)1∶4 (2分)? ClO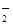 的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2?(2分)
的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2?(2分)
(5)NaClO2变质前后分别与Fe2+反应时,最终均得到等量NaCl,Cl元素均由+3价变为-1价,根据电子守恒,两个过程中得到的电子的物质的量相同(2分)
本题解析:(1)Ⅰ中发生的反应是亚硫酸钠被氯酸钠氧化,、Ⅲ中发生的反应是电解水,因此在这两个反应中还原剂分别是:Na2SO3? H2O(2分)
(2)2ClO2 + H2O2 + 2OH- = 2ClO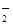 + O2↑+ 2H2O(2分)
+ O2↑+ 2H2O(2分)
(3)Ⅲ装置中左边氢氧根离子放电,剩余的氢离子跟硫酸根离子结合成硫酸,所以A是:H2SO4; 因为是氢氧根离子放电,所以这边是电解池的阳极。
(4)在这个反应中发生的是亚氯酸钠中氯元素的自身氧化还原反应,既作氧化剂,也作还原剂,作氧化剂的亚氯酸钠是化合价降低的,也就是由正三价变成正一价,为一摩尔,作还原剂的亚氯酸钠是化合价升高的,也就是由正三价变成正四价,为四摩尔,所以该反应中氧化剂和还原剂的物质的量之比是1∶4 ;ClO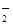 的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2 。
的氧化性或Cl-的还原性随溶液的酸性和浓度的增大而增强,因此Cl-被氧化得到Cl2 。
(5)NaClO2变质前后分别与Fe2+反应时,最终均得到等量NaCl,Cl元素均由+3价变为-1价,根据电子守恒,两个过程中得到的电子的物质的量相同(2分)
本题难度:一般
2、选择题 右图是一种试验某气体化学性质的实验装置。在A处通入氯气,图中B为开关,关闭B时,C中红色布条颜色无变化;打开B时,C处红色布条颜色褪去。由此做出的判断正确的是
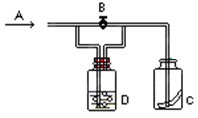
A.D中可以是水
B.D中可以是饱和食盐水
C.D中不可能是浓H2SO4
D.通入的氯气中含有水蒸气
参考答案:D
本题解析:氯气溶于水生成的次氯酸具有强氧化性,能使有色布条褪色。关闭B时,C中红色布条颜色无变化,这说明氯气通入D中时要么是氯气被D中溶液吸收而反应完全,要么就是氯气被D中溶液干燥。水或饱和食盐水均不能干燥氯气或完全吸收氯气,A、B选项不正确;浓硫酸具有吸水性,可以干燥氯气,因此D中试剂可以是浓硫酸,C不正确;又因为打开B时,C处红色布条颜色褪去,这说明通入的氯气一定含有水蒸气,所以选项D正确,答案选D。
本题难度:一般
3、填空题 (10分)新制氯水呈?色,说明氯水中有?存在。向氯水中滴入几滴AgNO3溶液,立即有?(填现象)生成,说明氯水中有?存在,蓝色石蕊试纸遇到氯水后,会首先变红,但很快褪色,说明氯水具有?性,氯水光照后,颜色?,溶液的酸性?,该反应的化学方程式是?
参考答案:黄绿,Cl2(或氯分子),白色沉淀,Cl-(或氯离子),酸性和漂白性,变浅(或褪去),增强, 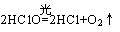
本题解析:新制的氯水中有H+、Cl-、ClO-、OH-、H2O、HClO、Cl2
本题难度:一般
4、填空题 氯气是一种重要的化工原料,除了用于消毒、制备盐酸和漂白剂外,还用于制备有机溶剂和农药。把氯气通入紫色石蕊溶液后,可以观察到的现象是_____________________________。请你解释其中的原因。
参考答案:溶液颜色应先变红,后逐渐褪为无色。因为氯气与水反应生成了盐酸和次氯酸:Cl2+H2O==HCl+HClO,溶液此时呈酸性使紫色石蕊溶液变红;因为生成的两种酸中有一种(次氯酸)具有漂白性,HClO把石蕊这种有机色质漂白,溶液红色又褪去。
本题解析:氯气通入紫色石蕊溶液后,溶液颜色应先变红,后逐渐褪为无色。这是因为氯气与水反应生成了盐酸和次氯酸:Cl2+H2O==HCl+HClO,溶液此时呈酸性使紫色石蕊溶液变红;因为生成的两种酸中有一种(次氯酸)具有漂白性,HClO把石蕊这种有机色质漂白,溶液红色又褪去。
本题难度:简单
5、实验题 (6分)为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。②该清液中滴加碳酸钠溶液产生白色沉淀。③该清液中滴加盐酸可产生大量气体。④该清液加热后变浑浊并产生大量气体。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有_________(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有______离子;清液中滴加盐酸产生的气体是________;清液加热后产生浑浊的原因是因为生成了________。
(2)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为:
?。
参考答案:(1)HClO Ca2+ CO2 CaCO3 (每空1分)
(2)2CaCO3+2Cl2+2H2O===Ca(HCO3)2+2HClO+CaCl2(2分)
本题解析:(1)有极强的漂白作用,说明含有次氯酸;清液中滴加碳酸钠溶液产生白色沉淀,白色沉淀是碳酸钙,说明该清液中含有Ca2+;清液中滴加盐酸产生的气体应该是CO2;该清液加热后变浑浊并产生大量气体,说明含有碳酸氢钙,加热使其分解生成了白色沉淀碳酸钙和CO2。
(2)根据以上分析可知,反应中生成物是碳酸氢钙、氯化钙和次氯酸,方程式是2CaCO3+2Cl2+2H2O===Ca(HCO3)2+2HClO+CaCl2。
本题难度:一般