微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据下列物质的名称,就能确认是纯净物的是
A.溴乙烷
B.二溴乙烷
C.已烯
D.淀粉
参考答案:A
本题解析:
本题难度:困难
2、选择题 将一定质量的镁、铜组成的混合物加入足量稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO).向反应后的溶液中加入过量的6mol/L?NaOH溶液至沉淀完全,测得生成沉淀的质量比原混合物的质量增加了7.65g,则下列叙述中正确的是
A.当金属全部溶解时收集到NO的体积为3.36?L
B.当生成的沉淀达到最大量时,形成沉淀需要NaOH溶液的体积为V=75?mL
C.参加反应的金属的总质量一定是9.9?g
D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.45?mol
参考答案:B
本题解析:分析:将一定量的镁和铜组成的混合物加入到稀HNO3中,金属完全溶解(假设反应中还原产物只有NO),发生反应:3Mg+8HNO3 (稀)=3Mg(NO3)2+2NO↑+4H2O;3Cu+8HNO3 (稀)=3Cu(NO3)2+2NO↑+4H2O;
向反应后的溶液中加入过量的6mol/L?NaOH溶液至沉淀完全,发生反应:Mg(NO3)2+2NaOH=Mg(OH)2↓+2NaNO3;Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3,沉淀为氢氧化镁和氢氧化铜,生成沉淀的质量比原合金的质量增加7.65g,则氢氧化镁和氢氧化铜含有氢氧根的质量为7.65g,氢氧根的物质的量为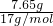 =0.45mol,则镁和铜的总的物质的量为0.225mol,
=0.45mol,则镁和铜的总的物质的量为0.225mol,
A.根据电子转移守恒计算NO物质的量,结合气体不一定是标准状况判断;
B.当生成的沉淀达到最大量时,溶液中溶质为NaNO3,硝酸根守恒可知n(NaNO3)=2n(硝酸铜+硝酸镁),由钠离子守恒由n(NaOH)=n(NaNO3),再根据V= 计算;
计算;
C.镁和铜的总的物质的量为0.225mol,金属的总质量与金属的含量有关;
D.根据氮元素守恒n(HNO3)=2n(硝酸铜+硝酸镁)+n(NO).
解答:将一定量的镁和铜组成的混合物加入到稀HNO3中,金属完全溶解(假设反应中还原产物只有NO),发生反应:3Mg+8HNO3 (稀)=3Mg(NO3)2+2NO↑+4H2O;3Cu+8HNO3 (稀)=3Cu(NO3)2+2NO↑+4H2O;
向反应后的溶液中加入过量的6mol/L?NaOH溶液至沉淀完全,发生反应:Mg(NO3)2+2NaOH=Mg(OH)2↓+2NaNO3;Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3,沉淀为氢氧化镁和氢氧化铜,生成沉淀的质量比原合金的质量增加7.65g,则氢氧化镁和氢氧化铜含有氢氧根的质量为7.65g,氢氧根的物质的量为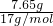 =0.45mol,则镁和铜的总的物质的量为0.225mol,
=0.45mol,则镁和铜的总的物质的量为0.225mol,
A.根据电子转移守恒可知生成的NO物质的量为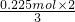 =0.15mol,若为标准状况下,生成NO的体积为0.15mol×22.4L/mol=3.36L,但NO不一定处于标准状况,故A错误;
=0.15mol,若为标准状况下,生成NO的体积为0.15mol×22.4L/mol=3.36L,但NO不一定处于标准状况,故A错误;
B.当生成的沉淀达到最大量时,溶液中溶质为NaNO3,硝酸根守恒可知n(NaNO3)=2n(硝酸铜+硝酸镁)=0.225mol×2=0.45mol,由钠离子守恒由n(NaOH)=n(NaNO3)=0.45mol,故此时氢氧化钠溶液的体积为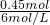 =0.075L=75mL,故B正确;
=0.075L=75mL,故B正确;
C、镁和铜的总的物质的量为0.225mol,假定全为镁,质量为0.225mol×24g/mol=5.4g,若全为铜,质量为0.225mol×64g/mol=14.4g,所以参加反应的金属的总质量(m)为5.4g<m<14.4g,故C错误;
D、根据氮元素守恒n(HNO3)=2n(硝酸铜+硝酸镁)+n(NO)=0.225mol×2+0.15mol=0.6mol,故D错误;
故选B.
点评:本题主要考查混合物有关计算,涉及镁铜与硝酸反应、生成的盐与氢氧化钠反应,综合考查学生的得失电子守恒、质量守恒等综合运用和解决复杂问题的能力,是一道考查能力的好题,难度较大.
本题难度:一般
3、选择题 下列各组中的两种有机物,其最简式相同但既不是同系物,又不是同分异构体的是:
A.苯、苯乙烯
B.甲醛、乙二醛
C.对甲基苯酚、苯甲醇
D.甲酸、乙醛
参考答案:A
本题解析:分子式相同而结构不同的化合物互为同分异构体,结构相似,分子组成相差若干个CH2原子团的同一类物质互为同系物,所以选项A正确;B和D中最简式是不相同的,C中互为同分异构体,所以答案选A。
考点:考查同系物、同分异构体的判断。
点评:对于同系物、同分异构体这2个概念,学习时应着重从其定义、对象、化学式、结构和性质等方面进行比较,抓住各自的不同点,注意从本质上理解和掌握。
本题难度:简单
4、选择题 下列各试剂中,不能用来鉴别Fe2+溶液和Fe3+溶液的是
A.NaOH?溶液
B.盐酸
C.NH4SCN?溶液
D.KSCN溶液
参考答案:B
本题解析:分析:三价铁离子的检验方法为:取待测液于试管中,向待测溶液中加入KSCN溶液,溶液立刻变成红色说明溶液中有Fe3+,即Fe3++3SCN-?Fe(SCN)3;根据常见离子的颜色判断Fe3+(黄色);Fe3+与OH-反应生成红褐色Fe(OH)3;
二价铁离子的检验方法为:再取待测液于试管中,加KSCN溶液没有明显现象,加入氯水溶液变成红色,说明溶液只有Fe2+;根据常见离子的颜色判断Fe2+(浅绿色);向Fe2+溶液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色;据此即可解答.
解答:A.向Fe2+溶液中加入NaOH溶液后,Fe2+与OH-反应生成Fe(OH)2,Fe2++2OH-=Fe(OH)2↓,Fe(OH)2不稳定易被氧气氧化为Fe(OH)3,4Fe(OH)2+O2+2H2O=4Fe(OH)3,白色的Fe(OH)2沉淀变成红褐色Fe(OH)3,向Fe2+溶液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色;Fe3+与OH-反应Fe3++3OH-=Fe(OH)3↓,生成红褐色Fe(OH)3,两者反应现象不同,故A正确;
B.盐酸和分Fe2+和Fe3+不反应,不能区别Fe2+和Fe3+,故B错误;
C.加入NH4SCN溶液,发生络合反应,Fe3++3SCN-?Fe(SCN)3溶液立即呈血红色,证明含有三价铁离子;加NH4SCN溶液没有明显现象加入氯水溶液变成红色,说明溶液只有Fe2+,故C正确;
D.加入KSCN溶液,发生络合反应,Fe3++3SCN-?Fe(SCN)3溶液立即呈血红色,证明含有三价铁离子;加KSCN溶液没有明显现象加入氯水溶液变成红色,说明溶液只有Fe2+,故D正确;
故选B.
点评:本题考查了二价铁离子和三价铁离子的实验检验方法的应用,根据离子检验产生特征现象进行判断是解答的关键,题目较简单.
本题难度:困难
5、选择题 2010年上海世博实现了环保世博、生态世博目标,下列做法不符合这一目标的是
A.推广和使用电动汽车
B.利用太阳能作为能源
C.在停车场安装催化光解设施处理汽车尾气
D.把世博会期间产生的垃圾焚烧或深埋处理
参考答案:D
本题解析:分析:推广使用电动汽车、利用太阳能作为能源可减少尾气排放,利用催化光解设施处理汽车尾气,减少对空气的污染,有利于环境保护,符合环保世博、生态世博的目标;焚烧垃圾或深埋处理会造成空气或土壤的污染.
解答:A、推广使用电动车可减少汽车尾气的排放,故A正确;
B、利用太阳能,节省能源,有利于环境保护,故B正确;
C、停车场的催化光解设施处理汽车尾气,减少对空气的污染,有利于环境保护,故C正确
D、处理垃圾中废弃塑料制品,如果焚烧,含氯塑料会产生有毒的氯化氢气体,从而污染空气;如果把垃圾深埋处理会造成土壤污染,因此该做法不符合环境保护的措施,故D错误;
故选D.
点评:本题考查化学环境的保护措施,题目较为简单,注意把握环境污染和环境保护的常识.
本题难度:一般