微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是( )
A.石英玻璃和普通玻璃成分相同
B.工艺师可用盐酸刻蚀玻璃制作工艺品
C.由石英沙制备单晶硅不涉及氧化还原反应
D.Si可用于信息存储,SiO2可用于光纤通讯
参考答案:D
本题解析:
本题难度:一般
2、填空题 据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4・nH2O)。
(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是?。
(2)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
①在101 KPa时,1.6 g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64 kJ。则甲烷与H2O(g)反应的热化学方程式:?。
②CH4不完全燃烧也可制得合成气:CH4(g)+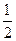 O2(g)===CO(g)+2H2(g);
O2(g)===CO(g)+2H2(g);
△H="-35.4" kJ・mol-1。则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为(填序号);原因是?。
③在温度为T,体积为10L的密闭容器中,加入1 mol CO、2 mol H2,发生反应
CO(g)+ 2H2(g)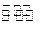 CH3OH(g);△H="-Q" kJ・mol-1(Q>O),达到平衡后的压强是开始时压强的0.6倍,放出热量Q1kJ。
CH3OH(g);△H="-Q" kJ・mol-1(Q>O),达到平衡后的压强是开始时压强的0.6倍,放出热量Q1kJ。
I.H2的转化率为?;
II.在相同条件下,若起始时向密闭容器中加入a mol CH3 OH(g),反应平衡后吸收热量Q2 kJ,且Q1+Q2=Q,则a=?mol。
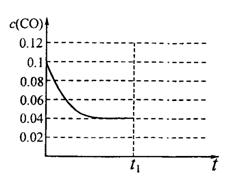
III.已知起始到平衡后的CO浓度与时间的变化关系如右图所示。则t1时将体积变为5L后,平衡向?反应方向移动(填“正”或“逆”);
 ?
?
在上图中画出从tl开始到再次达到平衡后,
CO浓度与时间的变化趋势曲线。
(3)将CH4设计成燃料电池,其利用率更高,装置示意如右图(A、B为多孔性碳棒)。
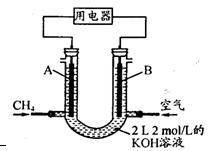
持续通人甲烷,在标准状况下,消耗甲烷体积VL。
①O<V≤44.8 L时,电池总反应方程式为?;
②44.8 L<V≤89.6 L时,负极电极反应为?;
③V=67.2 L时,溶液中离子浓度大小关系为?;
参考答案:
本题解析:略
本题难度:一般
3、选择题 下列叙述中,正确的是
A.三氧化二铁(Fe2O3)可用作红色涂料
B.硫在空气中燃烧生成三氧化硫
C.实验室收集氨气(NH3)应采用向上排空气法,因为其密度小于空气
D.干冰(CO)能用作制冷剂
参考答案:A
本题解析:分析:A、依据三氧化二铁的应用分析判断;
B、硫在氧气中反应只能生成二氧化硫;
C、氨气收集时用向下排气法收集;
D、干冰是二氧化碳固体;
解答:A、三氧化二铁(Fe2O3)颜色是红色,可用作红色涂料,故A正确;
B、硫在氧气中反应只能生成二氧化硫;故B错误;
C、氨气密度小于空气,收集时用向下排气法收集;故C错误;
D、干冰是二氧化碳固体,可以做制冷剂,故D错误;
故选A.
点评:本题考查了铁的氧化物性质的应用,氨气的收集,二氧化硫的生成,二氧化碳的性质应用,较简单.
本题难度:困难
4、选择题 化学和生活密切相关,下列叙述正确的是
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
B.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
C.氢能具有的优点是原料来源广、热值高、储存方便、制备工艺廉价易行
D.用聚苯乙烯全面代替木材,生产包装盒、快餐盒等以减少木材使用,保护森林
参考答案:B
本题解析:A 错误,汽油不是可再生能源
B 正确,使用太阳能、风能、海洋能、氢能,都不会生成二氧化碳,有利于缓解温室效应
C 错误,氢能不容易储存。
D 错误,聚苯乙烯不能降解,全面代替木材,生产包装盒、快餐盒等会造成大量白色污染。
本题难度:一般
5、填空题 (14分)无水AlCl3易升华,可用作有机合成的催化剂等。工业 上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
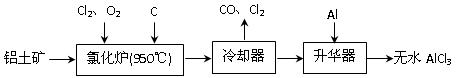
(1)氯化炉中Al2O3、C12和C反应的化学方程式为?▲?。
(2)用Na2SO3溶液可除去冷却器排出尾气中的Cl2,此反应的离子方程式为?▲ ?。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是?▲?。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3) 的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①写出除杂过程中涉及的离子方程式? ▲?、? ▲?。
②AlCl3产品的纯度为?▲ ?。
(5)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3・6H2O脱水制备无水AlCl3,实现这一步的方法是? ▲?。
参考答案:

本题解析:略
本题难度:简单