微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上由粗硅制取高纯硅有以下反应
①Si(固)+3HCl(气)==SiHCl3+H2(气),△H = -381kJ/mol"
②SiHCl3(气)+H2(气)==Si(固)+3HCl(气)
对上述反应的说法中正确的是
A.均为置换反应和氧化还原反应
B.反应①、②实际上互为可逆反应
C.由于反应①放热,则反应②可能是吸热的,也可能是放热的
D.提高SiHCl3产率,应采用加压和升温的办法
参考答案:A
本题解析:由①和②两个反应可知,都是单质和化合物反应,生成新的单质和化合物,并且都有电子的得失,故二者均为置换反应和氧化还原反应。又由于①和②可看成向两个方向进行的反应,但反应条件不同,故不属于可逆反应,B错;另,一个化学反应的一个方向为放热反应,则另一方向必为吸热反应,C错;由平衡移动原理可知,提高SiHCl3产率,应采用加压和降温的办法,D错。
本题难度:简单
2、选择题 下列冶炼方法中,可将化合物中的金属元素还原为金属单质的是
A.加热Al2O3
B.加热CaCO3
C.电解熔融NaCl
D.氯化钠与铝粉高温共热
参考答案:C
本题解析:A、铝是活泼的金属,只能通过电解法冶炼,因此电解熔融的氧化铝可以获得金属铝,A不正确;B、钙是活泼的金属,只能通过电解法冶炼。加热碳酸钙分解生成氧化钙和CO2,B不正确;C、钠是活泼的金属,只能通过电解法冶炼,因此电解熔融的氯化钠可以得到钠,C正确;D、钠是活泼的金属,且活泼性强于铝,金属铝与氯化钠不可能发生铝热反应,D不正确,答案选C。
本题难度:一般
3、填空题 工业上制造普通玻璃的主要原料是________,主要设备是________,主要原料熔化后,发生的主要化学反应是_______、________。普遍玻璃的成分主要是________。
参考答案:纯碱、石英、石灰石;玻璃熔炉;SiO2+Na2CO3 NaSiO3+CO2↑;SiO2+CaCO3
NaSiO3+CO2↑;SiO2+CaCO3 CaSiO3+CO2↑;
CaSiO3+CO2↑;
Na2SiO3・CaSiO3・SiO2
本题解析:
本题难度:一般
4、选择题 “白色污染”是环保治理的一个重要方面,“白色污染”是指工业或生活中排放或废弃的(?)
A.工业废气
B.工业废水
C.矿渣
D.塑料
参考答案:D
本题解析:“白色污染”是指工业或生活中排放或废弃的塑料。
本题难度:简单
5、填空题 (12分)氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO42-等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺如下:
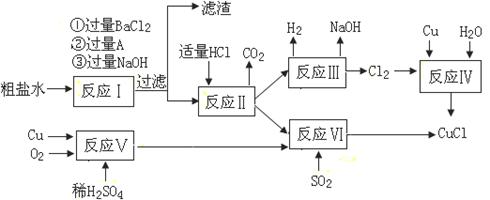
(1)A的化学式为?。
(2)写出反应V的化学方程式?。
(3)写出反应VI的离子方程式为?。
(4)本工艺中可以循环利用的物质是(用化学式表示)?。
(5)反应VI后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。于70℃真空干燥的目的是?、?。
参考答案:(1)Na2CO3?(2)2Cu+O2+2H2SO4=2CuSO4+2H2O
(3)2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO42-
(4)NaOH、H2SO4
(5)加快乙醇和水的蒸发,防止CuCl被空气氧化
本题解析:反应I是粗盐不的除杂过程,过滤后的滤液中加入适量盐酸,得到纯净的NaCl溶液;反应III是电解食盐水得到氯气,与铜、水一起制取CuCl。
反应V是制取硫酸铜,与SO2、NaCl通过反应VI也可制取CuCl
(3)由工艺流程可知,反应V消耗硫酸,而反应VI可产生硫酸;反应I消耗NaOH,而反应III电解食盐水过程中又可生产NaOH溶液。
(4)结合题目所给信息,在真空机中可防止产品的氧化、70℃温度可加快乙醇和水的蒸发
本题难度:一般