微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 实验室常用盐酸的质量分数为36.5%,密度为1.20g/cm3。
(1)此浓盐酸的物质的量浓度是多少?(列式计算)
(2)配制100mL3.00mol/L的盐酸,需以上浓盐酸多少mL?(列式计算)
(3)用浓盐酸配制该稀盐酸需要以下哪些步骤(按操作顺序填写序号):______________________。
①计算②装瓶③用50 mL量筒量取一定体积的浓盐酸④洗涤⑤移液⑥稀释⑦定容⑧摇匀
参考答案:(1)12mol/L
(2)25mL
(3)①③⑥⑤④⑦⑧②
本题解析:
本题难度:一般
2、选择题 相对分子质量为a的某物质在室温下的溶解度为bg,此时测得饱和溶液的密度为c?g?cm-3,则该饱和溶液的物质的量浓度是
A.mol?L-1
B.mol?L-1
C.mol?L-1
D.mol?L-1
参考答案:A
本题解析:分析:物质在室温下的溶解度为bg,饱和溶液的质量分数为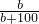 ,根据c=
,根据c=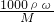 计算该饱和溶液的物质的量浓度.
计算该饱和溶液的物质的量浓度.
解答:该物质在室温下的溶解度为bg,所以饱和溶液的质量分数为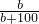 ,饱和溶液的密度为c?g?cm-3,该物质的相对分子质量为a,所以该饱和溶液的物质的量浓度为
,饱和溶液的密度为c?g?cm-3,该物质的相对分子质量为a,所以该饱和溶液的物质的量浓度为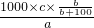 mol/L=
mol/L=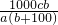 mol/L.
mol/L.
故选:A.
点评:考查物质的量浓度与溶解度的关系等,难度中等,可以根据定义法假设溶液体积计算溶质的物质的量进行计算.
本题难度:一般
3、选择题 已知t℃时一种饱和溶液的以下条件:①溶液质量?②溶剂质量?③溶液体积?④溶质的摩尔质量?⑤该温度下溶质的溶解度?⑥溶液密度.在以上条件的组合中,不能用来计算这种饱和溶液物质的量浓度的是( )
A.②③④⑥
B.④⑤⑥
C.①②④⑥
D.②③⑤
参考答案:A.根据③⑥可计算溶液的质量,再由②计算溶质的质量,再由④计算溶质的物质的量,利用c=nV可计算这种饱和溶液物质的量浓度,故A正确;
B.利用⑤可计算质量分数,再由④⑥结合c=1000ρwM可计算这种饱和溶液物质的量浓度,故B正确;
C.根据①②可计算溶质的质量,再由④计算溶质的物质的量,由①⑥可计算溶液的体积,利用c=nV可计算这种饱和溶液物质的量浓度,故C正确;
D.由②⑤可计算溶质的质量,但摩尔质量不知,则无法计算溶质的物质的质,所以无法计算浓度,故D错误;
故选D.
本题解析:
本题难度:简单
4、选择题 配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏低的原因是( )
A.称量时NaOH已经潮解
B.向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过
C.定容时俯视容量瓶的刻度线
D.定容摇匀后,有少量溶液外流
参考答案:A.氢氧化钠已经潮解,实际称量氢氧化钠的质量偏小,氢氧化钠的物质的量偏小,所配溶液的浓度偏低,故A符合;
B.溶液配制需加水定容,容量瓶事先用蒸馏水洗涤,对所配溶液浓度无影响,故B不符合;
C.定容是俯视刻度线,液面在刻度线以下,所配溶液的体积偏小,导致所配溶液的浓度偏高,故C不符合;
D.定容摇匀后,有少量溶液外流,剩余溶液浓度不变,故D不符合;
故选A.
本题解析:
本题难度:一般
5、简答题 (1)实验室需要用6mol/L的氢氧化钠浓溶液来配制0.3mol/L氢氧化钠稀溶液100mL,试列式计算所需氢氧化钠浓溶液的体积(mL).
(2)若将2.3g金属钠投入上述100mL氢氧化钠稀溶液中,设反应后溶液的体积仍然为100mL,此时溶液中的溶质是什么?其物质的量浓度是多少?
参考答案:(1)根据稀释定律,稀释前后溶液氢氧化钠的物质的量不变,令需要6mol/L的氢氧化钠浓溶液的体积为VmL,则:VmL×6mol/L=100mL×0.3mol/L,解得V=5,
答:需要6mol/L的氢氧化钠浓溶液的体积为5mL;
(2)将2.3g金属钠投入上述100mL氢氧化钠稀溶液中,钠与水反应生成氢氧化钠,溶液中溶质为NaOH;
2.3g金属钠的物质的量为2.3g23g/mol=0.1ml,根据钠元素守恒可知,溶液中生成的n(NaOH)=n(Na)=0.1mol,故NaOH浓度增大为0.1mol0.1L=1mol/L,故反应后NaOH的物质的量浓度为1mol/L+0.3mol/L=1.3mol/L,
答:反应后溶液中的溶质是NaOH,其物质的量浓度是1.3mol/L.
本题解析:
本题难度:一般