微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 常温下,向0.25mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液。
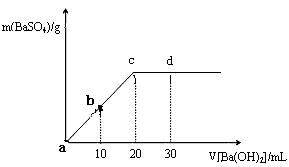
(1)硫酸溶液的体积为___________________ ;
(2)b时刻溶液中SO42-的浓度约为___________________mol/L;
(3)d时刻溶液中的pH约为____________________________;
(4)各时刻溶液的导电能力由大到小的顺序是_____________________________。
参考答案:(1)20mL
(2)0.5/3
(3)13
(4)a>b>d>c
本题解析:
本题难度:一般
2、选择题 日本核电厂爆炸释放出放射性131I,下列说法正确的是( )
A.131I与127I互为同素异形体
B.碘盐能使淀粉溶液变蓝
C.已知Ksp(AgBr)>Ksp(AgI),则AgBr可以转化为AgI
D.由I2(g)=2I(g)△H>0,说明碘原子比碘单质稳定
参考答案:A、131I与127I的质子数相同而中子数不同,二者属于同位素,同素异形体是指由同一种元素形成的不同单质,故A错误;
B、淀粉遇碘变蓝,而不是碘盐,故B错误;
C、结构相似的难溶电解质,溶度积常数越小越难溶,因Ksp(AgBr)>Ksp(AgI),则AgBr可以转化为AgI,故C正确;
D、I2(g)=2I(g)△H>0,该反应吸热说明反应物的总能力小于生成物的总能量,物质的总能量越高,越不稳定,说明碘单质比碘原子稳定,故D错误.
故选C.
本题解析:
本题难度:一般
3、选择题 某温度下向100g澄清的饱和石灰水中加入5.6g生石灰,充分反应后恢复原来的温度.下列叙述正确的是( )
A.沉淀物的质量为5.6g
B.沉淀物的质量为7.4g
C.饱和石灰水的质量大于98.2g
D.饱和石灰水的质量小于98.2g
参考答案:D
本题解析:向100g澄清石灰水中加入5.6g生石灰,反应如下:CaO+H2O=Ca(OH)2
5.6g 1.8g 7.4g,生成的7.4gCa(OH)2不能溶解,反应中消耗1.8g水,故与1.8g水对应的原溶质也要析出,
所以正确的答案选D。
本题难度:一般
4、选择题 下列有关溶度积常数Ksp的说法正确的是
A.常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp减小
B.溶度积常数Ksp只受温度影响,温度升高Ksp减小
C.溶度积常数Ksp只受温度影响,温度升高Ksp增大
D.常温下,向Mg(OH)2饱和溶液中加入NaOH固体,Mg(OH)2的Ksp不变
参考答案:D
本题解析:Ksp像其它常数一样,只与温度有关,对大多数难溶解电解质来说,温度升高,平衡向正向移动,Ksp增大,但也有减少的,A、B、C都错;答案选D。
本题难度:一般
5、选择题 向50 mL 0.018 mol/L的AgNO3溶液中加入50 mL 0.02 mol/L的盐酸生成沉淀。已知:Ksp(AgCl)=1.8×10-10 mol2・L-2,则生成沉淀后的溶液中c(Ag+)与pH分别为
A.1.8×10-7 mol/L,2
B.1×10-7 mol/L,2
C.1.8×10-7 mol/L,3
D.1×10-7 mol/L,3
参考答案:A
本题解析:硝酸银是0.0009mol,氯化氢是0.001mol,所以盐酸是过量的,反应后溶液中氯离子的物质的量是0.0001mol,浓度是0.0001mol÷0.1L=0.001mol/L,因此根据溶度积常数表达式可知,生成沉淀后的溶液中c(Ag+)=1.8×10-10 mol2・L-2÷0.001mol/L=1.8×10-7 mol/L。由于在反应中氢离子的物质的量是不变的,所以反应后溶液中氢离子浓度是0.001mol÷0.1L=0.01mol/L,因此pH=2,答案选A。
本题难度:一般