微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 若向某溶液中加入适量的溴水,溶液仍呈无色,则该溶液中可能含有的离子是(?)
A.Cu2+
B.I-
C.SO32-
D.Fe2+
参考答案:C
本题解析:若向溶液中加入适量的溴水溶液仍呈无色,则原溶液一定没有Cu2+、Fe2+、I-,因Cu2+、Fe2+有颜色,溴单质可与I-反应生成I2,碘水呈褐色或黄色,故原溶液中只能含有SO32-,因二者发生SO32-+Br2+H2O=SO42-+2Br-+2H+。
本题难度:一般
2、选择题 下列分离或提纯物质的方法正确的是
[? ]
A.用蒸馏的方法制取蒸馏水
B.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D.用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质
参考答案:A
本题解析:
本题难度:一般
3、填空题 除去括号内的杂质,写出所加试剂的化学式和相关反应的离子方程式。
(1)Cl-(SO42-) _____________,__________________ ;
(2)SO42-(CO32-) ____________,_____________________ ;
(3)NaCl(NaOH) _____________,_____________________ ;
(4)Fe2+(Cu2+) ______________,____________________ ;
参考答案:(1)BaCl2; Ba2++SO42- ==BaSO4
(2)H2SO4 ;CO32-+2H+ ==CO2 +H2O
(3)HCl; H+ +OH- = H2O
(4)Fe ;Fe +Cu2+ =Cu +Fe2+
本题解析:
本题难度:一般
4、选择题 NA表示阿伏加德罗常数的值,下列说法正确的是
A.标况下,22.4LNO2与水反应,转移的电子数为NA
B.常温下,78gNa2O2固体中阴离子数为NA
C.3g金刚石晶体中,含有的共价键数为NA
D.25℃时,pH=14的Ba(OH)2溶液1L,Ba2+数为NA
参考答案:B
本题解析:分析:A、体积换算物质的量,二氧化氮与水反应生成硝酸和一氧化氮,根据化学方程式计算电子转移;
B、质量换算物质的量结合过氧化钠的结构分析计算;
C、1mol碳原子和4mol碳原子形成共价键,每2mol碳原子形成1mol共价键;
D、计算氢氧根离子浓度结合体积计算物质的量,依据化学式计算钡离子.
解答:A、标况下,22.4LNO2物质的量为1mol,发生的反应为:3NO2+H2O=2HNO3+NO,3mol二氧化氮反应转移电子为2mol,所以1mol二氧化氮反应转移电子为 mol,故A错误;
mol,故A错误;
B、78gNa2O2固体物质的量为1mol,含阴离子O22-为1mol,故B正确;
C、3g金刚石晶体物质的量为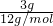 =0.25mol,含有的共价键数为0.5NA,故C错误;
=0.25mol,含有的共价键数为0.5NA,故C错误;
D、pH=14的Ba(OH)2溶液中氢氧根离子浓度为0.1mol/L,含氢氧根离子物质的量为0.1mol,所以钡离子物质的量为0.05ml,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,质量换算物质的量计算微粒数,金刚石的结构特征,pH有关的计算.
本题难度:一般
5、选择题 下列混合物的分离或提纯方法中,主要是从物质沸点的角度考虑的是
[?]
A.海水晒盐
B.蒸馏法淡化海水
C.分离豆浆和豆渣
D.熬煮中药
参考答案:B
本题解析:
本题难度:简单