| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《物质的量》高频试题特训(2017年最新版)(四)
参考答案:B 本题解析:物质的量的单位是mol,是国际上的七个基本物理量之一,用来描述一定数目微观粒子的集合体,不是质量,1mol任何微观粒子的数目大约是6.02×1023,但不能说物质的量的数值是6.02×1023,所以答案选B。 本题难度:简单 3、选择题 溶液中只含K+、Fe2+、Cl-、SO42-四种离子.已知K+、Fe2+、Cl-的个数比为3:2:1,则溶液中Fe2+与SO42-的个数比为 |
参考答案:A
本题解析:设K+、Fe2+、Cl-的物质的量分别为3mol,2mol,1mol。根据电荷守恒可以计算出硫酸根离子为3mol。所以溶液中Fe2+与SO42-的个数比为2:3
考点:电荷守恒
点评:本题难度不高,抓住选择题的做题技巧,可以把计算过程简略。
本题难度:一般
4、选择题 将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所
得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )
参考答案:D
本题解析:设蒸发后所得溶液的物质的量浓度为c,根据溶液浓缩过程中溶质的质量不变有:(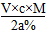 +m)×a%=V×c×M,解得:c=
+m)×a%=V×c×M,解得:c=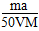 mol/L。
mol/L。
本题难度:一般
5、选择题 将百分比浓度为a%,物质的量浓度为c1 mol・L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol・L-1,则c1和c2的数值关系是( )
A.c2>2c1
B.c2=2c1
C.c2<2c1
D.无法确定
参考答案:A
本题解析:
试题解析:设将溶质质量分数为a%的硫酸溶液密度为ρ1,则c1= mol/L=
mol/L= mol/L,设将
mol/L,设将
溶质质量分数为2a%的硫酸溶液密度为ρ2,则c2= mol/L=
mol/L=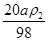 mol/L,所以c1:
mol/L,所以c1:
c2= :
: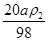 =ρ1:2ρ2,即c2=
=ρ1:2ρ2,即c2=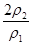 c1,硫酸溶液的浓度越大密度也越大,所以ρ2>ρ1,所以
c1,硫酸溶液的浓度越大密度也越大,所以ρ2>ρ1,所以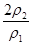 >2所以c2>2c1。
>2所以c2>2c1。
考点:物质的量浓度的相关计算
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《硫酸》高频.. | |