��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� 13�֣�A��B��C��D��EΪ��ѧ��ѧ�����ĵ��ʻ���ת����ϵ��ͼ��ʾ��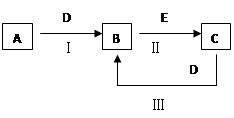
����A�ǵ���ɫ�����D��CO2��CΪNaOH��
��д��A�ĵ���ʽ?
��д����Ӧ��Ļ�ѧ����ʽ?
����A�ǵؿ��к������Ľ���Ԫ�صĵ��ʣ�B�ڻ���������ʱ����ʻ�ɫ��E��һ����ɫ��ζ�����壬�������ʯ��ˮ����ǡ�
��д��B�Ļ�ѧʽ?��д����Ӧ������ӷ���ʽ?
���õ����ŷ���ʾ��Ӧ�����ת�Ƶķ������Ŀ?��
�ο��𰸣�

�����������
�����Ѷȣ�һ��
2��ѡ���� ����������ȷ���ǣ�?��
A��Na+�к�ǿ�Ļ�ԭ��
B����ԭ���������11������
C�����ڿ�����ȼ������������
D���������ƿ���ΪDZˮͧ����������Դ
�ο��𰸣�D
���������A .Na+���������Ѵ��ȶ��ṹ��������ʧ���ӣ��������Ժͻ�ԭ�Զ���ǿ����A˵������
B.��ԭ������������Ϊ1�����������Ϊ11����B����
C.���ڿ�����ȼ�����ɹ������ơ�C����
��ѡD��
���������ⲻ�ѣ��������Ƶ�ԭ�ӽṹ�ص��뻯ѧ���ʵ���ϵ��ѧϰ���̶����⡰�ṹ�������ʡ���仰��
�����Ѷȣ�һ��
3��ѡ���� ���������ƣ�Ҳ���γ�O22�C���ӵĹ�����������������������?��?��

A��1mol�������ƻ��������������ˮ��Ӧ������0.5mol����

B�����������Ļ�ѧʽ��Ba2O2

C���������������ӻ�����

D���������ƺ�����������ǿ������
�ο��𰸣�
B



���������
���ݷ�Ӧ��2Na2O2+2H2O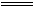 4NaOH+O2����2BaO2+2H2O
4NaOH+O2����2BaO2+2H2O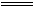 2Ba(OH)2
2Ba(OH)2
 +O2������֪1mol�������ƻ��������������ˮ��Ӧ������0.5mol������A��ȷ�����������Ļ�ѧʽΪBaO2��B��������������Ba2+��O22�C������ɣ��������ӻ����C��ȷ���������ƺ�������������ˮ��������̼��Ӧ�����������ʶ���ǿ��������D��ȷ��
+O2������֪1mol�������ƻ��������������ˮ��Ӧ������0.5mol������A��ȷ�����������Ļ�ѧʽΪBaO2��B��������������Ba2+��O22�C������ɣ��������ӻ����C��ȷ���������ƺ�������������ˮ��������̼��Ӧ�����������ʶ���ǿ��������D��ȷ��
�����Ѷȣ�һ��
4��ѡ���� ��ӦNaCl��CO2��NH3��H2O=NaHCO3����NH4Cl�������ġ������Ƽ������Ҫ��Ӧ��������4λͬѧ�Ը÷�Ӧ�漰���й�֪ʶ�����IJ��ּ��⡣���в���ȷ����? (����)��
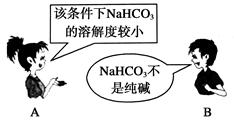

�ο��𰸣�C
�������������NaHCO3�����ҺΪNaHCO3�ı�����Һ��
�����Ѷȣ�һ��
5������� (1)��֪���ж����������ͨ��������������������ͳ�������ȡ�������мص������������Ļ��ϼۣ�
K2O________________,K2O2:________________,KO2:________________,KO3��_____________��
(2)������������������������ƣ���ǿ��������Ҳ�����������Էֱ�д��K2O2��CO2��H2O(g)��Ӧ�Ļ�ѧ����ʽ��
________________________________________��____________________________________��
(3)���������Ǹ�ǿ�������������������Էֱ�д����������(KO2)��CO2��H2O(g)��Ӧ�Ļ�ѧ����ʽ(�����绯��Ӧ)��
_________________________________________��___________________________________��
�ο��𰸣�(1)��-2? -1? -1/2? -1/3
(2)2K2O2+2CO2====2K2CO3+O2
2K2O2+2H2O====4KOH+O2��
(3)4KO2+2CO2====2K2CO3+3O2
4KO2+2H2O====4KOH+3O2��
���������(1)��K2O��K2O2��KO2��KO3����Ԫ�صĻ��ϼ۷ֱ�Ϊx��y��z���ء����ڻ����������������ϼ۵Ĵ���Ϊ0�����ԣ�
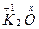 ��+1��2+x=0,x=-2;
��+1��2+x=0,x=-2;
 :+1��2+2y=0��y=-1��
:+1��2+2y=0��y=-1��
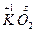 :+1+2z=0��z=-1/2��
:+1+2z=0��z=-1/2��
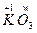 K+1Ow3:+1+3��=0����=-1/3��
K+1Ow3:+1+3��=0����=-1/3��
(2)K2O2��Na2O2����ɺͽṹ���ƣ����Na2O2��CO2��H2O�ķ�Ӧ����д��K2O2��CO2��H2O�ķ�Ӧ��
2Na2O2+2CO2====2Na2CO3+O2
2Na2O2+2H2O====4NaOH+O2��
2K2O2+2CO2====2K2CO3+O2
2K2O2+2H2O====4KOH+O2
(3)����KO2��CO2��H2O�ķ�Ӧ�����绯��Ӧ������CO2��H2O�и�Ԫ�صĻ��ϼ۷�Ӧǰ��δ�䡣����KO2����������������O2���ɣ�����һ������K2CO3��KOH��
2KO2+1CO2====1K2CO3+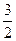 O2
O2
2KO2+1H2O====2KOH+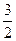 O2
O2
������������2�ã�
4KO2+2CO2====2K2CO3+3O2
4KO2+2H2O====4KOH+3O2
�����Ѷȣ���