微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了以下四种不同的方案,其中方法和现象判断不正确的是
A.用铂丝粘取固体在酒精灯火焰上灼烧,观察火焰的颜色
B.分别取样配成溶液,滴加CaCl2溶液,观察有无白色沉淀
C.分别加入1mol/L的盐酸溶液,看有无气泡产生
D.分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊
参考答案:C
本题解析:K2CO3和NaHCO3中阳离子不同,可用焰色反应鉴别,A可以;B.分别取样配成溶液,滴加CaCl2溶液,有白色沉淀的是K2CO3,无现象的是NaHCO3,B可以鉴别;K2CO3和NaHCO3都可以和盐酸反应产生气泡,C错误;D.分别取样在试管中加热,产生的气体通入澄清石灰水,变浑浊的是NaHCO3,正确。
本题难度:一般
2、选择题 如图是工业制纯碱的部分物质转化示意图,下列推测错误的是
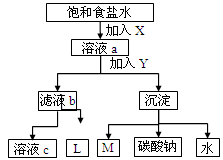
A.若是联碱法,溶液c可在转化流程中循环利用
B.若是氨碱法,则L的主要成分是NaCl
C.M可在转化流程中循环利用
D.X是NH3,Y是CO2
参考答案:AB
本题解析:A、若是联碱法,则X是氨气,Y是CO2,c是氯化铵溶液不能在转化流程中循环利用,A不正确;B、若是氨碱法,则L的主要成分是CaCl2,B不正确;C、M是CO2可以循环利用,C正确;D、由于氨气极易溶于水而CO2在水中的溶解性不大,所以X是NH3,Y是CO2,D正确,答案选AB。
本题难度:一般
3、选择题 Na3N是离子化合物,它和水作用可产生NH3,下列说法正确的是(?)
A.此反应是氧化还原反应
B.Na3N与盐酸反应可生成两种盐
C.Na3N和水反应时,Na3N是还原剂,H2O是氧化剂
D.在Na3N中氮显-3价,Na3N的电子式为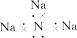
参考答案:B
本题解析:Na3N与水反应方程式为:Na3N+3H2O====3NaOH+NH3↑,分析可知该反应不是氧化还原反应,Na3N与水反应生成NaOH和NH3,所以Na3N与盐酸反应可生成钠盐和铵盐。Na3N是离子化合物,其电子式中的阴阳离子应标注电荷数,且N3-要用中括号。故答案为B。
本题难度:简单
4、选择题 将一定量的NaHCO3和Na2CO3的混合物加热到不再放出气体时,收集到CO2 aL,待冷却后。向残余物中加入足量盐酸又收集到CO22aL(体积均在标准状况下测定)。则混合物中Na2CO3和NaHCO3的物质的量之比为(?)
A.1∶1
B.1∶2
C.1∶3
D.1∶4
参考答案:B
本题解析:加热时碳酸氢钠分解生成碳酸钠和CO2以及水,反应的方程式是2NaHCO3 Na2CO3+H2O+CO2↑。碳酸钠和盐酸反应的方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑,其中和盐酸反应的碳酸钠包含碳酸氢钠分解生成的碳酸钠,所以根据CO2的体积可知混合物中Na2CO3和NaHCO3的物质的量之比为1∶2,答案选B。
Na2CO3+H2O+CO2↑。碳酸钠和盐酸反应的方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑,其中和盐酸反应的碳酸钠包含碳酸氢钠分解生成的碳酸钠,所以根据CO2的体积可知混合物中Na2CO3和NaHCO3的物质的量之比为1∶2,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的训练,有利于提高学生的逻辑推理能力。该题的关键是明确反应的原理,然后结合方程式灵活运用即可。
本题难度:简单
5、选择题 现有25 mL 2 mol・L-1 Na2CO3和75 mL 1 mol・L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中;②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况是( )。
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
参考答案:C
本题解析:①将Na2CO3溶液逐滴加入到盐酸中,开始时,HCl过量,有关反应为:
Na2CO3+ 2HCl=2NaCl+CO2↑+H2O
1 mol? 2 mol? 22.4 L
0.05 mol? 0.075 mol?V1
生成CO2的体积用HCl的量计算:
V1=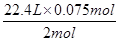 =0.84 L
=0.84 L
②将盐酸逐滴加入到Na2CO3溶液中,开始时,Na2CO3过量,反应分两步进行:
Na2CO3+ HCl = NaHCO3+NaCl
1 mol? 1 mol? 1 mol
0.05 mol? 0.05 mol? 0.05 mol
NaHCO3+ HCl=NaCl+H2O+CO2↑
1 mol 1 mol? 22.4 L
0.05 mol? (0.075-0.05)mol?V2
生成的CO2用剩余HCl的量计算:
V2=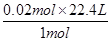 =0.56 L,所以V1>V2。
=0.56 L,所以V1>V2。
本题难度:一般