微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 不能用排水法收集的气体是(? )
A.H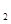
B.O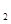
C.NO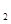
D.NO
参考答案:C
本题解析:3NO2+H2O=HNO3+NO,故NO2 不能用排水法收集;由于NO2的密度比空气大,所以只能用向上排空气法来收集。其它选项的气体都不能溶解于水,也不能和水反应反应,所以都可以用排水法收集,也可以用排空气法收集。选项为C.
本题难度:一般
2、实验题 (16分)乙二酸(HOOC-COOH)俗名草酸,易溶于水,属于二元中强酸,生产和科学实验中有着广泛的用途。草酸晶体的组成可用H2C2O4・xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液,量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol・L-1的KMnO4溶液滴定,
(1)将所发生的反应方程式完成并配平,将完整的化学方程式写在答题卡上。
 KMnO4 + H2C2O4?+ (?)---K2SO4 + CO2↑+ MnSO4 + (?)
KMnO4 + H2C2O4?+ (?)---K2SO4 + CO2↑+ MnSO4 + (?)
(2)整个实验过程中不需要的仪器有?(填序号)。
a.托盘天平(带砝码,镊子)b.酸式滴定管? c.烧瓶
d.100mL容量瓶? e.烧杯? f.漏斗? g.锥形瓶
h.玻璃棒? i.药匙?
(3)实验中,标准KMnO4溶液应盛装在____式滴定管中。滴定终点时溶液的
颜色变化为?。
(4)在滴定过程中若用去amol・L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为________mol・L-1,由此可计算x的值是___________。
(用含W、a、V的代数式表示)
(5)该小组同学将0.02mol草酸晶体(H2C2O4・2H2O)加入到100mL0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,则该溶液中各离子浓度由大到小的顺序为?
参考答案:(1)2KMnO4 +5 H2C2O4?+ 3H2SO4 ="==" K2SO4 + 10CO2↑+2 MnSO4 + 8H2O ?
(2)c , f?
(3)酸?溶液由无色变为浅紫色且半分钟不褪色?
(4)? 0.1aV?(5) C(Na+)>c(HC2O4-)>c(H+)>c(C2O42-) > c(OH-)
本题解析:根据题目中给出的条件,可以判断硫酸是反应物,根据守恒关系,可以判断生成物还有水,根据化合价的升高降低一致可以得到
(1)2KMnO4 +5 H2C2O4?+ 3H2SO4 ="==" K2SO4 + 10CO2↑+2 MnSO4 + 8H2O
(2)称取Wg草酸晶体,配成100.00mL水溶液,量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol・L-1的KMnO4溶液滴定,整个实验过程中必须的仪器a.托盘天平(带砝码,镊子)b.酸式滴定管 d.100mL容量瓶? e.烧杯? g.锥形瓶 h.玻璃棒? i.药匙?
(3)实验中,标准KMnO4溶液应盛装在酸式滴定管中,因为酸性高锰酸钾溶液具有强氧化性,会腐蚀橡胶软管,所以只能放在酸式滴定管中。滴定终点时溶液的颜色变化为溶液由无色变为浅紫色且半分钟不褪色
(4)在滴定过程中若用去amol・L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度根据定量关系2KMnO4? ---? -----5 H2C2O4 ?
2? 5
av/1000? 0.025y
所以y=0.1aV?
H2C2O4・xH2O 其摩尔质量是(18x+2+24+64)g/mol?
其物质的量是w/[(18x+2+24+64)] mol?实验时从100.00mL水溶液,量取25.00mL进行试验,所以滴定时消耗掉的草酸是0.01av? mol
所以0.01av=w/[(18x+2+24+64)]?所以 x=
(5)该小组同学将0.02mol草酸晶体(H2C2O4・2H2O)加入到100mL0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,因为草酸是二元中强酸,钠离子浓度最大,其次是HC2O4-仅仅小于钠离子浓度,氢离子有两部分构成,一部分是水电离的一部分是草酸电离的,所以c(H+)>c(C2O42-),所以该溶液中各离子浓度由大到小的顺序为 C(Na+)>c(HC2O4-)>c(H+)>c(C2O42-) > c(OH-)
点评:解答本题要从实验的目的出发,抓住定量关系,问题都会迎刃而解。酸碱中和滴定,是用已知物质量浓度的酸(或碱)来测定未知物质物质的量浓度的碱(或酸)的方法叫做酸碱中和滴定。实验中石蕊等做酸碱指示剂来判断是否完全中和。只要学生学习过程中牢记并理解这些基本定义,便不难解答此题。
本题难度:一般
3、填空题 (14分)高纯六水氯化锶(SrCl2・6H2O)可用于制造高档磁性材料、电解金属钠的助熔剂、高档颜料和液晶玻璃等,具有很高的经济价值。高纯六水氯化锶的制备过程如下:
Ⅰ.将纯水加入烧杯内,搅拌下加入适量工业碳酸锶粉末(含少量Ba、Fe的化合物),制成浆料。
Ⅱ.缓慢加入工业盐酸进行酸化,将固体物质溶解。
Ⅲ.然后喷淋加入适量的硫酸,再加入质量分数为30%的双氧水少许。
Ⅳ.调节pH至8~10, 加热至60~70℃, ,搅拌1h,过滤,除去残渣。
Ⅴ.滤液加热至沸,继续浓缩至氯化锶质量浓度(溶质质量与溶液体积之比)为 x g/L。
请回答:
(1)用电子式表示HCl的形成过程?。
(2)已知Sr为第五周期第ⅡA族元素,则不符合Sr>Ca的是?(填序号)。
①原子半径?②最外层电子数
③金属性?④最高价氧化物对应的水化物的碱性
(3)写出步骤Ⅱ中加入盐酸时发生反应的离子方程式:?。
(4)加入硫酸后会先生成硫酸锶沉淀,进而转化为硫酸钡沉淀,试分析原理?。
(5)步骤Ⅲ中在酸性环境下加入双氧水是为将亚铁离子氧化成铁离子,写出该反应的离子方程式:?。
(6)步骤Ⅳ中调节pH至8~10,最好选用的试剂为?。
(7)已知某次实验得到浓缩后的氯化锶溶液中溶质为818g,溶剂为1000 g,经测定该溶液的密度为1.5 g/mL,则该溶液溶质的质量浓度x为??g/L(计算结果保留整数)。
参考答案:(14分)
(1) (2分)
(2分)
(2)②(2分)
(3)SrCO3+2H+=Sr2++H2O+CO2↑(2分)
(4)溶液中大部分是氯化锶,所以加入硫酸后会先生成硫酸锶,由于硫酸钡的溶解度小于硫酸锶,所以会进一步转化为硫酸钡沉淀(2分)
(5)2Fe2+ + H2O2 + 2H +=2Fe3+ + 2H2O (2分)
(6)Sr(OH)2(2分)
(7)675(2分)
本题解析:略
本题难度:一般
4、实验题 (8分)下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生改进后的装置:

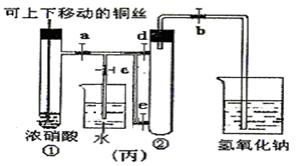
(1)写出铜和浓硝酸反应的化学方程式??。
(2)和甲装置相比,乙装置的优点??。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。先关闭弹簧夹??,再打开弹簧夹??,才能使NO2气体充满②试管。
(4)当气体充满②试管后,欲使烧杯中的水进入②试管应如何操作??。
参考答案:(1)Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O?(2分)
(2)①可以控制反应。②吸收NO2气体,防止污染环境。(2分)
(3)关闭c,d;打开a、b,e。(2分)
(4)先关闭b,迅速将铜丝提起与溶液脱离,再关闭a,e, 然后打开c,d,用手捂住②试管(热水、热毛巾、加热)。(合理答案均给分)?(2分)
本题解析:(1)硝酸具有强氧化性,能把铜氧化生成硝酸铜、NO2和水,方程式为
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。
(2)乙中铜丝可以上下移动,因此便于控制反应;其次有尾气处理装置,吸收NO2气体,防止污染环境。
(3)NO2的密度大于空气的,所以应该是先关闭弹簧夹c、d,然后再打开弹簧夹a、b、e,才能时NO2气体充满试管②。
(4)欲使烧杯中的水进入②试管,则必须使NO2溶于水降低越强,所以正确的操作是先关闭b,迅速将铜丝提起与溶液脱离,再关闭a,e,然后打开c,d,用手捂住②试管(热水、热毛巾、加热)。
本题难度:一般
5、选择题 下列实验能达到相应目的的是
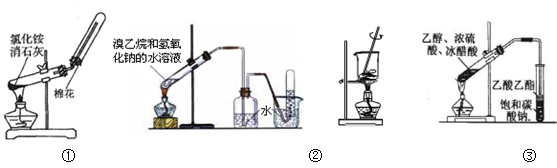
A.用图①装置制取并收集氨气
B.用图②装置制取和收集乙烯
C.用图③装置将海带灼烧成灰
D.用图④装置制取乙酸乙酯
参考答案:D
本题解析:A、实验室制取氨气时,因为有水生成,所以发生装置的试管应向下倾斜,错误;B、溴乙烷与氢氧化钠的水溶液发生取代反应,得到的是乙醇,不是乙烯,错误;C、灼烧海带应在坩埚中进行,错误;D、乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的溶解度小,所以用饱和碳酸钠吸收,正确,答案选D。
本题难度:一般