��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� д��ʵ�����ɱ���Ũ���ᷴӦ��ȡ�������Ļ�ѧ����ʽ��
?�÷�Ӧ����?��Ӧ��
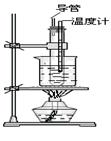
��2����ͼ��ʾ��ʵ��װ��ͼ�д�����Щ������ָ����
��?��
��?��
��?��
��3��ˮԡ��������Щ�ŵ㣿?��
���Թ��н�����Ũ���͵IJ���������?��
�ο��𰸣���14�֣�
��1��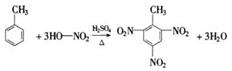 ?ȡ����Ӧ?
?ȡ����Ӧ?
��2���¶ȼ�Ӧ�����ձ��е���ˮ��?ֱ���ܲ�����?�Թܲ��������ձ��ײ�?
��3�����Ⱦ��ȱ��ڿ����¶�?��ȡһ������Ũ���ᣬȻ������������ע��Ũ���ᣬ�ӱ���
�����������1����Ũ����������£�����Ũ���ᷢ��������Ӧ��������������Ӧ�Ļ�ѧ����ʽ�� ���÷�ӦҲ��ȡ����Ӧ��
���÷�ӦҲ��ȡ����Ӧ��
��2���÷�Ӧ��ˮԡ���ȣ������¶ȼ�Ӧ�����ձ��е���ˮ�У����Թܲ��������ձ��ײ������ӷ�����ֱ���ܼ��������ͻ������ã���Ȼֱ���ܲ�������
��3������ˮԡ������ʹ���Ⱦ����ұ��ڿ����¶ȣ�Ũ������ܶȴ�������ģ���Ũ��������ˮ���ȣ��������Թ��н�����Ũ���͵IJ�����������ȡһ������Ũ���ᣬȻ������������ע��Ũ���ᣬ�ӱ���
�����������ǻ���������Ŀ��飬Ҳ�Ǹ߿��еij������㡣���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ��������������ѶȲ�����������Ҫ���Գ���������ѡ�á�ʵ���������Ϊ���ģ�ͨ����ʲô��Ϊʲô���������ص㿼��ʵ����������Ĺ淶�Ժ�ȷ�Լ��������֪ʶ���ʵ�������������
�����Ѷȣ�һ��
2��ѡ���� ���������У���������ˮ���ռ����ǣ�?��
A��O2
B��H2
C��NO2
D��NO
�ο��𰸣�C
�������������ˮ���ռ�����Ҫ�����岻����ˮ��Ӧ��������ˮ��NO2��ˮ��Ӧ���������һ���������ʲ�������ˮ���ռ���
���������������ռ�������ѡȡԭ������ס������������ʡ�
�����Ѷȣ���
3������� �������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
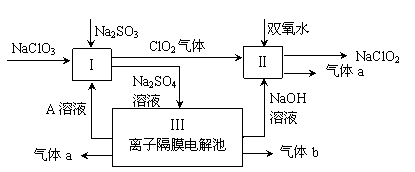
��1��˫��ˮ�ĽṹʽΪ��?�����з�����Ӧ�Ļ�ԭ�����������������ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ������������?������ ��
��3��A�Ļ�ѧʽ���������������� ��װ�â���A���������������� ����������
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���
��д���÷�Ӧ�Ļ�ѧ����ʽ����������������
���о�����������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��������������?����
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ���������?(����ͬ������ͬ�����ж�)
�ο��𰸣���14�֣���1��H-O-0-H? Na2SO3������2�֣�����
��2��2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O��2�֣�
��3��H2SO4����������2�֣�
��4��5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O������2�֣���
ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O��2�֣�
��5����ͬ��2�֣�
�����������H2O2��������ԭ�Ӽ��γ�һ�����õ��Ӷԣ��ṹʽΪ��H�DO�DO�DH����ӦI��2ClO3�D��SO32�D��2H��=2ClO2��SO42�D��H2O������SO32�D��S��+4�۱��+6�ۣ�����ԭ�������Ϊ��H�DO�DO�DH��Na2SO3�����ƴ�ͼ�ж�����Ӧ��ΪClO2��H2O2,��������������ΪNaClO2��ClO2����������H2O2�����ɨD1�۱�ɨD2��2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O���ʴ𰸣�2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O���Ǣ�������2H2O�D4e�D=4H�� ��O2��,aΪO2,������4H2O��4e�D=4OH�D?��2H2��,?bΪH2�� A�Ļ�ѧʽ��H2SO4, װ�â���A���������������𰸣�H2SO4��������Cl�DŨ�ȴ�ʱ����ԭ����ǿ�������ɵ�ClO2������5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O��ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O����Ϊ��5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O��ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O����ClO2�D��ClO3�D��Fe2�� ��Ӧ���ն����Cl�D������ǰ��ת�Ƶĵ�������ͬ����������Fe2+�����ʵ�����ͬ���𰸣���ͬ��
�����Ѷȣ���
4��ѡ���� ���ü�ʯ�Ҹ���������ǣ�������
A��NH3
B��Cl2
C��HCl
D��CO2
�ο��𰸣���ʯ���������ƺ��������ƵĻ������Լ�ʯ���Ǽ������ʣ����ܸ����������ʣ�
A�������Ǽ������壬���ͼ�ʯ�ҷ�Ӧ�����ü�ʯ�Ҹ����A��ȷ��
B��Cl2���������壬���Ժ��������Ʒ�Ӧ�������ü�ʯ�Ҹ����B����
C���Ȼ��������������壬�����������ƺ������Ʒ�Ӧ�����Բ����ü�ʯ�Ҹ����C����
D��������̼�����������壬�����������ƺ������Ʒ�Ӧ�����Բ����ü�ʯ�Ҹ����D����
��ѡA��
���������
�����Ѷȣ���
5��ʵ���� ��16�֣�.ijѧ������С�飬ģ���������еķ�Ӧԭ�����������ͼ��ʾ����������ȡ���������������������ͼ������װ��E�ɼס���������������ɣ���������Ƥ����ͨ����װ������ˮ�����п̶ȣ�0��50 mL�����������ã��ҹܿ������ƶ�����Һ��ߵ͡�
ʵ��ɹ�ѡ�õ�ҩƷ���У�ϡ���ᡢ���ᡢ�������ơ�̼���ơ�����ʯ��ˮ��
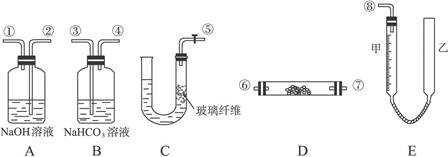
������������⣺
��1��ͼ�и�װ�ýӿ�����˳����_____������ӿڵı�ţ��������ӽ��ܼ��г�װ�þ�ʡ�ԣ���
��2��װ��C�з���ķ�Ӧ����__________��__________��
��3��װ��D�з����Ļ�ѧ��Ӧ����ʽ?
?
��4��װ��A��������___________________________________________________________��װ��B��������___________________________________________________________��
��5��Ϊ�˽�ȷ������������������˱���������װ�õ�������֮�⣬�ڶ���Ӧǰ�����Һ��Ķ����������ֵ�Ĺ����У�Ӧע��__________��__________������ĸ��ţ���
a.�����밼Һ����ʹ���ƽ? b.�ȴ�Ƭ�̣����ҹ���Һ�治������ʱ���̶���
c.����ʱӦ�����ƶ��ҹܣ�ʹ�ס�������Һ����ƽ? d.����ʱ��һ��ʹ�ס�������Һ����ƽ
��6����Ӧ������ò����������״�������Ϊ22.4 mL����Ӧ������ת�Ƶĵ�����ĿΪ??��
�ο��𰸣���1���ݢۢܢޢߢڢ٢ࣨ�ޡ��߿ɻ�λ��
��2������ʯ������
��3��2Na2O2��2H2O=4NaOH��O2��? 2Na2O2��2CO2=2Na2CO3��O2��
��4����ȥ����O2��δ��Ӧ��CO2������CO2�л��е�HCl
��5��ac
��6��1.204��1021
�����������1��ʵ����ͼӦ��������ȡCO2��Ȼ����ӣ���ͨ�����������O2��Ȼ���ȥO2�е����ʣ��ٲ���O2����������ԣ�ͼ�и�װ�ýӿ�����˳���Ǣݢۢܢޢߢڢ٢ࣨ�ޡ��߿ɻ�λ��
��2��װ��C��CO2�ķ���װ�ã����з���ķ�Ӧ���Ǵ���ʯ������
��3��ˮ������������̼������Na2O2��Ӧ����������2Na2O2��2H2O=4NaOH��O2��? 2Na2O2��2CO2=2Na2CO3��O2��
��4��װ��A�������dz�ȥ����O2��δ��Ӧ��CO2��װ��B������������CO2�л��е�HCl
��5��Ϊ�˽�ȷ������������������˱���������װ�õ�������֮�⣬�ڶ���Ӧǰ�����Һ��Ķ��������ֵ�Ĺ�����Ӧע�⣺�����밼Һ����ʹ���ƽ������ʱӦ�����ƶ��ҹܣ�ʹ��������Һ����ƽ����ѡac
��6���ɷ�Ӧ����ʽ��֪��ÿ��1molO2���ɣ�����2mol���ӵ�ת�ƣ��������ɵ�����Ϊ0.001mol����Ӧ������ת�Ƶĵ�����ĿΪ1.204��1021
�����Ѷȣ�һ��