| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《物质的量》高频考点特训(2017年练习版)(十)
参考答案:D 本题解析: 本题难度:一般 2、填空题 (8分)(1)两个同容积的密封容器A、B,常温下,A中充入a g A气体,B中充入a g CH4气体,A与B内的压强之比是4∶11,则A的摩尔质量为_________________。 参考答案:(每空2分,共8分) 本题解析:略 本题难度:一般 3、选择题 实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19 g・cm-3,则该浓盐酸物质的量浓度是( ) |
参考答案:B
本题解析:盐酸的溶质质量分数为36.5%,密度为1.19g/cm3,物质的量浓度为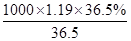 =11.9mol/L,答案选B.
=11.9mol/L,答案选B.
考点:物质的量浓度的计算
本题难度:一般
4、选择题 常温下Ca(OH)2溶于水达到饱和时存在如下平衡:Ca(OH)2(s) Ca2++2OH-,饱和石灰水的密度为d g/cm3,溶液pH=12。下列有关叙述中,不正确的是
Ca2++2OH-,饱和石灰水的密度为d g/cm3,溶液pH=12。下列有关叙述中,不正确的是
A.加热至50℃,溶液的Ca2+的浓度增大
B.该温度下Ca(OH)2的溶解度为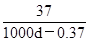 (g/100gH2O)
(g/100gH2O)
C.该饱和石灰水中,水电离出的OH-的浓度为10-12mol/L
D.加入生石灰并恢复至常温后, 值不变
值不变
参考答案:A
本题解析:A、氢氧化钙的溶解度随温度的升高而降低,因此加热至50℃,溶液的Ca2+的浓度减小,A不正确;B、溶液的pH=12,则溶液中氢氧根的浓度是0.01mol/L,所以氢氧化钙的浓度是0.01mol÷2=0.005mol/L。假设溶液是1L,则氢氧化钙的物质的量是0.005mol,质量是0.37g,其中溶剂水的质量是1000d-0.37g,所以氢氧化钙的溶解度是S=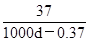 ,B正确;C、氢氧化钙是强碱抑制水的电离,则该饱和石灰水中,水电离出的OH-的浓度就是溶液中氢离子浓度为10-12mol/L,C正确;D、温度不变,离子的浓度不变,因此比值
,B正确;C、氢氧化钙是强碱抑制水的电离,则该饱和石灰水中,水电离出的OH-的浓度就是溶液中氢离子浓度为10-12mol/L,C正确;D、温度不变,离子的浓度不变,因此比值 不变,D正确,答案选A。
不变,D正确,答案选A。
本题难度:一般
5、选择题 由FeSO4和Fe2(SO4)3组成的混合物中,含硫为a%,则所含铁的质量百分含量为( )
A.3a%
B.(100-2a)%
C.20%
D.1-3a%
参考答案:FeSO4和Fe2(SO4)3中n(S):n(O)=1:4,可知混合物中硫元素与氧元素的质量比为32:16×4=1:2,混合物中含硫为a%,故混合物中氧元素质量分数=2a%,混合物中Fe元素质量分数=1-a%-2a%=1-3a%,
故选D.
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《常见的化学.. | |