微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 相对分子质量为M的某物质在室温下的溶解度为S,此时测得饱和溶液的密度为d?g?cm-3,则该饱和溶液的物质的量浓度为
A.mol?L-1
B.mol?L-1
C.mol?L-1
D.mol?L-1
参考答案:C
本题解析:分析:饱和溶液,由溶解度可计算质量分数,密度为d?g?cm-3,再利用c=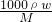 来计算.
来计算.
解答:在室温下的溶解度为S,此时测得饱和溶液的密度为d?g?cm-3,
溶质的质量分数为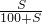 ×100%,
×100%,
由相对分子质量为M,c=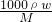 ,
,
则c=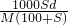 mol/L,
mol/L,
故选C.
点评:本题考查物质的量浓度的计算,熟悉质量分数与饱和溶液的溶解度的关系,质量分数与物质的量浓度的关系即可解答,难度不大.
本题难度:简单
2、选择题 将16 g Na2CO3・xH2O固体加热到质量不变,得固体10.6 g,则x值为(? )
A.3
B.5
C.8
D.10
参考答案:A
本题解析:Na2CO3・xH2O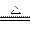 Na2CO3+xH2O
Na2CO3+xH2O
106? 18x
10.6 g? 16-10.6 g
x=3
本题难度:简单
3、选择题 使相同体积的NaCl、MgCl2、AlCl3 溶液中Cl-完全沉淀,若用去0.2mol/L 的AgNO3溶液的体积相等,则上述三溶液溶质的物质的量浓度之比为
[? ]
A.6:3:2
B.3:2:1
C.1:2:3
D.1:1:1
参考答案:A
本题解析:
试题分析:
解:用去0.2mol/L 的AgNO3溶液的体积相等,即消耗AgNO3的物质的量相等。
1molNaCl中Cl-完全沉淀需1molAgNO3,1/2molMgCl2 溶液中Cl-完全沉淀需1molAgNO3,1/3molAlCl3?溶液中Cl-完全沉淀需1molAgNO3,则上述三溶液溶质的物质的量浓度之比等于物质的量之比为1:1/2:1/3=6:3:2
故选:A.
本题难度:简单
4、选择题 0.2 mol某元素的单质直接与Cl2化合后,生成物质质量增加了14.2 g,这种元素的化合价是(? )
A.+1
B.+2
C.+3
D.+5
参考答案:B
本题解析:14.2 g Cl2的物质的量为: ="0.2" mol,故该元素M与Cl2反应的计量数比为1∶1,即M+Cl2====MCl2,故MCl2中M为+2价。
="0.2" mol,故该元素M与Cl2反应的计量数比为1∶1,即M+Cl2====MCl2,故MCl2中M为+2价。
本题难度:简单
5、选择题 相同物质的量浓度、相同体积的KOH溶液,分别使相同体积Fe2(SO4)3溶液、FeSO4溶液反应恰好完全沉淀,则FeSO4溶液、Fe2(SO4)3溶液的物质的量浓度之比为
[? ]
A.3:2
B.1:3
C.3:1
D.1:1
参考答案:C
本题解析:
本题难度:简单