微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 短周期金属元素甲~戊在元素周期表中的相对位置如右表所示:

下面判断正确的是
A.原子半径: 丙<丁<戊? B金属性:甲>丙?
C.氢氧化物碱性:丙>丁>戊? D.最外层电子数:甲>乙
参考答案:C
本题解析:同周期自左向右原子半径逐渐减小,金属性逐渐减弱,最高价氧化物的水化物的碱性逐渐减弱,A不正确,C正确。同主族自上而下金属性逐渐增强,B不正确。同周期自左向右最外层电子数逐渐增多,D不正确,答案选C。
本题难度:简单
2、选择题 具有以下结构的原子,一定属于主族元素的是
A.最外层有8个电子的原子
B.最外层电子排布为ns2的原子
C.次外层无未成对电子的原子
D.最外层有3个未成对电子的原子
参考答案:D
本题解析:A不正确,属于0族元素;B不正确,也可能是0族或副族;C不正确,也可能属于副族元素,例如铜元素;最外层有3个未成对电子的原子,一定是第ⅤA族元素,答案选D。
点评:该题是基础性试题的考查,试题注重基础,兼顾能力的培养。该题的关键是熟练掌握元素的核外电子排布以及元素周期表的结构,有利于培养学生的灵活应变能力。
本题难度:一般
3、填空题 A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的1/6;B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍。请填写下列空格:
(1)请写出A的元素符号?;
(2)C的一价阴离子的结构示意图?;
B的原子的结构示意图?;
(3)A、B两元素相比较,A元素的金属性较强,可以验证该结论的实验是(?)。
A.将这两种元素的块状单质分别放入冷水中
B.将这两种元素的单质分别和同浓度的盐酸反应
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试液?
D.比较这两种元素的气态氢化物的热稳定性
参考答案:(1)Mg? (2)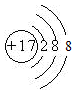 ?
?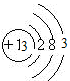 ?(3)BC
?(3)BC
本题解析:A元素有三个电子层,其中最外层电子数占总电子数的1/6,说明A的原子序数是6的倍数,在第三周期元素中,6的倍数的元素有12号元素Mg、18号元素Ar。B元素原子核外电子数比A元素原子核外电子数多1,所以短周期内A只能是Mg,则B是Al;C-离子核外电子层数比A元素的离子核外电子层数多1,则C是第三周期元素Cl;D元素原子最外层电子数是次外层的2倍,说明D是第二周期元素C。
(1)A的元素符号Mg
(2)C的一价阴离子Cl-的结构示意图为 ,B的原子的结构示意图
,B的原子的结构示意图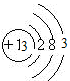
(3)A、镁、铝与冷水不反应,无法判断金属性的强弱,错误;B、与同浓度的盐酸反应,反应剧烈的金属性强,可以判断,正确;C、镁、铝与热水反应,比较反应分快慢及滴入酚酞的颜色变化,可以判断金属性的强弱,正确;D、金属不存在气态氢化物,错误,答案选BC。
本题难度:一般
4、选择题 下列物质属于混合物的是
A.液氯
B.蒸馏水
C.漂白粉
D.冰醋酸
参考答案:C
本题解析:分析:本题考查利用纯净物和混合物的概念来判断物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子为纯净物,否则为混合物.
解答:A、液氯是氯气的液体,是单质为纯净物,故A不符合;
B、蒸馏水是一种物质组成的属于纯净物,故B不符合;
C、漂白粉是氯气和氢氧化钙反应的生成产物为氯化钙和次氯酸钙的混合物,故C符合;
D、冰醋酸是固体醋酸为纯净物,故D不符合;
故选C.
点评:本题考查了纯净物、混合物概念的分析应用,在熟悉概念的基础上能从宏观和微观两个方面来判断纯净物和混合物,还要从社会实践中了解生活中常见物质的组成.
本题难度:困难
5、选择题 根据物质结构和元素周期表进行分析判断,下列叙述不正确的是(?)
A.第15列元素的最高价氧化物为R2O5
B.第三周期元素的离子半径,从左到右逐渐减小
C.同周期第ⅡA族与第IIIA族的元素原子序数之差可能为1或11或25
D.只含有非金属元素的化合物不一定是共价化合物
参考答案:B
本题解析:第15列元素是第ⅤA族元素,最高价是+5价,所以最高价氧化物为R2O5,A正确;第三周期元素的金属阳离子离子半径小于非金属元素的阴离子半径,即选项B不正确;由于从第四周期开始第ⅡA族与第IIIA族中间相隔副族和第Ⅷ族,因此选项C正确;D正确,例如氯化铝是共价化合物,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。主要是考查学生对周期表和元素周期律的熟悉了解程度,特别是灵活运用元素周期律解决实际问题的能力,有利于培养学生的逻辑推理能力,提高学生的应试能力和灵活应变能力。
本题难度:简单