微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氯的含氧酸根有ClO-、ClO2-、ClO3-、ClO4-,其中的Cl原子都是以sp3杂化轨道与O成键。 请回答下列问题:
(1)ClO2-的空间构型是____,写出一个与之构型相同的分子的化学式:____。
(2)下列离子的空间构型与ClO3-相同的是____(填字母,下同)。
A. CO32-
B. SO42-
C. NO3-
D. SiO32-
(3)下列四种酸中,酸性最强的是____。
A. HClO
B. HClO2
C. HClO3
D.HClO4
(4)如果成酸元素R相同,羟基个数不同,则含氧酸的酸性随着分子中连接在中心原子上的非羟基氧的个数的增大而增大, 即(HO)mROn 中n值越大,酸性越强。下列酸中的酸性与HClO3相近的是________ 。
A. H3BO3
B. H3PO4
C. HNO3
D. H2SO3
参考答案:(1)V形;H2O(其他合理答案均可)
(2)B
(3)D
(4)C
本题解析:
本题难度:一般
2、选择题 将pH值相同的盐酸和醋酸稀溶液,分别用蒸馏水稀释至原体积时m倍和n倍后,两溶液的pH值仍然相同,则m和n的关系是( )。
A.m<n
B.m>n
C.m=n
D.无法确定
参考答案:A
本题解析:盐酸为强酸,醋酸为弱酸,若将pH值相同的盐酸和醋酸稀溶液,分别用蒸馏水稀释至原体积的相同倍数后,醋酸溶液的PH更小,若要使稀释后溶液的PH相同,则醋酸加水更多,即.m<n
本题难度:一般
3、选择题 已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O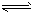 HCl+HClO,HClO
HCl+HClO,HClO 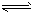 H++ClO-。达平衡后要使HClO浓度增加,可加入
H++ClO-。达平衡后要使HClO浓度增加,可加入
[? ]
A. SO2
B.Na2CO3
C.HCl
D.NaOH
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列哪些能说明醋酸是弱酸的事实( )
(1)醋酸不易腐蚀衣服;
(2)0.1mol/L的CH3COONa溶液的pH约为9;
(3)进行中和滴定时,等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多;
(4)0.1mol/L的CH3COOH溶液pH约为2.9;
(5)相同体积的pH均等于4的盐酸和CH3COOH溶液,被同一物质的量浓度的NaOH溶液中和,CH3COOH溶液消耗的NaOH溶液多;
(6)镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠可以降低反应速率但不改变产生气体的总量.
A.(2)(4)(5)(6)
B.(2)(3)(5)(6)
C.(3)(4)(5)(6)
D.全是
参考答案:(1)醋酸不易腐蚀衣服,只能说明醋酸为酸,不能说明为弱酸,故(1)不选;
(2)0.1mol/L的CH3COONa溶液的pH约为9,有弱才水解,水解显碱性,则醋酸为弱酸,故(2)选;
(3)等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多,是因硫酸为二元酸,不能说明醋酸为弱酸,故(3)不选;
(4)0.1mol/L的CH3COOH溶液pH约为2.9,说明醋酸电离不完全,存在电离平衡,则说明醋酸为弱酸,故(4)选;
(5)相同体积的pH均等于4的盐酸和CH3COOH溶液,被同一物质的量浓度的NaOH溶液中和,CH3COOH溶液消耗的NaOH溶液多,说明醋酸的浓度大于10-4mol/L,即醋酸为弱酸,
故(5)选;
(6)镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠可以降低反应速率是因氢离子结合醋酸根离子结合生成弱电解质醋酸,醋酸的电离是不完全的,随反应的进行醋酸在持续电离,则醋酸为弱电解质,故(6)选;
故选A.
本题解析:
本题难度:简单
5、选择题 H2A为弱电解质,0.1mol/LH2A水溶液加水稀释为0.01mol/L时,下列各粒子的浓度减小最多的是( )
A.A2-
B.HA-
C.H+
D.H2A
参考答案:H2A溶液中存在:H2A?HA-+H+,HA-?A2-+H+,加水稀释,促进电解质电离,n(H2A)减小,n(HA-)、n(H+)、n(A2-)增大,由于体积增大程度大于电离程度,则c(H2A)、c(HA-)、c(H+)、C(A2-)都减小,但溶液中还存在水的电离,则c(H+)>c(CH3COO-)>c(CH3COOH),根据Kw=c(H+)?c(OH-),可知c(OH-)浓度增大,
所以微粒浓度减小得最多的是H2A.
故选D.
本题解析:
本题难度:简单